Cytomegalovirus (CMV) infekce u pacientů s HIV/AIDS a diagnostických hodnot CMV-DNA detekce napříč různými typy vzorků
- Úvod
- metody
- subjekty
- inkluze a vyloučení
- Činidel a zařízení
- HIV-RNA kvantifikace
- CD4+ T lymfocytů počítání
- kvantifikace CMV-DNA
- CMV protilátek test
- Studie metody
- detekce Nukleové kyseliny
- Detekce T-lymfocytů podskupin
- Detekce imunitních protilátek
- Statistická analýza
- Výsledky
- Obecné údaje
- Pozitivní sazby z CMV-DNA CMV-IgG a CMV-IgM
- Korelace mezi CMV infekce andCD4+ T lymfocytů
- Detekce CMV-DNA v různých vzorcích
- Diskuse
- závěry
- Poděkování
- Poznámka
Úvod
Cytomegalovirus (CMV) je společný herpesvirus, který je rozšířený v celé lidské populaci. Infekce CMV obvykle nezpůsobuje příznaky a postihuje hlavně slinné žlázy, ledviny a další orgány. K replikaci viru však může dojít u imunokompromitovaných pacientů a může přispívat k poškození orgánů a jejich funkcí. Oportunní infekce jsou častější a závažnější u pacientů s HIV / AIDS. Infekce virem CMV je u těchto pacientů běžná a může ovlivnit více orgánů/systémů včetně očí, plic, nervového systému a trávicího systému. Mnoho studií zkoumalo virologické a imunologické charakteristiky jednoduché infekce CMV (1), zejména těch, které se vyskytují u žen a dětí. Imunologické rysy infekce CMV jsou však zcela jedinečné u již imunokompromitovaných pacientů s HIV / AIDS. Existují rozdíly v klinických charakteristikách, léčebných opatřeních, prognostických faktorech mezi pacienty s HIV s infekcí CMV a pacienty s infekcí CMV samotnou (2). Pokyn Číny doporučeno, aby okamžitě antivirové terapie CMV a UMĚNÍ jsou potřebné v těch HIV/AIDS, pacienti s komplikacemi (retinitis, zápal plic, CMV encefalitida, enteritida, atd.) při identifikaci infekce CMV. Vzhledem k nespecifičnosti klinických příznaků způsobených infekcí CMV je laboratorní vyšetření hlavním základem pro diagnostiku infekce CMV. Nejvíce dva široce používané klinické metody jsou CMV replikaci viru a séra imunologických metod, včetně detekce CMV IgG, CMV IgM a CMV antigenu PP65 (2) U pacientů s poruchou funkce imunitního systému, produkce CMV protilátek je oslabena nebo opožděné, což může vést k falešně negativní a zvýšit rychlost minul diagnózy, pro ně PCR detekce CMV-DNA je do značné míry stala standardní metodou pro diagnostiku CMV infekce a monitorování léčby (3). Daisuke Mizushima et al. uvádí se, že plazmatická CMV-DNA PCR má důležitou hodnotu v diagnostice jak pro CMV retinitidu, tak pro všechny CMV-EOD u pacientů s pokročilou infekcí HIV-1 (4). CMV-DNA PCR lze detekovat v různých typech vzorků, jako je plazma, moč, mozkomíšní mok, komorová voda, výkaly atd. (5). Nicméně, několik článků analyzovalo a diskutovalo o významu a hodnotě detekce PCR CMV-DNA ve vzorcích jiných než plazma. V této studii jsme retrospektivně analyzovali laboratorní testy (včetně CMV-DNA, CMV protilátky, počtu CD4+ T lymfocytů, virové zátěže HIV atd.) u 808 pacientů s HIV / AIDS, kteří byli léčeni v našem centru v letech 2017 až 2019, aby pochopili koinfekci CMV a silné a slabé stránky několika detekčních metod. Předkládáme následující článek / případ v souladu s kontrolním seznamem hlášení MDAR (k dispozici na http://dx.doi.org/10.21037/apm-20-1352).
metody
subjekty
bylo zařazeno celkem 808 pacientů s HIV / AIDS přijatých do našeho Centra mezi lednem 2017 a říjnem 2019. U každého pacienta byly měřeny HIV-RNA, počet CD4+ T lymfocytů, CMV-DNA a příbuzné protilátky. Diagnóza infekce HIV byla založena na HIV/AIDS, Diagnostika a Léčba Pokyny (třetí vydání) (6), a u všech pacientů byly potvrzeny jako HIV infekce do Fuzhou Městského Centra pro Kontrolu Nemocí (CDC) nebo místní CDC, které léčit pacienta. Diagnostika infekce CMV byla na základě následujících kritérií: (I) CMV-DNA pozitivní v plazmě, alveolární laváže tekutiny, moči, mozkomíšního moku (CSF), a/nebo jiných tělesných tekutin; (II) v séru CMV-imunoglobulin M (IgM) kladná; (III) oftalmologické diagnózy CMV retinitidy; (IV) CMV pneumonie hlavně projevující se jako rýma, kašel, hlen, a pocit tíhy na hrudi; CMV-DNA pozitivní alveolární laváže tekutiny; (V) CMV enteritida nebo ezofagitida hlavně projevující se jako dysfagie/polykání bolest, průjem nebo bolest břicha, a účinná diagnostika anti-CMV léčba; (VI) CMV encefalitida projevuje jako příznaky nervového systému a CMV-DNA pozitivní CSF nebo mozkovou tkáň; (VII) CMV hepatitida, projevující se jako horečka, abnormální funkce jater, a nepohodlí v oblasti jater, a CMV-DNA pozitivní biopsie jater. Diagnóza infekce CMV byla provedena, pokud bylo splněno kterékoli z výše uvedených kritérií kromě bodu II) nebo pokud byla splněna položka II) plus jakékoli jiné kritérium (7).
všechny postupy provedené v této studii zahrnující lidské účastníky byly v souladu s Helsinskou deklarací (revidovanou v roce 2013). Studie byla schválena lékařskou etickou komisí našeho centra (schválení č. KS2019-070-01). Údaje jsou anonymní, a proto bylo upuštěno od požadavku na informovaný souhlas.
inkluze a vyloučení
kritéria pro zařazení: pacientů s HIV/AIDS, který poprvé navštívil Mengchao Hepatobiliární Nemocnice Fujian Lékařské Univerzity a úspěšně absolvováno detekci HIV-RNA, CMV-DNA CMV-IgG protilátky proti CMV-IgM protilátek a CD4+ T lymfocytů do 14 dnů. Vyloučit případy HIV / AIDS, které nemohou dokončit výše uvedené testovací položky z důvodu nedostatečné velikosti vzorku.
Činidel a zařízení
HIV-RNA kvantifikace
Fluorescenční kvantitativní real-time polymerázové řetězové reakce (PCR) (FQ-PCR) byla provedena na Mx3000p QPCR systému (Agilent, USA) pomocí HIV-RNA kvantifikace kit produkován QiaGen (Shenzhen, Čína).
CD4+ T lymfocytů počítání
nástroje byl použit průtokový cytometr FACSCalibur (BD Biosciences, USA) a činidlo byl použit BD Multitest CD3/CD4/CD8/průkazu cd45 (BD Biosciences, USA).
kvantifikace CMV-DNA
FQ-PCR byla provedena na systému MX3000P QPCR (Agilent, USA) k detekci hladin CMV-DNA v plazmě, moči a CSF. Použitá souprava byla vyrobena společností Sansure Biotech (Hunan, Čína).
CMV protilátek test
Chemiluminiscenční imunoanalýza byla provedena pro detekci anti-CMV-IgG a IgM protilátky na Cobas e601 analyzer (Roche Diagnostics, Německo) s nosnou kit (Roche Diagnostics, Německo).
Studie metody
detekce Nukleové kyseliny
Po HIV/AIDS pacienti byli přijati do naší nemocnice, 3 mL půstu kyseliny ethylendiamintetraoctové (EDTA)-antikoagulované plné krvi vzorku bylo odebráno a poté centrifugována při 3 000 ot/min po dobu 5 minut, aby sklizeň 200 µL plazmy HIV-RNA a CMV-DNA detekce. U všech pacientů bylo ráno odebráno 5 mL vzorku moči a důkladně promícháno a poté bylo odebráno 200 µL pro detekci CMV-DNA. U pacientů s neurologickými příznaky byl získán 1 mL CSF pro detekci CMV-DNA. Podle detekčního limitu a pozitivního úsudku standardu CMV-DNA kit a HIV-RNA kit. Vzorky byly považovány za pozitivní, pokud byla hodnota CMV-DNA vyšší než 400 kopií / mL nebo pokud byla hladina HIV-RNA vyšší než 500 kopií / ml.
Detekce T-lymfocytů podskupin
V HIV/AIDS pacientů, 3 mL EDTA-antikoagulancia, půst celý krevní vzorek byl odebrán na vstupné a pak důkladně promíchat pro T-lymfocytů podmnožina detekce na BD FACSCalibur flow cytometr pomocí pomocných činidel.
Detekce imunitních protilátek
V HIV/AIDS pacientů, 3 mL půstu krevní vzorek byl odebrán na vstupné, odstředěny při 3 000 ot/min po dobu 5 minut v séru trubky s gel oddělovač, a pak testovány na stroji.
Všechny výše uvedené testy byly prováděny striktně v souladu s činidlem podle pokynů v návodu výrobce a standardní operační postupy, nástroje.
Statistická analýza
Statistická analýza byla provedena pomocí softwaru SPSS 21.0. Normálně distribuovaná data měření jsou prezentována pomocí střední ± směrodatné odchylky (x ±SD) a normálně distribuovaná data jsou vyjádřena jako medián (25-75 percentilů). Údaje o počtu jsou vyjádřeny v procentech a sazbách. Srovnání běžně distribuovaných dat měření mezi dvěma skupinami bylo provedeno pomocí neparametrického testu rank sum, zatímco údaje o počtu byly porovnány pomocí testu chí-kvadrát. Hodnota P <0,05 byla považována za statisticky významnou.
Výsledky
Obecné údaje
obecné údaje o 808 pacientů s HIV/AIDS jsou shrnuty v Tabulce 1. Pohlaví a věk neprokázaly žádný významný rozdíl mezi skupinou CMV a skupinou bez CMV. Absolutní počet CD4 u CMV infikovaných skupina byla výrazně nižší než v CMV-neinfikované skupiny (Z=-8.87, P<0, 001) a HIV-RNA v plazmě byla významně vyšší u CMV infikovaných, než ve skupině non-CMV infikovaných skupiny (Z=-3.207, P<0.05) (Tabulka 1).
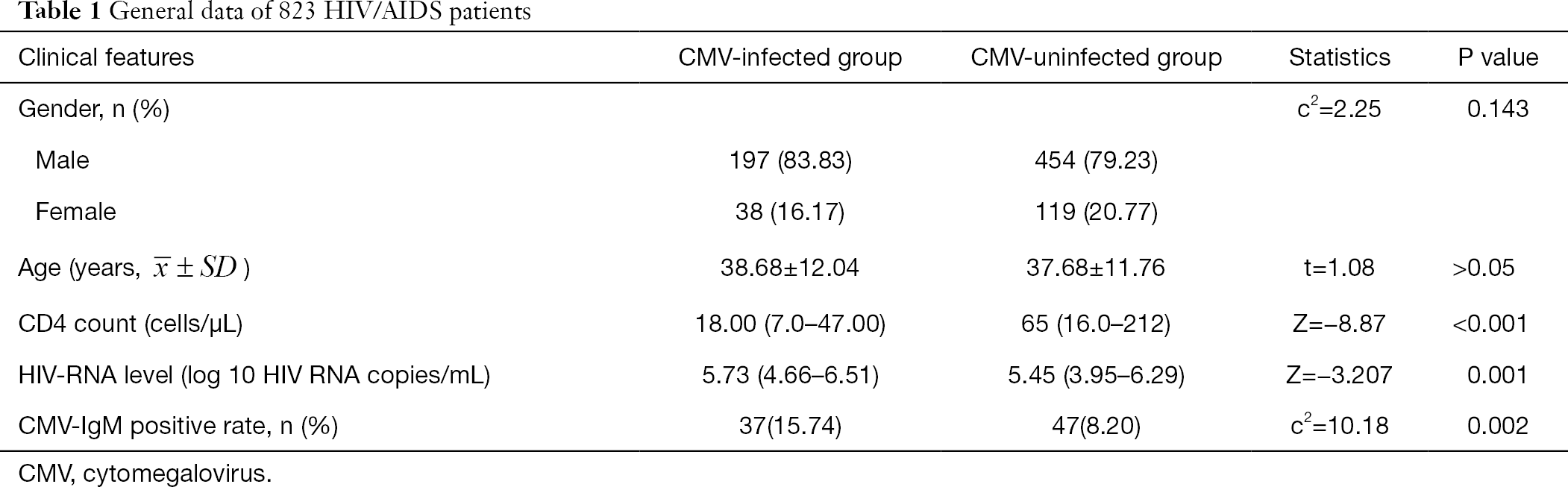
Plné tabulky
Pozitivní sazby z CMV-DNA CMV-IgG a CMV-IgM
celkový pozitivní sazba z CMV-DNA byla 29.08% (235/808); konkrétně to byl 5.70% (13/228) v CSF 26.01% (77/296) v plazmě, a 25.75% (180/699) v moči. Pozitivní míra CMV-IgG byla 99,8% (806/808), a pozitivní sazba z CMV-IgM byla 10.40% (84/808).
Korelace mezi CMV infekce andCD4+ T lymfocytů
Po seskupení CD4+ T lymfocytů jsme zjistili, že podíl pacientů infikovaných s cytomegalovirus na nízké frekvence CD4+ T lymfocytů byla větší, než non-CMV infikovaných pacientů. Incidence infekce CMV se zvyšovala s poklesem počtu CD4 (Tabulka 2).
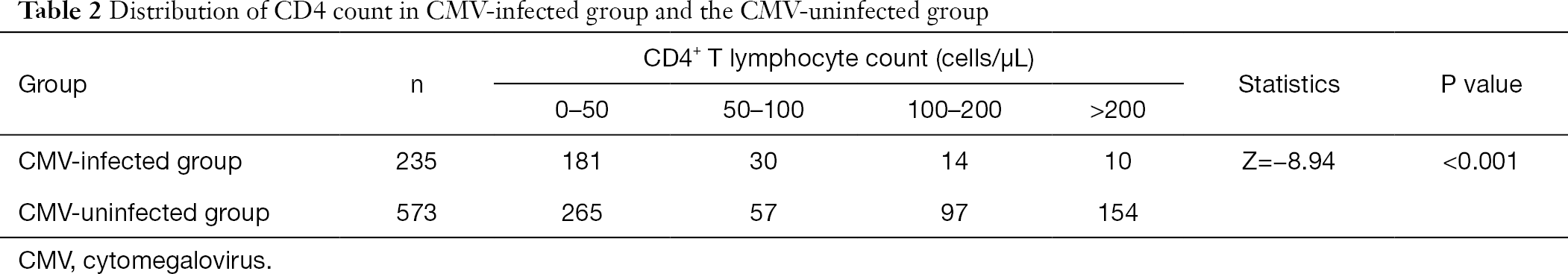
Plné tabulky
Detekce CMV-DNA v různých vzorcích
Z těchto 808 pacientů, 198 pacientů dostávalo také testy pro plazmě a moči CMV-DNA a plazmatické anti-CMV-IgG a CMV-IgM protilátek. Pomocí analýzy chí-kvadrát pro párová data, provedli jsme párová srovnání CMV-DNA v moči a plazmatické CMV-DNA s plazmatickou CMV-IgM protilátkou, resp. Bylo zjištěno, že výsledky z moči a plazmy CMV-DNA detekce výrazně lišily od plasma CMV-IgG protilátek (P<0.001), vzhledem k tomu, že výsledkem plasma CMV-DNA detekce byla výrazně neliší od moči CMV-DNA detekce (P>0.05) (Tabulka 3,4).

Plný stůl
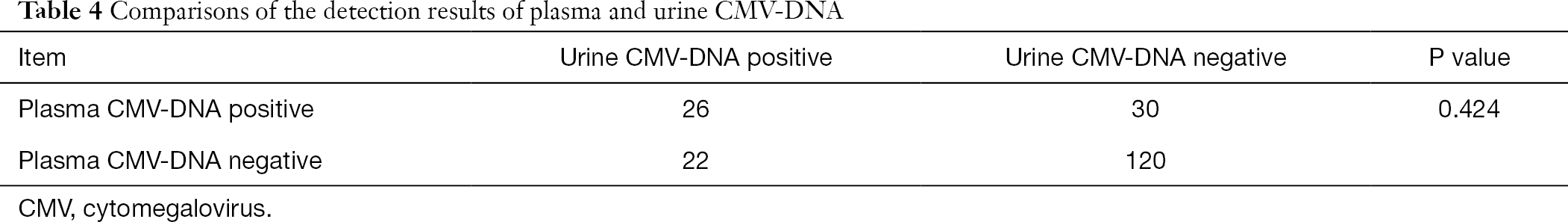
Plné tabulky
Diskuse
CMV je člen β-herpes virus skupiny a se vyznačuje přísnou druhovou specificitu a rozšířený výskyt v lidské populaci. SÉROPREVALENCE CMV je asi 85% u dětí a až 95% u dospělých. V naší současné studii dosáhla pozitivní míra CMV-IgG 99,8%. CMV je latentní ve většině případů, ale u imunokompromitovaných jedinců se virus množí exponenciálně a šíří se po celém těle s krví, což způsobuje CMV virózy a dokonce i organické CMV onemocnění (8). Infekce CMV je jednou z běžných oportunních infekcí u pacientů s HIV / AIDS. CD4+ T lymfocyty jsou cílovými buňkami viru HIV a jejich počty mohou často odrážet průběh AIDS a mohou být také použity jako indikátor pro hodnocení imunitního stavu pacientů s AIDS. Tato studie analyzovala CMV infekci, počet CD4 a hladinu HIV-RNA u 808 pacientů s HIV / AIDS. Zjistili jsme, že pozitivní míra CMV u pacientů s AIDS se zvyšovala s poklesem počtu CD4 a se zvýšením virové zátěže HIV. Také v naší současné studii, a to až do 77.02% CMV-pozitivní pacienti měli počet CD4 <50 buněk/µL, což naznačuje, že CD4 <50 buněk/µL je rizikový faktor pro HIV-CMV coinfection, což je v souladu s nálezem Deng et al. (9). Kvantitativní úroveň HIV-RNA v CMV infikovaných skupině byla vyšší, než ve CMV neinfikované skupiny, které nepřímo naznačují, že vysoké hladiny HIV-RNA virové zátěže byl dalším rizikovým faktorem pro CMV infekci u HIV/AIDS pacientů .Proto se doporučuje, aby pacienti s HIV/AIDS by měla zahájit UMĚNÍ léčbu co nejdříve, aby podporovaly imunitní rekonstituce, aby se zabránilo oportunní infekce a screening pro HCMV je zásadní pro HIV/AIDS pacientů se počet CD4 <50 buněk/µL (2).
hodnotili jsme také hodnoty testů virových nukleových kyselin a imunologických metod v klinické detekci CMV infekce. Studie v Číně a na mezinárodní úrovni ukázaly, že CMV-DNA se objevuje dříve než klinické příznaky a sérologické reakce infekcí CMV. FQ-PCR je v současné době nejpřesnější a nejrychlejší metodou mikrobiální kvantifikace a je schopna překonat některé problémy tradiční PCR (např. V naší současné studii, pozitivní míra CMV-DNA byla 5.70% (13/228) ve vzorcích mozkomíšního moku u 228 pacientů s neurologickými příznaky, které byly mnohem nižší než u vzorků plazmy a moči, což lze vysvětlit hematoencefalickou bariérou a vnímavostí orgánů. Anti-CMV-IgM protilátek je často používán jako marker aktivní virové infekce; nicméně, pozitivní kurz anti-CMV-IgM protilátek byla pouze 10.40% (84/808) v našich pacientů s HIV/AIDS, která byla nižší než pozitivní sazba CMV infekce hlášeny u non-HIV/AIDS populace (11). Kromě toho, jeho pozitivní sazba špatná dohoda s výsledky detekce nukleové kyseliny, které by mohly být vzhledem k oslabení imunitního systému nebo v důsledku opožděné generace IgM protilátek u pacientů s HIV/AIDS. Proto má detekce protilátek CMV-IgM omezenou roli při screeningu HCMV u pacientů s HIV / AIDS. Navíc, pozitivní míra infekce CMV v 808 pacientů byl 29.05% (235/808) v naší současné studii, která je mírně vyšší než 21.85% uvedlo, Li et al., a může být způsobeno větší rozmanitostí vzorků (včetně plazmy, moči a CSF) odebraných v této studii (12). Pozitivní míra CMV-DNA byla 25.57% v moči a 26.01% v plazmě, rozdíl nebyl statisticky významný. Proto doporučujeme, aby CMV-screening DNA v plazmě a moči by mělo být provedeno při CD4+ T lymfocytů nižší než 200 buněk/µL, zvláště když <50 buněk/µL; kromě toho, detekce CMV-DNA v CSF je vyžadována, pokud je zřejmé, neurologické příznaky nejsou přítomny.
závěry
Závěrem lze říci, že nízký počet CD4+ T lymfocytů a vysoká virová zátěž HIV-1 jsou rizikovými faktory infekce CMV u pacientů s HIV / AIDS. Detekce moči nebo plazmatické CMV-DNA pomocí FQ-PCR je vysoce cenná při screeningu infekce CMV u pacientů s HIV / AIDS, zatímco detekce hladin CMV IgG a CMV IgM v krvi má omezenou klinickou hodnotu. U pacientů s AIDS se doporučuje screening CMV-DNA v krvi nebo moči, aby se včas zabránilo a diagnostikovala infekce CMV a zlepšila se jejich kvalita života.
Poděkování
Financování: Podporovaný Klíčových Klinických Speciální Disciplína Stavební Program Fujian, P. R. C.
Poznámka
Hlášení Kontrolní seznam: autoři dokončili MDAR hlášení kontrolní seznam. K dispozici na http://dx.doi.org/10.21037/apm-20-1352
Sdílení Údajů Prohlášení: Dostupné na http://dx.doi.org/10.21037/apm-20-1352
Střety Zájmů: Všichni autoři dokončili redaktorů lékařských časopisů-icmje jednotný formulář (k dispozici na http://dx.doi.org/10.21037/apm-20-1352). Autoři nemají žádný střet zájmů vyhlašovat.
Etické Prohlášení: autoři jsou zodpovědní za všechny aspekty práce v zajištění toho, že otázky týkající se přesnosti a integrity jakékoliv části práce jsou řádně prošetřeny a vyřešeny. Všechny postupy provedené v této studii zahrnující lidské účastníky byly v souladu s Helsinskou deklarací (revidovanou v roce 2013). Studie byla schválena lékařskou etickou komisí našeho centra (schválení č. KS2019-070-01). Údaje jsou anonymní, a proto bylo upuštěno od požadavku na informovaný souhlas.
Prohlášení o otevřeném přístupu: toto je článek s otevřeným přístupem distribuovaný v souladu s mezinárodní licencí Creative Commons Attribution-NonCommercial-NoDerivs 4.0 (CC BY-NC-ND 4.0), který umožňuje non-komerční replikace a distribuce článek s přísnou podmínkou, že žádné změny nebo úpravy jsou provedeny a originální dílo je řádně citován (včetně vazby jak na formální zveřejnění prostřednictvím příslušných DOI a licence). Viz: https://creativecommons.org/licenses/by-nc-nd/4.0/.
- Yu X, Tong M, He G. účinky cytomegalovirové infekce na regulační imunitní buňky u těhotných žen Číňanů. Žurnál Nosokomiologie. 2017;27:2103-6.
- Národní vědecký a technologický Hlavní Projekt pomáhá oportunistické skupině pro výzkum infekcí během 13. pětiletého plánu. Odborný konsensus o klinické diagnostice a léčbě AIDS komplikovaného cytomegalovirovým onemocněním . Journal of Southwest University (Natural Science Edition): 1-17 .
- Hodowanec AC, Pikis A, Komatsu TE, et al. Léčba a prevence CMV onemocnění u příjemců transplantátu: současné znalosti a budoucí perspektivy. J Clin Pharmacol 2019; 59: 784-98.
- Mizushima D, Nishijima T, Yashiro S, et al. Diagnostická užitečnost kvantitativní plazmatické cytomegalovirové DNA PCR pro onemocnění koncových orgánů cytomegaloviru u pacientů s infekcí HIV-1. Jaromír Jágr 2015; 68:140-6.
- Michaelides A, Liolios L, Glare EM, et al. Zvýšené zatížení DNA lidského cytomegaloviru (HCMV) v leukocytech periferní krve po transplantaci plic koreluje s pneumonitidou HCMV. Transplantace 2001; 72: 141-7.
- infekce neurologie, skupina AIDS čínské lékařské asociace. Pokyny pro diagnostiku a léčbu HIV/AIDS (třetí vydání). Čínský žurnál infekčních nemocí 2015; (10): 577-93.
- Corrales I, Giménez E, Solano C, et al. Výskyt a dynamiku aktivní cytomegalovirové infekce v alogenní transplantaci kmenových buněk pacientů podle jednonukleotidové polymorfismy v dárce a příjemce CCR5, MCP-1, IL-10, a TLR9 geny. J Med Virol 2015; 87: 248-55.
- Tagarro A, Del Valle R, Dominguez-Rodríguez S, et al. Růstové vzorce u dětí s vrozenou cytomegalovirovou infekcí. Pediatr Infect Dis J 2019; 38: 1230-5.
- Teng X, Liu J, Zhang M, et al. Analýza virologických a imunologických charakteristik HIV / AIDS v kombinaci s cytomegalovirovou infekcí. Čínský žurnál nemocniční infekce 2019; 29: 2241-6.
- Kawano Y, Kawada J, Kamya Y, et al. Analýza cirkulujících pacientů s lidským a virovým mikroRNA sin s vrozenou cytomegalovirovou infekcí. J Perinatol 2016; 36: 1101-5.
- Li L, Gao S, Zhang T, et al. Porovnání detekce DNA a IgM detekce lidské cytomegalovirové infekce a diskuse o jejich kombinované aplikační hodnotě. Čínský žurnál experimentální diagnostiky 2015; (1): 78-80.
- Li X, Cao L, Yu C, et al. Studie o infekci cytomegaloviru u pacientů s AIDS. Moderní Preventivní Medicína 2012;39:2278-9.
(anglický Jazyk Editor: J. Gray)