Cytomegalovirus (CMV) – infektion hos HIV/AIDS-patienter og diagnostiske værdier for CMV-DNA-detektion på tværs af forskellige prøvetyper
- introduktion
- metoder
- emner
- inklusion og eksklusion
- reagenser og udstyr
- HIV-RNA-kvantificering
- CD4+ T-lymfocyttælling
- CMV-DNA-kvantificering
- CMV antistof test
- undersøgelsesmetoder
- Nukleinsyredetektion
- påvisning af T-lymfocytundersæt
- påvisning af immunantistoffer
- statistisk analyse
- resultater
- generelle data
- Positive satser for CMV-DNA, CMV-IgG og CMV-IgM
- korrelation mellem CMV-infektion ogcd4+ t-lymfocytantal
- påvisning af CMV-DNA i forskellige prøver
- Diskussion
- konklusioner
- anerkendelser
- fodnote
introduktion
Cytomegalovirus (CMV) er et almindeligt herpesvirus, der er udbredt på tværs af humane populationer. CMV-infektion forårsager normalt ikke symptomer og påvirker hovedsageligt spytkirtlerne, nyrerne og andre organer. Imidlertid kan viral replikation forekomme hos immunkompromitterede patienter og kan bidrage til skader på organer og deres funktioner. Opportunistiske infektioner er hyppigere og mere alvorlige hos HIV/AIDS-patienter. CMV – virusinfektion er almindelig hos disse patienter og kan påvirke flere organer/systemer, herunder øjne, lunger, nervesystem og fordøjelsessystem. Mange undersøgelser har undersøgt de virologiske og immunologiske egenskaber ved simpel CMV-infektion (1), især dem, der findes hos kvinder og børn. De immunologiske træk ved CMV-infektion er imidlertid ret unikke hos allerede immunkompromitterede HIV/AIDS-patienter. Der er forskelle i kliniske egenskaber, behandlingsforanstaltninger, prognostiske faktorer mellem HIV-patienter med CMV-infektion og dem med CMV-infektion alene (2). Kinas retningslinje anbefalede, at der straks kræves antiviral behandling af CMV og ART hos de HIV/AIDS-patienter med komplikationer (retinitis, lungebetændelse, CMV encephalitis, enteritis osv.) når CMV-infektion er identificeret. På grund af ikke-specificiteten af kliniske symptomer forårsaget af CMV-infektion er laboratorieundersøgelse det vigtigste grundlag for diagnosen CMV-infektion. De to mest anvendte kliniske metoder er CMV-virusreplikation og serumimmunologiske metoder, herunder påvisning af CMV IgG, CMV IgM og CMV-antigen PP65 (2) hos patienter med nedsat immunfunktion svækkes eller forsinkes produktionen af CMV-antistof, hvilket kan føre til falsk negativ og øge hastigheden af savnet diagnose, derfor PCR-påvisning af CMV-DNA er stort set blevet standardmetoden til diagnose af CMV-infektion og overvågning af behandling (3). Daisuke Misushima et al. rapporteret, at plasma CMV-DNA PCR har vigtig værdi i diagnosen for både CMV retinitis og alle CMV-EOD hos patienter med avanceret HIV-1-infektion (4). CMV-DNA PCR kan påvises i en række forskellige prøvetyper, såsom plasma, urin, cerebrospinalvæske, vandig humor, afføring osv. (5). Imidlertid har få artikler analyseret og diskuteret betydningen og værdien af CMV-DNA PCR-detektion i andre prøver end plasma. I den foreliggende undersøgelse analyserede vi retrospektivt laboratorietestene (inklusive CMV-DNA, CMV-antistof, CD4+ T-lymfocytantal, HIV-viral belastning osv.) hos 808 HIV / AIDS-patienter, der blev behandlet i vores center fra 2017 til 2019 for at forstå CMV-coinfektion og styrker og svagheder ved flere påvisningsmetoder. Vi præsenterer følgende artikel / sag i overensstemmelse med mdar-rapporteringschecklisten (tilgængelig på http://dx.doi.org/10.21037/apm-20-1352).
metoder
emner
i alt 808 HIV/AIDS-indlagte patienter indlagt på vores center mellem januar 2017 og oktober 2019 blev tilmeldt. HIV-RNA, CD4 + T-lymfocyttal, CMV-DNA og relaterede antistoffer blev målt i hver patient. Diagnosen af HIV-infektion var baseret på hiv / AIDS diagnose og behandlingsretningslinjer (tredje udgave) (6), og alle patienter blev bekræftet som HIV-infektion af Fushou Municipal Centers for Disease Control (CDC) eller den lokale CDC, der behandlede patienten. Diagnose af CMV-infektion var baseret på følgende kriterier: (I) CMV-DNA-positiv i plasma, alveolær skyllevæske, urin, cerebrospinalvæske (CSF) og / eller andre kropsvæsker; (II) serum CMV-immunoglobulin M (IgM) positiv; (III) en oftalmologisk diagnose af CMV retinitis; (IV) CMV-lungebetændelse manifesterer sig hovedsageligt som feber, hoste, slim og tæthed i brystet; CMV-DNA-positiv i alveolær skyllevæske; (V) CMV-enteritis eller esophagitis manifesterer sig hovedsageligt som dysfagi/synkesmerter, diarre eller mavesmerter og effektiv diagnostisk anti-CMV-behandling; (VI) CMV-encephalitis manifesterer sig som nervesystemsymptomer og CMV-DNA-positiv i CSF eller hjernevæv; (VII) CMV-hepatitis manifesterer sig som feber, unormal leverfunktion og ubehag i leverområdet og CMV-DNA-positiv i leveren biopsi. En diagnose af CMV-infektion blev stillet, hvis et af ovenstående kriterier undtagen punkt (II) var opfyldt, eller hvis punkt (II) plus ethvert andet kriterium var opfyldt (7).
alle procedurer udført i denne undersøgelse, der involverede menneskelige deltagere, var i overensstemmelse med Helsinki-erklæringen (som revideret i 2013). Undersøgelsen blev godkendt af det medicinske etiske udvalg i vores center (godkendelse nr. KS2019-070-01). Oplysningerne er anonyme, og kravet om informeret samtykke blev derfor frafaldet.
inklusion og eksklusion
inklusionskriterier: patienter med HIV / AIDS, der først besøgte Mengchao Hepatobiliary Hospital ved Fujian Medical University og afsluttede påvisning af HIV-RNA, CMV-DNA, CMV-IgG-antistof, CMV-IgM-antistof og CD4+ T-lymfocytter inden for 14 dage. Ekskluder HIV / AIDS-tilfælde, der ikke kan gennemføre ovenstående testelementer på grund af utilstrækkelig prøvestørrelse.
reagenser og udstyr
HIV-RNA-kvantificering
fluorescerende kvantitativ realtidspolymerasekædereaktion (PCR) blev udført på MKS3000P-KPCR-systemet (Agilent, USA) ved hjælp af HIV-RNA-kvantificeringssæt produceret af Chiagen (Kina).
CD4+ T-lymfocyttælling
det anvendte instrument var FACSCalibur-strømningscytometeret (BD Biosciences, USA), og det anvendte reagenssæt var BD Multitest CD3/CD4/CD8/CD45 (BD Biosciences, USA).
CMV-DNA-kvantificering
PCR blev udført på Mks3000p-systemet (Agilent, USA) for at detektere CMV-DNA-niveauerne i plasma, urin og CSF. Det anvendte sæt blev produceret af Sansure Biotech (Hunan, Kina).
CMV antistof test
Chemiluminescens immunoassay blev udført for at detektere anti-CMV-IgG og IgM antistoffer på Cobas e601 analysatoren (Roche Diagnostics, Tyskland) med understøttende kits (Roche Diagnostics, Tyskland).
undersøgelsesmetoder
Nukleinsyredetektion
efter at HIV/AIDS-patienterne blev indlagt på vores hospital, blev 3 mL fastende ethylendiamintetraeddikesyre (EDTA)-antikoaguleret fuldblodsprøve opsamlet og derefter centrifugeret ved 3.000 r/min i 5 minutter for at høste 200 liter plasma til HIV-RNA og CMV-DNA-detektion. Hos alle patienter blev 5 mL urinprøve opsamlet om morgenen og blandet grundigt, og derefter blev 200 liter høstet til CMV-DNA-detektion. For patienter med neurologiske symptomer blev 1 mL CSF opnået til CMV-DNA-detektion. I henhold til detektionsgrænsen og den positive vurderingsstandard for CMV-DNA-kit og HIV-RNA-kit. Prøverne blev betragtet som positive, hvis CMV-DNA-værdien var over 400 kopier/mL, eller hvis HIV-RNA-niveauet var over 500 kopier/mL.
påvisning af T-lymfocytundersæt
hos HIV/AIDS-patienterne blev 3 mL EDTA-antikoaguleret fastende helblodprøve opsamlet ved indlæggelse og derefter blandet grundigt til T-lymfocytundersætsdetektion på et Bd FACSCalibur-strømningscytometer ved hjælp af de supplerende reagenser.
påvisning af immunantistoffer
hos HIV/AIDS-patienterne blev 3 mL fastende blodprøve opsamlet ved optagelse, centrifugeret ved 3.000 r/min i 5 minutter i et serumrør med gelseparator og derefter testet på maskinen.
alle ovennævnte test blev udført strengt i overensstemmelse med reagensinstruktionerne i producentens manual og instrumentets standardprocedurer.
statistisk analyse
statistisk analyse blev udført ved hjælp af SPSS 21.0-programmer. De normalt distribuerede måledata præsenteres ved hjælp af gennemsnitlig standardafvigelse ( SD), og ikke-normalt distribuerede data udtrykkes som median (25-75 percentiler). Tælledataene udtrykkes i procent og satser. Sammenligningen af de ikke-normalt distribuerede måledata mellem to grupper blev udført ved hjælp af en ikke-parametrisk rank sum-test, hvorimod tælledataene blev sammenlignet ved hjælp af Chi-firkantet test. En p-værdi på <0,05 blev betragtet som statistisk signifikant.
resultater
generelle data
de generelle data for 808 HIV/AIDS-patienter er opsummeret i tabel 1. Køn og alder viste ingen signifikant forskel mellem CMV-gruppen og ikke-CMV-gruppen. Det absolutte CD4-tal i den CMV-inficerede gruppe var signifikant lavere end i den CMV-uinficerede gruppe (å=-8,87, P<0,001), og HIV-RNA-niveauet var signifikant højere i den CMV-inficerede gruppe end i den ikke-CMV-inficerede gruppe (å=-3,207, P<0,05) (tabel 1).
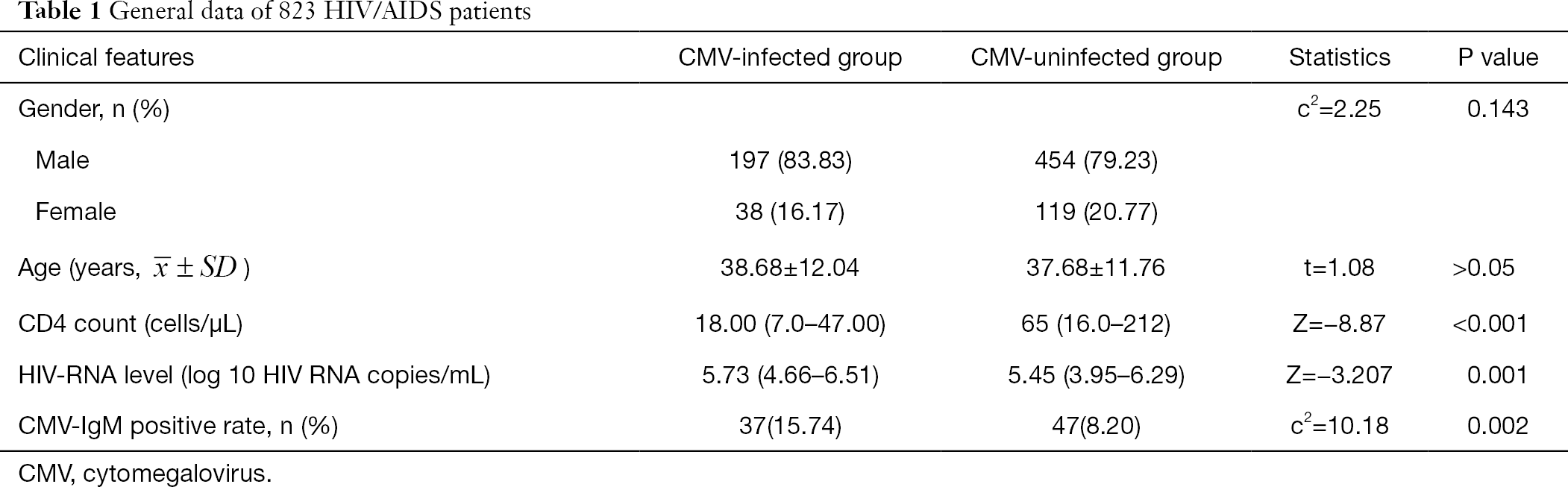
fuld tabel
Positive satser for CMV-DNA, CMV-IgG og CMV-IgM
den samlede positive rate af CMV-DNA var 29,08% (235/808); specifikt var det 5,70% (13/228) i CSF 26,01% (77/296) i plasma og 25,75% (180/699) i urin. Den positive rate af CMV-IgG var 99,8% (806/808), og den positive rate af CMV-IgM var 10,40% (84/808).
korrelation mellem CMV-infektion ogcd4+ t-lymfocytantal
efter gruppering af CD4+ T-lymfocytantalet fandt vi, at andelen af patienter inficeret med cytomegalovirus ved lav frekvens af CD4+ T-lymfocyt var større end for ikke-CMV-inficerede patienter. Forekomsten af CMV-infektion steg med faldet i CD4-antallet (tabel 2).
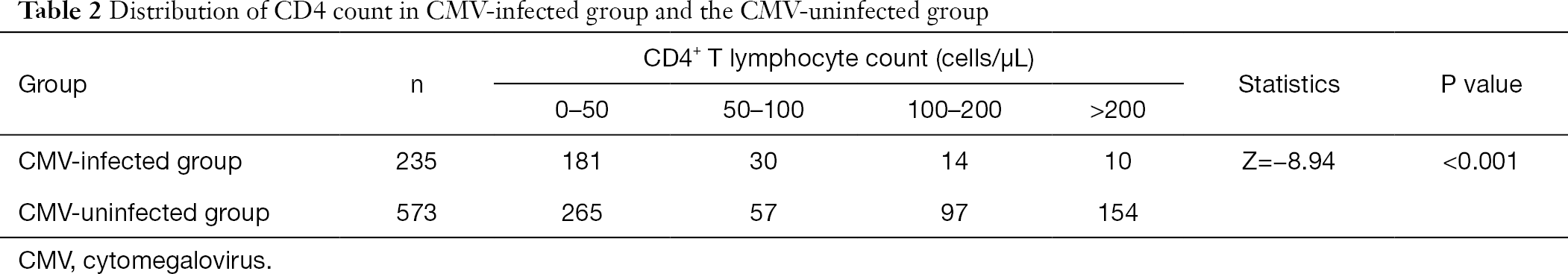
fuld tabel
påvisning af CMV-DNA i forskellige prøver
af disse 808 patienter modtog 198 patienter også test for plasma-og urin CMV-DNA og plasma-anti-DNA-CMV-IgG og CMV-IgM antistoffer. Ved at bruge Chi-kvadratisk analyse for parrede data, vi udførte parvise sammenligninger af urin CMV-DNA og plasma CMV-DNA med plasma CMV-IgM antistof, henholdsvis. Det blev fundet, at resultaterne af urin-og plasma-CMV-DNA-detektion signifikant adskiller sig fra resultaterne af plasma CMV-IgG-antistofassay (P<0,001), mens resultatet af plasma CMV-DNA-detektion ikke var signifikant forskelligt fra resultatet af urin CMV-DNA-detektion (P>0,05) (tabel 3,4).

fuld tabel
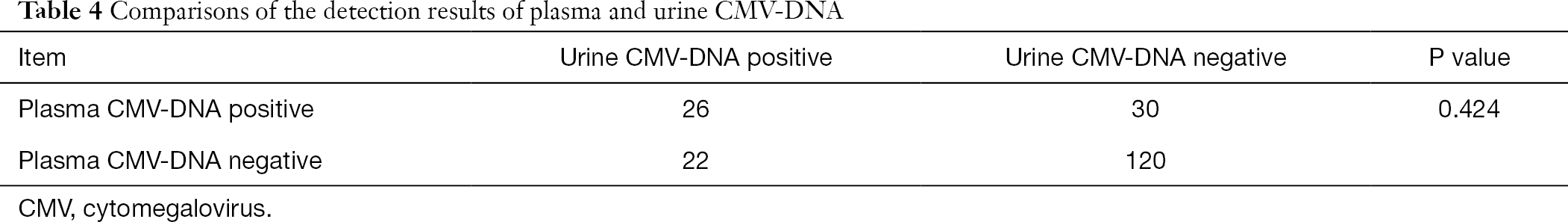
fuld tabel
Diskussion
CMV er medlem af gruppen af herpesvirus og er kendetegnet ved dens strenge artsspecificitet og udbredt forekomst i humane populationer. CMV seroprevalens er omkring 85% hos børn og op til 95% hos voksne. I vores nuværende undersøgelse nåede den positive rate af CMV-IgG 99,8%. CMV er latent i de fleste tilfælde, men hos immunkompromitterede individer replikerer virussen eksponentielt og spreder sig gennem kroppen med blodet, hvilket forårsager CMV-viræmi og endda organisk CMV-sygdom (8). CMV-infektion er en af de almindelige opportunistiske infektioner hos HIV/AIDS-patienter. CD4 + T-lymfocytter er målcellerne for HIV-virus, og deres tællinger kan ofte afspejle AIDS-forløbet og kan også bruges som en indikator til evaluering af AIDS-patienters immunstatus. Denne undersøgelse analyserede CMV-infektion, CD4-antal og HIV-RNA-niveau hos 808 patienter med HIV/AIDS. Vi fandt ud af, at den positive rate af CMV hos AIDS-patienter steg med faldet i CD4-tælling og med stigningen i HIV-viral belastning. Også i vores nuværende undersøgelse havde op til 77,02% af CMV-positive patienter et CD4-tal på <50 celler/larrl, hvilket tyder på, at CD4 <50 celler/larrl er en risikofaktor for HIV-CMV-coinfektion, hvilket er i overensstemmelse med fundet af Deng et al. (9). Det kvantitative niveau af HIV-RNA i CMV-inficeret gruppe var højere end i CMV-uinficeret gruppe, hvilket indirekte antydede, at høje niveauer af HIV-RNA-viral belastning var en anden risikofaktor for CMV-infektion hos HIV/AIDS-patienter .Derfor anbefales det, at patienter med HIV/AIDS indleder ART-behandling så hurtigt som muligt for at fremme immunrekonstitution for at forhindre opportunistiske infektioner, og screening for HCMV er afgørende for HIV/AIDS-patienter med et CD4-tal på <50 celler/rolil (2).
vi vurderede også værdierne af virale nukleinsyreanalyser og immunologiske metoder i den kliniske påvisning af CMV-infektion. Undersøgelser i Kina og internationalt har vist, at CMV-DNA forekommer tidligere end de kliniske symptomer og serologiske reaktioner af CMV-infektioner. PCR er i øjeblikket den mest nøjagtige og hurtige mikrobielle kvantificeringsmetode og er i stand til at overvinde nogle problemer med traditionel PCR (f.eks. amplifikationsproduktforurening og ikke-kvantificering) (10). I vores nuværende undersøgelse var den positive rate af CMV-DNA 5.70% (13/228) i CSF-prøverne af 228 patienter med neurologiske symptomer, hvilket var meget lavere end i plasma-og urinprøver, hvilket kan forklares med blod-hjerne-barrieren og organfølsomhed. Anti-CMV-IgM-antistoffet bruges ofte som en markør for aktiv virusinfektion; imidlertid var den positive rate af anti-CMV-IgM-antistoffet kun 10,40% (84/808) hos vores HIV/AIDS-patienter, hvilket var lavere end den positive rate af CMV-infektion rapporteret I ikke-HIV/AIDS-populationer (11). Derudover havde dens positive hastighed dårlig overensstemmelse med resultaterne af nukleinsyredetektion, hvilket kan skyldes det svækkede immunsystem eller på grund af den forsinkede generation af IgM-antistoffer hos HIV/AIDS-patienter. Derfor har påvisning af CMV-IgM-antistof en begrænset rolle i HCMV-screening hos HIV/AIDS-patienter. Desuden var den positive rate af CMV-infektion hos 808 patienter 29,05% (235/808) i vores nuværende undersøgelse, hvilket er lidt højere end de 21,85% rapporteret af Li et al., og kan skyldes det større udvalg af prøver (inklusive plasma, urin og CSF) indsamlet i denne undersøgelse (12). Den positive rate af CMV-DNA var 25,57% i urinen og 26,01% i plasma, forskellen var ikke statistisk signifikant. Derfor anbefaler vi, at CMV-DNA-screening i plasma og urin skal udføres, når CD4+ T-lymfocyttallet er mindre end 200 celler/larrl, især når <50 celler/larrl; derudover kræves detektion af CMV-DNA i CSF, hvis åbenlyse neurologiske symptomer er til stede.
konklusioner
afslutningsvis er lavt CD4+ T-lymfocytantal og høj HIV-1 viral belastning risikofaktorer for CMV-infektion hos HIV/AIDS-patienter. PCR er meget værdifuldt ved screening af CMV-infektion hos HIV/AIDS-patienter, mens påvisning af blod CMV IgG og CMV IgM niveauer har begrænset klinisk værdi. Blod eller urin CMV-DNA-screening anbefales til AIDS-patienter for at forebygge og diagnosticere CMV-infektion tidligt og forbedre deres livskvalitet.
anerkendelser
finansiering: sponsoreret af Key Clinical Specialty Discipline Construction Program of Fujian, P. R. C.
fodnote
Rapporteringscheckliste: forfatterne har afsluttet mdar-rapporteringschecklisten. Tilgængelig på http://dx.doi.org/10.21037/apm-20-1352
Data Sharing Statement: tilgængelig på http://dx.doi.org/10.21037/apm-20-1352
interessekonflikter: alle forfattere har udfyldt ICMJE uniform disclosure form (tilgængelig på http://dx.doi.org/10.21037/apm-20-1352). Forfatterne har ingen interessekonflikter at erklære.
etisk Erklæring: forfatterne er ansvarlige for alle aspekter af arbejdet med at sikre, at spørgsmål relateret til nøjagtigheden eller integriteten af enhver del af arbejdet undersøges og løses korrekt. Alle procedurer udført i denne undersøgelse, der involverede menneskelige deltagere, var i overensstemmelse med Helsinki-erklæringen (som revideret i 2013). Undersøgelsen blev godkendt af det medicinske etiske udvalg i vores center (godkendelse nr. KS2019-070-01). Oplysningerne er anonyme, og kravet om informeret samtykke blev derfor frafaldet.
Open Access-erklæring: Dette er en open Access-artikel distribueret i overensstemmelse med Creative Commons Attribution-NonCommercial-NoDerivs 4.0 International License (CC BY-NC-ND 4.0), som tillader ikke-kommerciel replikering og distribution af artiklen med det strenge forbehold, at der ikke foretages ændringer eller redigeringer, og det originale værk citeres korrekt (inklusive links til både den formelle publikation gennem den relevante DOI og licensen). Se: https://creativecommons.org/licenses/by-nc-nd/4.0/.
- Yu, Tong M, He G. virkninger af cytomegalovirusinfektion på regulatoriske immunceller hos gravide kvinder Kinesisk. Tidsskrift for Nosokomiologi. 2017;27:2103-6.
- det nationale videnskab og teknologi store projekt AIDS opportunistisk infektion forskningsgruppe under den 13.femårsplan. Ekspert konsensus om klinisk diagnose og behandling af AIDS kompliceret med cytomegalovirus sygdom . Tidsskrift for Sydvestuniversitet( Natural Science Edition): 1-17 .
- Hodanec AC, Pikis a, Komatsu TE, et al. Behandling og forebyggelse af CMV-sygdom hos transplantationsmodtagere: nuværende viden og fremtidsperspektiver. J Clin Pharmacol 2019; 59: 784-98.
- Misushima D, Nishijima T, Yashiro S, et al. Diagnostisk anvendelighed af kvantitativ plasma cytomegalovirus DNA PCR til cytomegalovirus endorgansygdomme hos patienter med HIV-1-infektion. J Erhverver Immun Defic Syndr 2015; 68:140-6.
- Michaelides a, Liolios L, Glare EM, et al. Øget humant cytomegalovirus (HCMV) DNA-belastning i perifere blodleukocytter efter lungetransplantation korrelerer med HCMV pneumonitis. Transplantation 2001; 72:141-7.
- infektionen af neurologi, AIDS-gruppen af kinesisk medicinsk forening. HIV / AIDS diagnose og behandling retningslinjer (tredje udgave). Kinesisk Tidsskrift for infektionssygdomme 2015;(10):577-93.
- Corrales I, GIM Larsen E, Solano C, et al. Forekomst og dynamik af aktiv cytomegalovirusinfektion hos allogene stamcelletransplantationspatienter i henhold til enkelt nukleotidpolymorfier i donor-og recipient CCR5 -, MCP-1 -, IL-10-og TLR9-gener. J Med Virol 2015;87: 248-55.
- Tagarro A, Del Valle R, Domingues-Rodr, et al. Vækstmønstre hos børn med medfødt cytomegalovirusinfektion. Pediatr Inficere Dis J 2019;38:1230-5.
- Deng, Liu J, Jang M, et al. Analyse af virologiske og immunologiske egenskaber ved HIV / AIDS kombineret med cytomegalovirusinfektion. Kinesisk Tidsskrift for Hospitalinfektion 2019; 29: 2241-6.
- Kovano Y, Kovada J, Kamya Y, et al. Analyse af cirkulerende humane og virale microRNA sin patienter med medfødt cytomegalovirusinfektion. J Perinatol 2016; 36: 1101-5.
- Li L, Gao S, Jang T, et al. Sammenligning af DNA-detektion og IgM-detektion af human cytomegalovirusinfektion og diskussion af deres kombinerede anvendelsesværdi. Kinesisk Tidsskrift for Eksperimentel diagnostik 2015;(1):78-80.
- Li, Cao L, Yu C, et al. Undersøgelse af infektion af cytomegalovirus hos AIDS-patienter. Moderne Forebyggende Medicin 2012;39:2278-9.
(engelsk Sprogredaktør: J. Gray)