Hvad er Computer System validering, og hvordan gør jeg det rigtigt?

processen med programvalidering sikrer, at systemet passer til den tilsigtede anvendelse og fungerer som det skal. Computersystemvalidering (CSV) til laboratorieinformatik er afgørende, fordi regulerede virksomheder skal sikre deres produkters sikkerhed for forbrugerne, og deres laboratorieinformatiksystemer (LIMS, ELN, CDS) er en integreret del heraf. I betragtning af dets betydning har Validering tendens til at blive betragtet som forvirrende og udfordrende at udføre korrekt. Det er selvfølgelig muligt at gøre det rigtigt, og CSols har bevis. I næsten 30 år med CSV har vi ikke hørt om nogen af vores kunder, der modtager en FDA 483-formular.
Validering er en del af programudviklingens livscyklus. I denne blog gennemgår vi, hvad det betyder, og hvordan du gør det, så dit system kan forsvares i en lovgivningsmæssig revision.
Grundlæggende om Computersystemvalidering
ingen diskussion af validering af computersystemer er komplet uden en oversigt over lovgivningen omkring den. I USA regulerer Food and Drug Administration (FDA) specifikke industrier, der direkte påvirker forbrugernes sundhed, herunder lægemidler, kosmetik og mad og drikke. Disse industrier har et ekstra ansvar for at sikre, at deres produkter er sikre, og deres data er sikre. Den relevante lovgivning, der vedrører aspekter af validering af computersystemer i USA, kommer fra Code of Federal Regulations (CFR), mest specifikt 21 CFR del 11 (Del 11), der beskæftiger sig med elektroniske poster og underskrifter. Lignende offentlige myndigheder og regler gælder også i andre lande.
en del 11 kræver, at kravene til elektroniske poster og underskrifter betragtes som nøjagtige, pålidelig, let hentes, og sikker, at erstatte papirregistre og håndskrevne underskrifter lovligt. Validering af dit computersystem er det primære middel til at bestemme, at elektroniske poster og signaturer kan bruges på denne måde.
valideringsprocessen
Validering kan tage mange former under computersystemets livscyklus, afhængigt af om det er en ny implementering eller en opgradering til et eksisterende system. For nye systemer, som brugeren håber kan løse et aktuelt problem, sker validering fra bunden. For et eksisterende system, der har brug for en opgradering eller udvider omfanget af dets tilsigtede anvendelse, er behovet for at holde systemet i en valideret tilstand ved at teste de nye kapaciteter, inden de frigives til produktionsbrug. Valideringsprocessen slutter, når et system trækkes tilbage, og dets data overføres til et nyt system eller arkiveres. Figuren nedenfor viser, hvordan Validering understøtter projektets livscyklus.

valideringen masterplan
din Validering masterplan guider dig gennem valideringsprocessen og bliver en slags en check-off liste for at sikre, at alt sker som det skal. Når du har vurderet dit systems As-Is-tilstand, omfatter validerings masterplanen alle de andre trin, du vil tage for at sikre, at dit system er valideret i dets nuværende tilstand og egnet til dets tilsigtede anvendelse.

validerings-masterplanen skal tage højde for indsamling af krav, en funktionel risikovurdering, en sporingsmatrice, protokoller og test af KVALITETSSIKRINGSPROTOKOLLER samt ændringskontrolprocedurer med periodiske gennemgange. Hver del af validerings masterplanen udføres i en defineret rækkefølge. Dine krav skal være komplette og risikovurderingen udført, før du går videre til at udvikle spormatricen og derefter udføre testen. På denne måde minimerer du risikoen for at skulle gå tilbage og udvikle nye testsager sent i processen.
forholdet mellem kravindsamling og kvalifikationstest
det er afgørende at sikre, at dine krav og specifikationer er veldefinerede og godkendte, før du validerer computersystemet. Validerings-V-modellen bruges ofte til at visualisere forholdet mellem krav og specifikationer og den test, der udføres på dem (Se diagram nedenfor). Kvalifikationstest (nede i højre side af V) er designet ud fra din tilsigtede brug og den funktionalitet, der kræves for at imødekomme denne brug (repræsenteret nede i venstre side af V).
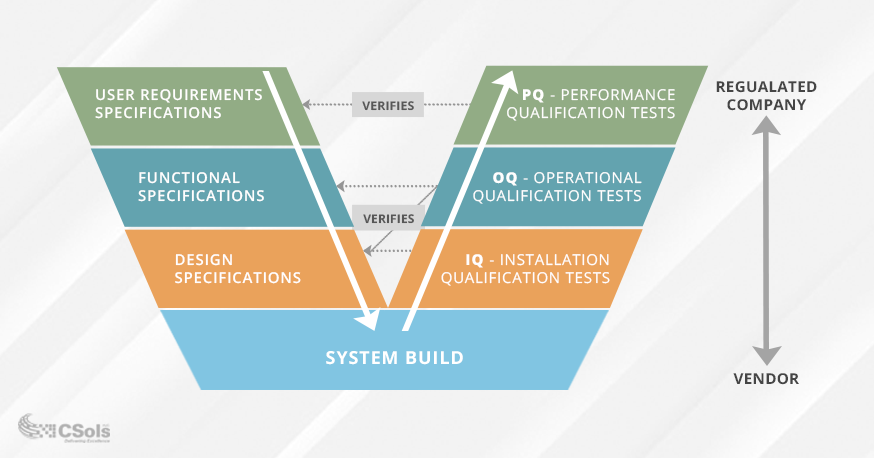
- specifikationen for brugerkrav dokumenterer, hvad brugerne har brug for, at systemet skal gøre, og PK-test verificerer disse krav.
- specifikationen for funktionelle krav dokumenterer den systemfunktionalitet, der kræves for at opfylde specifikationen for brugerkrav, og OK-test verificerer disse specifikationer.
- Designspecifikationerne dokumenterer systemdesignet (f.eks. moduler, enheder osv.), og ik-test kontrollerer, at systemets installation opfylder disse designkrav.
test er uden tvivl en væsentlig del af valideringsprocessen. En vellykket gennemførelse af testen vil kontrollere, at dit system fungerer efter hensigten og er egnet til dets tilsigtede anvendelse i dit miljø. Det er bedste praksis at godkende dine brugerkrav og funktionelle specifikationer inden test for at undgå omfangskrybning og mulig gentestning.
hvis du vil vide mere om vores test, kan du se vores hjemmeside.
de personer, der skriver og udfører din test, skal være grundigt bekendt med dit laboratorieinformatiksystem (LIMS, ELN, CDS) og din tilsigtede anvendelse. Hvis dit interne personale ikke har båndbredde eller erfaring til korrekt test, skal du arbejde med kvalificerede CSV-konsulenter, som CSols, der har den nødvendige erfaring med dine informatiksystemer.
ALCOA+ og dataintegritet
betydningen af laboratorieinformatikdata kan ikke undervurderes. Når du har data i et valideret miljø, skal du sikre dig, at dine data forbliver sikre og pålidelige. Akronymet ALCOA identificerer de fem grundlæggende principper for dataintegritet: data skal kunne henføres, læselig, samtidige, Original, og nøjagtig. For nylig er der tilføjet fire yderligere principper, så akronymet nu er ALCOA+. De fire tilføjelser er komplette, konsistente, varige og tilgængelige.

dataintegritet er en integreret del af alle valideringsaktiviteter. At følge principperne i ALCOA+ sikrer, at dit system indfanger, producerer, rapporterer, overfører og gemmer data, der er sikre, kan hentes efter ønske og pålidelige.
fremtiden for CSV: Computer System Assurance
selvom vi stadig venter på, at FDA frigiver deres forventede vejledning om computer system assurance (CSA), kommer den. I sin kerne styrker CSA en risikobaseret tilgang, der udvider GAMP 5-principperne for produkt-og procesforståelse, kvalitetsrisikostyring og udnyttelse af leverandøraktiviteter. Risiko vurderes ud fra det store billede af den samlede forretningsproces. Dette lægger større vægt på testeffektivitet og fokuserer på test, der sikrer, at systemet er egnet til formålet.
udfordringer med validering af computersystemer
validering af computersystemer kan indebære udfordringer, herunder risikoen for systemfejl, restriktive virksomhedspolitikker og stadig strengere lovkrav. Et andet vigtigt problem er, når brugerne skal afbalancere risikoen vs. omkostningsligningen, efter at risikokategorier er defineret. En risikobaseret tilgang til CSV kan hjælpe med at afbøde nogle af disse udfordringer.
yderligere trin, du kan tage for at undgå valideringsproblemer, inkluderer følgende:
- sikre, at din valideringsplan er færdig og følger branchens bedste praksis og regler
- definition af computersystemet (dvs. udstyr, programmer, personer og processer), der skal valideres
- giver klare grænser for dine forventede resultater; dvs., hvad der er acceptabelt
- beskrivelse og opfyldelse af grundige krav og specifikationer til din tilsigtede brug af programmet
korrekt udførelse af en computersystemvalidering er en involveret proces, men du kan gøre det, når du har den rigtige ekspertise. Hvis du ikke er sikker på, at dit interne personale har den nødvendige CSV-erfaring, skal du kontakte os.