Classification du Sang Humain / Immunologie
ANNONCES:
Le sang humain peut être classé dans différents systèmes de groupes sanguins, par exemple le groupe sanguin ABO, le groupe sanguin MN et le groupe sanguin Rh.
Tous ces groupes sanguins chez l’homme sont sous contrôle génétique, chaque série de groupes sanguins étant sous contrôle de gènes à un seul locus ou de gènes étroitement liés et se comportant dans l’hérédité comme s’ils se trouvaient à un seul locus.
- Groupe sanguin ABO:
- Génétique du groupe sanguin ABO:
- Sous-divisions des groupes sanguins A, AB et B:
- Mode d’héritage:
- Cas Génétiques Particuliers du Groupe Sanguin ABO:
- Groupes sanguins MN:
- Facteur Rh :
- Importance clinique:
- Détails sur le facteur Rh:
- Contrôle génétique de la Structure antigénique:
- Une comparaison schématique des concepts de Wiener et de Fisher-Race:
- Le concept de Weiner de Rh:
- Le concept de Race Fischer de Rh:
- Héritage des facteurs sanguins Rh:
- Importance de développer le Concept Correct des Relations génétiques des antigènes Rh:
Groupe sanguin ABO:
Si l’on considère les réactions immunitaires liées au groupe sanguin ABO, on constate que certaines d’entre elles contiennent des anticorps “naturels” contre d’autres.
ANNONCES:
Voici la teneur en anticorps du groupe sanguin ABO:

De même, si nous considérons la présence d’antigène dans les globules rouges de différentes personnes du groupe sanguin ABO, nous trouvons:
En raison de la présence de différents antigènes et anticorps dans les groupes sanguins de A, B,
ANNONCES:
AB et O, tous les types de sang ne peuvent pas être mélangés en raison de leur réaction d’agglutination comme suit:

Lorsqu’une transfusion sanguine est faite, cela ne nuit pas si le sang du donneur contient des anticorps contre celui du receveur car le sang du donneur est faible en quantité par rapport au volume total du receveur et, par conséquent, les anticorps sont dilués.
Mais cela ferait du mal si le sang du receveur avait les anticorps, car maintenant la quantité d’anticorps est relativement importante. Une personne du groupe sanguin O, par exemple, ne pouvait pas recevoir de sang d’un autre groupe que le sien, car son sérum agglutine tous les corpuscules sauf le sien, bien qu’il puisse être un donneur pour n’importe quel groupe puisque le sang de personne ne contient d’anticorps contre ses corpuscules.
Génétique du groupe sanguin ABO:
Nous ne savons pas lequel des quatre groupes sanguins est le groupe sanguin normal. En génétique, il est généralement admis que les individus ayant des traits normaux sont les plus nombreux que dans tous les autres. Pour une compréhension plus facile, si nous considérons le groupe O comme normal, alors les groupes A et B sont issus du groupe O à la suite de deux mutations dominantes (une pour chaque groupe), le gène mutant peut recevoir les symboles A et B, respectivement. Ces deux gènes sont apparus dans le même locus à partir d’un des gènes normaux du groupe O.
Si nous désignons le gène normal en utilisant le symbole +, alors trois gènes +. A et B occupent le même locus et sont des allèles multiples. Comme le gène + est récessif, le groupe O doit donc être homozygote pour + /+, et comme les gènes mutants A et B sont dominants, les combinaisons pour un groupe soit A / A, soit + / A et de même pour le groupe B, B / B ou + / B. Le groupe sanguin AB, en revanche, est toujours l’hybride
, A / B (C’est un exemple de l’expression phénotypique de la co-dominance).
Certains généticiens ont également proposé que l’hérédité des groupes sanguins A, B, AB et O chez l’homme soit déterminée par une série de trois gènes allélomorphes dont i pour aucun antigène, IA pour l’antigène A, IB pour l’antigène B. IA & IB montrent une domination complète sur i.
Sous-divisions des groupes sanguins A, AB et B:
ANNONCES:
Les globules sanguins d’un groupe sanguin ont été subdivisés en deux sous-groupes appelés A1 et A2, mais parmi ces deux sous-groupes, A2 est moins fréquent. Il a été constaté que les corpuscules A1 ne sont pas agglutinés par le sérum A2, ni l’inverse; mais les corpuscules A1 et A2 sont agglutinés par le sérum B et le sérum O.
Il a également été noté que deux autres sous-groupes de A (mis à part A1 et A2) ont été identifiés qui sont A3 et A4mais ces deux groupes sont plus rares que A2. Chacun des sous-groupes A est déterminé par un gène distinct et les gènes des quatre sous-groupes sont des allèles.
De même, le sérum du groupe B contient au moins deux types d’anticorps, l’un agglutine les corpuscules des groupes A1 et A2 et l’autre agglutine uniquement A1. Le groupe sanguin AB a également été divisé en A1B, A2B, A3B et A4B.
Ainsi, le gène ‘I’ est un allèle multiple (qui détermine la production d’antigènes) et peut produire 15 génotypes et 10 phénotypes de groupes sanguins, qui sont:
Mode d’héritage:
Si les deux parents d’une famille donnée sont du groupe sanguin O, tous les enfants d’entre eux doivent avoir un groupe sanguin O comme leurs parents. Si, d’un autre côté, les deux parents font partie d’un groupe et que les deux sont hybrides (A / +), ils peuvent avoir des enfants avec un groupe sanguin O.
Ainsi, si nous connaissons les groupes sanguins d’un enfant et de sa mère, nous pouvons légitimement revendiquer ou tester le groupe sanguin probable du père de l’enfant.
Le tableau suivant est la forme résumée application médicolégale des groupes sanguins :
ANNONCES:
ANNONCES:
Le tableau suivant (tableau 13.1) est le mode d’héritage du groupe sanguin aux enfants des parents:
Cas Génétiques Particuliers du Groupe Sanguin ABO:
Il a été constaté que certaines personnes ont également des antigènes A ou B dans leurs sécrétions corporelles (des yeux, du nez, de la glande salivaire et de la glande mammaire) et sont connues comme sécrétrices. Les personnes qui sont des sécréteurs ont un antigène soluble dans l’eau qui peut sortir des globules rouges et est donc présent dans les sécrétions corporelles.
Mais dans le cas des non-sécréteurs, les antigènes ne sont que solubles dans l’alcool et ne peuvent pas être dissous dans les sécrétions. Ainsi, les sécréteurs peuvent être identifiés par test sur le sang ainsi que sur les sécrétions corporelles. Ce trait sécréteur est hérité en tant que gène dominant “S” tandis que le trait non sécréteur est hérité par l’allèle récessif homozygote “s”. On estime que près de 77% des populations américaines sont des sécréteurs.
De même, un autre antigène dit antigène ” H “, également identifié sur les érythrocytes qui peut être mis en évidence par des agglutinations par sérum anti-H. On pense que cet antigène est un intermédiaire entre l’antigène A et B. Le gène dominant H est responsable de la production de l’antigène H et les géotypes sont les suivants :
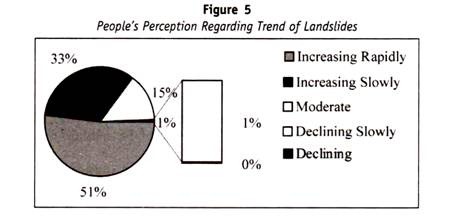
Il est intéressant de noter que les individus dont le sang ne réagit pas avec l’Anti-A ou l’Anti-B ou l’Anti-H appartiennent à un groupe très rare et sont connus sous le nom de “phénotype de Bombay”, car il a été décrit pour la première fois dans un très petit groupe de personnes dans la ville de Bombay.
Groupes sanguins MN:
Les globules sanguins de différentes personnes peuvent contenir l’un ou l’autre, ou les deux M et N et ces antigènes n’ont aucun rapport avec les groupes sanguins ABO. C’est–à-dire qu’une personne du groupe sanguin A peut appartenir à l’un des trois groupes sanguins (M, N ou MN) MN. Le gène responsable de la production des antigènes M et N sont dominants et sont des allèles.
ANNONCES:
Les gènes hétérozygotes pour M et N ont montré une co-dominance. Cependant, ces trois classes (M, N et MN) ne se produisent pas dans un rapport mendélien simple dans la population générale et le pourcentage de chaque classe varie d’une race à l’autre. Le groupe sanguin MN n’a aucune importance dans la transfusion sanguine mais a une importance médicolégale, par exemple un test de paternité. Le tableau suivant (Tableau 13.2) montre le test de paternité pour le groupe sanguin MN.
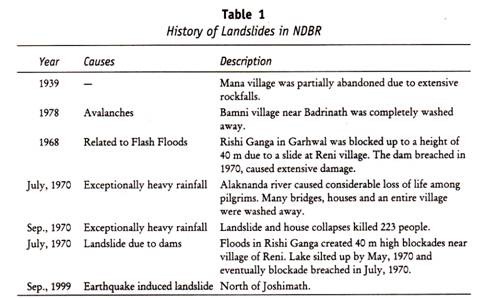
Facteur Rh :
Un agglutinogène important a été mis en évidence (1940) dans les globules rouges humains également par Landsteiner et Wiener. Il est agglutinogène du singe Rhésus et est présent chez 85% des Blancs. Bien que les informations soient limitées, on constate cependant que chez les Indiens et les Ceylonais, la proportion est encore plus importante (environ 95% ou plus). Il n’y a pas d’agglutinine correspondante dans le plasma humain.
Des études récentes indiquent que le facteur Rh n’est pas une entité unique. Il existe six agglutinogènes Rh – C, c; D, d; E, e; parmi ceux-ci, D et osez le plus commun. Ces deux groupes fourniront trois sous-groupes – D, Dd et d. D est à dominante mendélienne, tandis que d est récessif. Par conséquent, les groupes D et Dd (collectivement appelés groupe D) seront Rh positifs (Rh +) et d seront rh négatifs (Rh ~). Pratiquement toutes les personnes Rh positives appartiennent au groupe D et les personnes rh négatives au groupe d.
Importance clinique:
1. Si le sang Rh+ est transfusé à un patient Rh”, un facteur Anti-Rh se développera dans le sang du patient en environ 12 jours. Si une deuxième transfusion du même sang est administrée à un tel patient après cette période, une hémoagglutination des corpuscules du donneur aura lieu. En d’autres termes, le sang qui était compatible avant est devenu incompatible maintenant. De sorte que, avant la transfusion, le test de facteur rh doit être soigneusement effectué.
2. Pendant la grossesse, le fœtus peut être Rh + alors que la mère Rh-. L’agglutinogène Rh (légèrement présent également dans le plasma) du fœtus passe dans le sang maternel et stimule la formation de facteur Anti-Rh. Cet anticorps pénètre dans le sang fœtal et détruit les globules rouges du fœtus. Le fœtus peut mourir (provoquant une fausse couche) ou, s’il naît vivant, souffrir d’anémie sévère. Cette maladie est connue sous le nom d’érythro-blastose fœtale.
3. Une telle mère devient sensibilisée au facteur Rh. À l’avenir, si elle reçoit une transfusion de sang autrement compatible mais contenant du facteur Rh, une agglutination aura lieu.
4. Pour la même raison, une femme Rh “, avant la ménopause, ne devrait pas recevoir de transfusion de sang Rh +. Parce qu’au cas où elle tomberait enceinte d’un fœtus Rh positif, le problème tel que décrit sous no. (2) deviendra d’autant plus aigu.
Les agglutinines spécifiques ne sont pas présentes dans le plasma fœtal. Mais les agglutinines maternelles, filtrées à travers le placenta, se trouvent dans le plasma fœtal. Seulement 50% des nouveau-nés présentent une quantité appréciable de cette agglutinine.
Les agglutinines spécifiques commencent à apparaître vers le 10e jour après la naissance et atteignent leur maximum vers la 10e année. Les agglutinines, comme les autres anticorps, se trouvent dans la fraction globuline du sérum. Ils sont également présents en faibles dilutions dans les fluides corporels riches en protéines, tels que le lait, les exsudats lymphatiques et les transsudats. Ils ne se trouvent pas dans l’urine et le liquide céphalo-rachidien. Les hémoagglutinines augmentent temporairement pendant la maladie sérique et sont réduites dans la leucémie.
Comme les autres anticorps, la concentration d’agglutinine spécifique varie à tous les âges d’un homme à l’autre et même chez un même individu dans des conditions différentes. Ils agissent mieux à une température plus basse.
Le groupe sanguin d’un sujet particulier est de caractère fixe et ne varie pas avec l’âge ou la maladie.
Des agglutinines non spécifiques peuvent parfois apparaître dans le sang qui agissent par temps froid (à 0 °-5 °C ou F) et non à température corporelle. Ces agglutinines froides peuvent parfois être suffisamment élevées pour provoquer une auto-agglutination à la température corporelle. Pour cette raison, il peut y avoir une hémolyse intravasculaire conduisant à une hémoglobinurie (hémoglobinurie paroxysomique).
Détails sur le facteur Rh:
1. Agglutinogènes Rh:
Il existe trois paires d’agglutinogènes Rh C, c; D, d; et E, e; C, D et E sont dominants mendéliens et c, d et e sont récessifs.
2. Globules rouges humains (RBC):
R.B.C. portera toujours trois agglutinogènes – un de chaque paire, mais ils ne porteront jamais les deux membres d’une paire. Ainsi, ODE, CDe et cDE sont possibles mais cDC et CDd ne le sont pas.
3. Groupes Rh (génotypes) :
Il s’ensuit donc qu’il existe 8 combinaisons possibles, dont l’une peut être portée par les deux parents. Par conséquent, mathématiquement, il y a 64 combinaisons possibles (génotypes). Parmi ces 28 étant identiques, 36 sous-groupes sont biologiquement disponibles. Parmi ceux-ci encore une fois, seuls 5 sont couramment trouvés, à savoir, CDe / CDe, CDe / cDe, CDe / cde, cDe / cde et cde / cde. D’autres sont rares.
4. Groupes Rh+ et Rh-:
Ces groupes contenant les agglutinogènes dominants – c’est—à-dire, C, D, E – seront Rh+. Mais comme C et E restent rarement sans D, pratiquement tous les cas Rh + contiennent D, c’est-à–dire appartiennent au groupe D
. Les cas Rh- contiendront les agglutinogènes récessifs – c, d et e et, pour des raisons similaires, l’état 4 ci-dessus appartient au groupe d. Chaque homme porte un agglutinogène Rh. La majorité ont D et sont de Rh +. Les autres portent d et sont de Rh-. Toutes les réactions incompatibles avec le Rh sont dues à des interactions entre le groupe D (donneur) et le groupe d (receveur).
5. Anticorps Rh:
a) Chacun des six agglutinogènes a une propriété antigénique, c’est-à-dire qu’ils peuvent stimuler la formation d’anticorps. Les anticorps correspondants sont appelés Anti-C, Anti-D, etc. D est fortement antigénique, d’autres sont très faibles.
b) Si des cellules D sont injectées à plusieurs reprises dans un sujet Rh “, de l’Anti-D se développera. Cet anticorps peut être de deux types — “précoce” et “tardif”. L’Anti-D précoce est formé en premier et s’appelle anticorps complet. Il peut agglutiner les cellules D in vitro, lorsqu’elles sont en suspension dans une solution saline ou d’albumine. Par conséquent, il est également connu sous le nom d’agglutinine saline. L’Anti-D tardif se forme plus tard et s’appelle anticorps incomplet.
Il peut agglutiner les cellules D in vitro, lorsqu’elles sont en suspension uniquement dans des solutions d’albumine et non dans des solutions salines. Par conséquent, il est également appelé agglutinine d’albumine. Mais dans ce dernier cas, bien que les cellules D ne soient pas agglutinées, elles sont néanmoins quelque peu modifiées. Car, ces cellules, une fois ainsi traitées, ne seront pas agglutinées par le sérum Anti-D précoce, même lorsqu’elles sont en suspension dans une solution d’albumine. Par conséquent, l’Anti-D tardif est également connu sous le nom d’anticorps bloquant.
c) Comme mentionné ci-dessus, D est très fortement antigénique. Il provoque la formation d’Anti-D même par injection intramusculaire; de sorte que les injections intramusculaires répétées de sang total — comme souvent dans la pratique médicale sans correspondre aux groupes sanguins — ne sont pas nécessairement une procédure sûre. Par conséquent, l’appariement direct avant chaque engagement de ce type est la seule garantie la plus sûre.
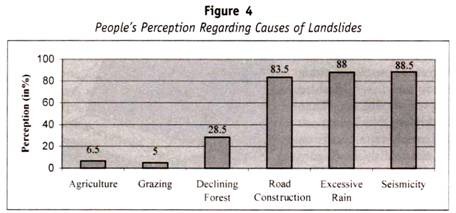
6. Distribution raciale:
Écrire des personnes – 85% Rh +, dont D–35%, Dd-48% et les 2% restants contiennent également D avec un autre agglutinogène. Indiens, Ceylonais – 95% Rh +, Japonais environ 100% Rh + Par conséquent, dans ce dernier cas, les réactions d’incompatibilité Rh sont extrêmement rares.
7. Maladie hémolytique du Nouveau-né :
Cette maladie est due à la destruction du Rh+ R.B.C. chez le fœtus par une agglutinine Anti-Rh, présente dans le sérum de la mère, qui a filtré à travers le placenta pendant la grossesse. L’incompatibilité entre le sang de la mère et de l’enfant est causée par l’héritage du facteur Rh. Le tableau suivant (Tableau 13.3) indique les probabilités du groupe Rh chez l’enfant.
Dans cette maladie, la destruction de la R.B.C. normale entraîne la présence de R.B.C. nucléée anormale dans la circulation. Quelques heures après la naissance, il y a une anémie, une jaunisse aiguë et des symptômes associés.
Importance du groupe sanguin:
1. Transfusion sanguine.
2. Certaines maladies du sang.
3. Test de paternité.
4. En médecine légale.
5. Études ethnologiques.
6. Études anthropologiques.
7. Divers buts expérimentaux.
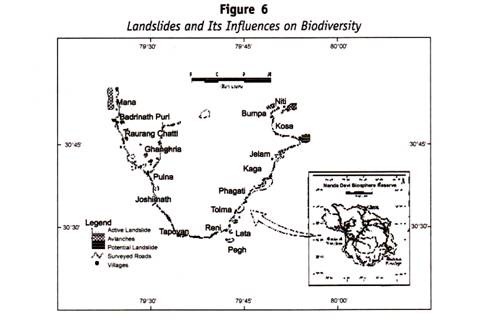
Une incompatibilité du sang ne peut survenir que dans les cas marqués d’un astérisque (*) — car dans ces deux groupes, la mère est capable de produire une agglutinine Anti-Rh pour détruire le Rh + R.B.C. présent chez le fœtus.
Contrôle génétique de la Structure antigénique:
Les antigènes Rh:
Les deux ensembles indépendants de gènes du groupe sanguin allélique discutés jusqu’à présent sont des exemples relativement simples du contrôle génétique des substances du groupe sanguin. Un dernier cas sera présenté en détail afin d’illustrer la situation la plus complexe chez l’homme qui a été rendue intelligible grâce à une compréhension des relations entre gènes et antigènes.
Ce cas est celui des substances rhésus, qui représentent une série d’antigènes hérités indépendamment des antigènes MN et ABO et qui sont déterminés par des gènes présents sur une autre paire de chromosomes. La série d’antigènes tire son nom, Rh, du singe rhésus (Macaca mulatta), chez lequel le premier membre de la série a été découvert par Landsteiner et Winner en 1940.
Levine et Stetson (1939) avaient établi que la maladie hémolytique des nouveau-nés appelée érythroblastose foetale était due à l’isoimmunisation des mères en un antigène inconnu sur les globules rouges de leurs enfants. Peu de temps après la description des antigènes Rh, Levine, Katsin et Burnham (1941) ont découvert qu’il s’agissait de l’antigène responsable de la maladie qu’ils étudiaient.
Ces découvertes initient une étude intensive des antigènes Rh qui se poursuit depuis. Cette enquête a non seulement apporté une solution à de nombreux problèmes associés à la maladie, mais elle a considérablement avancé les concepts de la nature de l’hérédité des substances du groupe sanguin en général.
Deux hypothèses majeures ont été avancées pour expliquer le mécanisme génétique qui contrôle les antigènes Rh. L’un d’eux, proposé par Wiener, postule une série d’allèles à un seul locus m une paire de chromosomes différents de ceux porteurs de tout autre gène pour les antigènes de groupement sanguin.
L’autre, avancé par Fisher et Race, est d’accord avec ce qui précède en déclarant que les gènes impliqués se trouvent sur leur propre paire de chromosomes, mais n’est pas d’accord en ce sens qu’il postule trois paires d’allèles étroitement liés à trois loci distincts.
La liaison impliquée est considérée comme si étroite que des croisements se produisent avec des fréquences aussi basses que jamais observées. Malheureusement, les prédictions génétiques de ces deux hypothèses sont vivantes sous tant d’aspects qu’il n’a pas encore été possible d’établir avec finalité laquelle est correcte.
Une comparaison schématique des concepts de Wiener et de Fisher-Race:
L’un des points fondamentaux en question est de savoir s’il existe ou non une relation un à un entre le nombre de types d’anticorps Rh avec lesquels une cellule va se combiner et le nombre de types de gènes déterminant les spécificités antigéniques responsables de cette combinaison.
Ce point est illustré en considérant des cellules (d’un individu génétiquement homozygote) capables de se combiner avec trois types d’anticorps différents, anti-1, anti-2 et anti-3. L’hypothèse de Weiner permettrait le concept selon lequel les trois anticorps se combinaient avec différentes parties d’une seule molécule d’antiges, dont les spécificités complexes étaient déterminées par un seul type de gène.
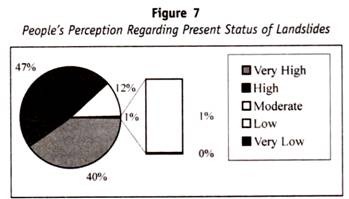
L’hypothèse de la race de Fisher ne permettrait pas ce concept, mais visualise chaque anticorps se combinant avec une molécule d’antigène avec une seule spécificité, déterminée par un seul gène. Le diagramme ci-joint décrit la nature du contraste entre ces deux concepts.

Une attention particulière doit être portée au point que le concept de Wiener n’entre pas en conflit avec la relation un gène-un antigène mentionnée au début de ce chapitre. Au contraire, il est facilement concevable que l’antigène déterminé par un seul gène puisse avoir une structure topographique complexe qui induira, et se combinera avec, plus d’un type d’anticorps d’une manière analogue à celle observée dans l’étude des antigènes “artificiels”; En d’autres termes, le concept de relation un à un entre un gène et la spécificité antigénique qui est son produit ne nécessite pas du tout une relation un à un entre cette spécificité antigénique et les anticorps qu’elle engendre.
Le concept de Weiner de Rh:
Le concept de Weiner postule une série de base de 8 gènes alléliques (des membres supplémentaires ont été ajoutés à cette série, mais ceux-ci n’ont pas besoin d’être considérés ici), dont deux peuvent se produire chez un seul individu hétérozygote. Chacun de ces gènes détermine un antigène capable d’induire et de se combiner avec un à trois types d’anticorps (et plus).
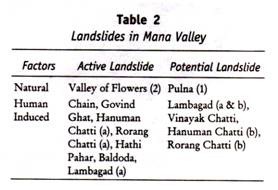
Les spécificités antigéniques impliquées se manifestent dans diverses combinaisons, déterminées par l’allèle particulier responsable d’un antigène donné. (Les anticorps utilisés dans cette recherche sont généralement obtenus à partir d’humains isoimmunisés, volontaires ou mères ayant un enfant souffrant d’une maladie hémolytique; Les symboles de Wiener pour les différents gènes, les antigènes qu’ils déterminent et les réactions de ces antigènes à des antisérums sélectionnés se trouvent dans le tableau 13.4. Un tel gène est écrit en une seule lettre, suivie d’un exposant, tandis que l’antigène que chacun détermine est écrit en deux lettres suivies d’un indice ou d’un exposant. Les différents antigènes vont maintenant être considérés.

Le symbole Rho est en majuscule car il représente le premier antigène Rh qui a été découvert et qui reste encore le plus significatif dans la maladie hémolytique. Les symboles rh’ et rh” représentent des antigènes supplémentaires trouvés par la suite. Les symboles Rh1 et Rh2 représentent des antigènes complexes constitués de deux spécificités. Rhj est composé des unités Rho et rh’; Rh2 est composé des unités Rho et rh”. Les symboles supplémentaires Rhz et rhy représentent des antigènes ayant de multiples spécificités comme indiqué. Le symbole rh nécessite un commentaire spécial.
À l’origine, ce symbole signifiait l’absence de spécificités antigéniques connues (c’est-à-dire Rh0, rh’ et rh”). Cependant, la découverte de deux nouveaux types d’antisérums a révélé l’existence de deux types supplémentaires de spécificités antigéniques. Ceux-ci se produisent dans diverses combinaisons avec les autres, spécificités qui viennent d’être décrites.

Le premier de ces antisérums, trouvé à l’origine par Levine et ses collaborateurs, identifie une spécificité maintenant appelée hr’ qui se produit sur toutes les cellules dépourvues de la spécificité rh’. La seconde identifie une spécificité appelée hr ” qui se produit sur toutes les cellules dépourvues de la spécificité rh”. (La contrepartie antigénique de l’antigène Rh0, Hr0, n’a pas encore été identifiée avec certitude.) Cette situation historiquement compliquée a conduit à la reconnaissance du symbole rh comme représentant un antigène complexe avec les spécificités hr ‘ et hr “.
De plus, les deux nouveaux antisérums ont étendu la description des autres symboles Rh. Ces relations sont présentées dans le tableau 13.5. Afin de comprendre ceux-ci (et ceux déjà présentés dans le tableau 13.4) l’étudiant doit préparer des diagrammes similaires à ceux montrés précédemment, en substituant les symboles Wiener aux nombres utilisés.
Pour étayer le schéma de Wiener, les cinq antisérums considérés ici permettent la détection d’amas variables d’une série de spécificités antigéniques (appelées individuellement facteurs sanguins) qui, ensemble, proviennent du groupe sanguin Rh d’une personne donnée. Ces grappes passent de génération en génération, leur continuité spécifique et structurelle étant déterminée par l’allèle particulier dont elles sont le produit. Un examen plus approfondi de l’héritage de ces facteurs est donné dans une section ultérieure.
Le concept de Race Fischer de Rh:
Le concept de Race Fischer trouve son origine dans la vision analytique du généticien et mathématicien britannique R. A. Fischer. Il a proposé, dans une suggestion présentée par Race en 1944, que les antigènes Rh alors connus puissent être considérés comme les produits de l’action d’une série de trois paires d’allèles très étroitement liés, chaque gène de chaque paire produisant un seul antigène ayant la capacité d’induire et de réagir avec un seul type d’anticorps.
Les paires alléliques de gènes proposées étaient symbolisées par C, c; D, d; et E, e. Chacun était considéré comme produisant un antigène distinct désigné par la même lettre. Aucune dominance n’est impliquée par l’utilisation de majuscules et de minuscules, sélectionnées simplement pour montrer leur allélisme.
Les relations formalisées de ces plusieurs gènes sur les chromosomes d’un individu hétérozygote pour chacun d’eux sont:
CDE / cde
D’autres combinaisons de trois allèles sur des chromosomes particuliers se produisent bien sûr, par exemple, C D e, c D E, C d e, etc. (certaines autorités écrivent la séquence de lettres en cause comme D. C. E en reconnaissance de considérations génétiques de liaison et de délétion possible; cependant, ce ne sont pas des considérations pertinentes ici.)
Au moment où le concept de race de pêcheur a été établi, les antisérums étaient connus pour les antigènes C, c; D; et E. Les antisérums supplémentaires, pour les antigènes d et e, ont été prédits, dont l’anti-e a maintenant été établi avec certitude.
De plus, l’existence du chromosome c(d)E alors inconnu a été prédite et trouvée par la suite. Le succès de ces prédictions, ainsi que la relative simplicité de la terminologie et des concepts impliqués, ont conduit à une large acceptation du schéma de la race de Pêcheur, en particulier parmi les cliniciens et les chercheurs européens.
En résumé, le concept britannique reconnaît une série de chromosomes portant différentes combinaisons des allelles C, D, E très étroitement liées. Ces combinaisons sont considérées comme le résultat d’un croisement, si peu fréquent qu’elles n’ont pas été détectées.
Le symbole D correspond à celui de Rho, et d’autres parallèles dans les deux terminologies sont présentés dans le tableau 13.6. De même, les deux ensembles de symboles pour les cinq types d’anticorps Rh peuvent être liés comme suit:

Héritage des facteurs sanguins Rh:
Il est évident qu’en l’absence de dominance, de croisement de mutations et d’épistose (dont aucune n’a encore été trouvée au cours des études génétiques sur les antigènes Rh), les facteurs sanguins Rh réapparaîtront de génération en génération sous forme d’amas caractéristiques.
Par exemple, un croisement entre un père de génotype R2r (CDE/cde) et une mère de génotype ϒR” (Cde/cdE) peut potentiellement produire quatre types d’enfants, comme le montre facilement l’utilisation du carré de Punnett:

Deux, parmi les enfants montrés, posséderaient l’antigène RhofD) dont leur mère manque. Dans l’usage classique des termes Rh, leur mère serait “Rh négative” alors qu’ils seraient “Rh positifs”. Cet exemple montre également que la définition de la positivité et de la négativité Rh est une définition relative qui doit être faite en termes d’antigènes impliqués.
En théorie, tout enfant possédant des antigènes Rh qui manquent à sa mère est positif par rapport à ces antigènes, tandis que sa mère est négative par rapport à eux. En pratique, cependant, l’antigène Rho(D) s’est avéré être le plus fréquemment impliqué dans la maladie hémolytique, rh’ (C) le suivant, les autres facteurs sanguins étant beaucoup moins fréquemment impliqués.
Importance de développer le Concept Correct des Relations génétiques des antigènes Rh:
Les sections précédentes ont montré que les systèmes de nomenclature Weiner ou Fisher-Race peuvent être utilisés pour décrire les antigènes et les anticorps Rh. Ce point est reconnu par l’Institut national de la Santé qui exige que les deux systèmes soient appliqués à l’étiquetage des antisérums produits commercialement.
Cependant, cela ne devrait pas détourner l’attention de la nécessité de déterminer la validité de l’un ou l’autre concept sous-jacent à cette nomenclature, même si cela peut sembler “académique” et non directement préoccupant dans le travail clinique.
Une seule raison de la nécessité d’efforts continus pour résoudre ce problème est que, comme souvent déjà noté, les antigènes semblent être les produits directs des gènes qui les produisent. Les anticorps qu’ils induisent deviennent donc, du fait de leurs spécificités fines, les indicateurs les plus sensibles des variations d’action génique connues.
Cela rend indispensable l’obtention d’un schéma conceptuel précis qui reliera la production d’antigènes aux schémas en cours d’évolution concernant la relation des gènes aux enzymes et de la structure de l’acide nucléique au “code génétique ” utilisé dans la transmission héréditaire des messages “.
L’examen détaillé de ces relations dépasse largement le cadre de ce texte, le lecteur intéressé étant renvoyé aux “récits populaires de Crick, Gamow et Beadle pour une introduction aux histoires impliquées.
Stomont a résumé les raisons d’une tendance croissante de la part de plusieurs généticiens de premier plan à privilégier le concept de Wiener, malgré sa terminologie plus difficile. Son résumé, trop avancé pour être présenté ici, est basé sur des parallèles entre le comportement des antigènes Rh chez l’homme et les séries d’allèles B et C qui déterminent les groupes sanguins chez les bovins.
Ces séries d’allèles contrôlent de loin l’ensemble le plus complexe de facteurs sanguins connus, un ensemble dont les relations ne peuvent raisonnablement être expliquées qu’en termes d’allèles multiples plutôt qu’en séries de gènes liés. Des détails supplémentaires concernant les groupes sanguins de bovins sont donnés plus loin dans ce chapitre. Race et Sanger et Levine présentent des discussions et d’autres références du point de vue de Fisher.
L’étudiant doit se rendre compte que les principaux partisans de l’un ou l’autre schéma ont mené des recherches qui ont rarement été excellées dans les annales de la biologie et que les résolutions expérimentales de leurs différences ne seront ni faciles ni triviales.