サイトメガロウイルス(CMV)HIV/AIDS患者における感染とCMVの診断値-異なるサンプルタイプ間のDNA検出
はじめに
サイトメガロウイルス(CMV)は、ヒト集団に広く普及している一般的なヘルペスウイルスである。 CMV感染は、通常、症状を引き起こさず、主に唾液腺、腎臓、および他の器官に影響を及ぼす。 しかし、ウイルス複製は免疫不全患者で起こり、臓器およびその機能の損傷に寄与する可能性がある。 日和見感染は、HIV/AIDS患者においてより頻繁かつ重症である。 CMVウイルス感染は、これらの患者で一般的であり、目、肺、神経系、および消化器系を含む複数の器官/システムに影響を与える可能性があります。 多くの研究は、単純なCMV感染(1)のウイルス学的および免疫学的特徴、特に女性および子供に見られるものを探求してきた。 しかし,CMV感染の免疫学的特徴は,既に免疫不全のHIV/AIDS患者においては非常にユニークである。 CMV感染を有するHIV患者とCMV感染のみを有するHIV患者との間には、臨床的特徴、治療手段、予後因子に違いがある(2)。 中国のガイドラインは、合併症(網膜炎、肺炎、CMV脳炎、腸炎など)を有するHIV/AIDS患者には、直ちにCMVおよびARTの抗ウイルス療法が必要であることを推奨した。)CMV感染が確認された場合。 CMV感染によって引き起こされる臨床症状の非特異性のために、実験室検査はCMV感染の診断のための主な基礎である。 最も広く使用されている臨床方法は、CMVウイルス複製およびcmv IgG、CMV IgMおよびCMV抗原PP65の検出を含む血清免疫学的方法である(2)免疫機能障害を有する患者では、CMV抗体の産生が弱化または遅延し、偽陰性につながり、診断を逃した率を増加させる可能性があるため、CMV-DNAのPCR検出は、CMV感染の診断および治療のモニタリングのための標準的な方法となっている(3)。 水島大介他 進行したHIV−1感染患者において、血漿CMV−DNA PCRは、CMV網膜炎および全てのCMV−EODの両方の診断において重要な値を有することを報告した(4)。 CMV-DNA PCRは、血漿、尿、脳脊髄液、房水、糞便などの様々なサンプルタイプで検出することができます。 (5). しかし、血漿以外の試料におけるCMV−DNA PCR検出の意義および値を分析し、議論した論文はほとんどない。 本研究では、臨床検査(CMV-DNA、CMV抗体、CD4+Tリンパ球数、HIVウイルス量などを含む)を遡及的に分析した。 2017年から2019年まで当センターで治療を受けた808人のHIV/AIDS患者において、CMV共感染およびいくつかの検出方法の長所と短所を理解する。 MDAR報告チェックリスト(http://dx.doi.org/10.21037/apm-20-1352で入手可能)に従って、以下の記事/ケースを提示します。
メソッド
被験者
2017年1月から2019年10月の間に当センターに入院した合計808人のHIV/AIDS入院患者が登録されました。 各患者において、HIV−RNA、CD4+tリンパ球数、CMV−DNA、および関連抗体を測定した。 HIV感染の診断は、HIV/AIDS診断と治療ガイドライン(第三版)(6)に基づいており、すべての患者は、患者を治療した福州市疾病管理センター(CDC)または地元のCDCに CMV感染の診断は、以下の基準に基づいた:(i)血漿、肺胞洗浄液、尿、脳脊髄液(CSF)、および/または他の体液中のCMV−DNA陽性;(I I)血清CMV−免疫グロブリンM(Igm)陽性;(III)cmv網膜炎; 性の診断的抗CMV治療として発現するCMV腸炎または食道炎;(VI)神経系症状として発現するCMV脳炎およびCSFまたは脳組織においてCMV-DNA陽性;(VII)発熱、異常な肝肝生検。 項目(II)を除く上記の基準のいずれかが満たされた場合、または項目(II)に加えて他の基準が満たされた場合(7)、CMV感染の診断が行われた。
人間の参加者を含む本研究で実施されたすべての手順は、ヘルシンキ宣言(2013年に改訂)に従ったものであった。 この研究は、当センターの医療倫理委員会によって承認されました(承認番号。 KS2019-070-01)。 データは匿名であり、インフォームドコンセントの要件は放棄されました。
包含および除外
包含基準: 最初に福建医科大学のMengchaoのHepatobiliary病院を訪問し、14日以内のHIV-RNA、CMV-DNA、CMV-IgGの抗体、CMV-IgMの抗体およびCD4+tのリンパ球の検出を完了したHIV/AIDSの患者。 サンプルサイズが不足しているため、上記の検査項目を完了できないHIV/AIDS症例を除外します。<6 9 1 1><1 9 7 4>試薬および装置<4 2 1 6><1 5 3 3>HIV−RNA定量<5 4 6 6><3 4 2 2>蛍光定量リアルタイムポリメラーゼ連鎖反応(PCR)(FQ−PCR)は、Qiagen(深セン、中国)製のHIV−RNA定量キッ<6 9 1 1><1 5 3 3>CD4+tリンパ球計数<5 4 6 6><3 4 2 2>使用した器具はFacscalibur flow cytometer(B D Biosciences,USA)であり、使用した試薬キットはB D Multitest CD3/CD4/CD8/CD4 5(B D Biosciences,USA)であった。<6 9 1 1><1 5 3 3>CMV−DNA定量<5 4 6 6><3 4 2 2>fq−PCRをM X3 0 0 0P QPCRシステム(Agilent、USA)で行い、血漿、尿およびCSF中のCMV−DNAレベルを検出した。 使用されたキットは、Sansure Biotech(Hunan,中国)によって製造された。<6 9 1 1><1 5 3 3>CMV抗体試験<5 4 6 6><3 4 2 2>化学発光イムノアッセイを、支持キット(Roche Diagnostics、Germany)を用いて、Cobas e6 0 1アナライザ(Roche Diagnostics、Germany)上で抗CMV−IggおよびIgm抗体を検出す
研究方法
核酸検出
HIV/AIDS患者を当院に入院させた後、3mLの絶食エチレンジアミンテトラ酢酸(EDTA)-抗凝固全血標本を採取し、3,000r/分で5分間遠心分離し、HIV-RNAおよびCMV-DNA検出のための血漿200μ lを採取した。 すべての患者において、午前中に5mLの尿検体を採取し、十分に混合し、次いで、CMV−DNA検出のために2 0 0μ Lを採取した。 神経学的症状を有する患者のために、CMV−DNA検出のために1mlのCSFを得た。 CMV-DNAのキットおよびHIV-RNAのキットの検出の限界そして肯定的な判断の標準に従って。 CMV-DNA値が400コピー/mLを超えていた場合、またはHIV-RNAレベルが500コピー/mLを超えていた場合、標本は陽性であると考えられた。
Tリンパ球サブセットの検出
HIV/AIDS患者では、3mLのEDTA抗凝固絶食全血標本を入院時に収集し、補助試薬を使用してBD FACSCaliburフローサイトメーター上でtリンパ球サブセットの検出のために十分に混合した。
免疫抗体の検出
HIV/AIDS患者では、空腹時血液検体3mLを入院時に採取し、ゲルセパレータ付き血清チューブ中で3,000r/minで5分間遠心分離し、機械で試験した。
上記の試験はすべて、製造元のマニュアルに記載されている試薬の説明書および機器の標準的な操作手順に従って厳密に実施されました。
統計解析
統計解析は、SPSS21.0ソフトウェアを使用して実行しました。 正規分布の測定データは、平均±標準偏差(x±SD)を使用して提示され、非正規分布データは中央値(25-75百分位)として表されます。 カウントデータは、パーセンテージとレートで表されます。 二つのグループ間の非正規分布測定データの比較はノンパラメトリックランクサム検定を用いて行ったが,カウントデータはカイ二乗検定を用いて比較した。 P値<0.05は統計的に有意であると考えられた。
結果
一般データ
808人のHIV/AIDS患者の一般データを表1にまとめた。 性別および年齢はCMV群と非CMV群との間に有意差を示さなかった。 CMV感染群の絶対CD4カウントは、CMV非感染群(Z=-8.87、P<0.001)よりも有意に低く、HIV-RNAレベルは、非CMV感染群(Z=-3.207、P<0.05)よりもCMV感染群で有意に高かった(表1)。
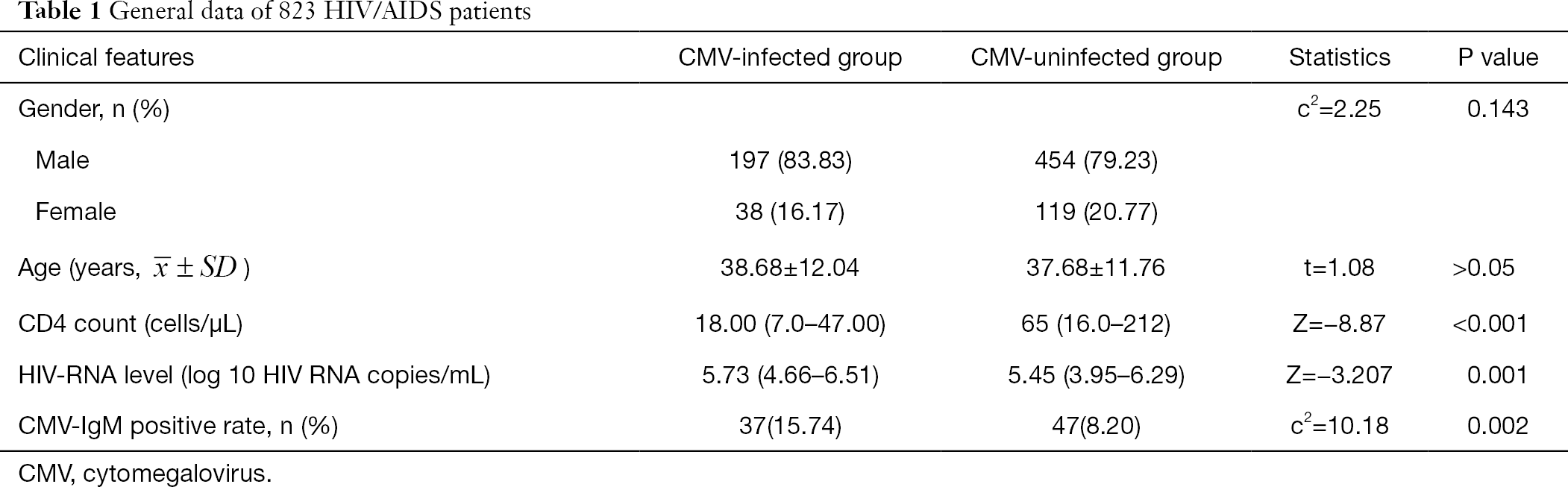
全表
CMV-DNA、CMV-IgG、およびCMV-IgMの陽性率は全体で29.08%であった(235/808)。
CMV-DNAの全体的な陽性率は29.08%であった(235/808)。具体的には、Csfでは5.70%(13/228)、血漿では26.01%(77/296)、尿では25.75%(180/699)であった。 CMV-IgGの陽性率は99.8%(806/808)であり、CMV-IgMの陽性率は10.40%(84/808)であった。
CMV感染とcd4+Tリンパ球数との相関
CD4+Tリンパ球数をグループ化した後、CD4+Tリンパ球の低頻度でサイトメガロウイルスに感染した患者の割合 CMV感染の発生率は、CD4カウントの減少とともに増加した(表2)。
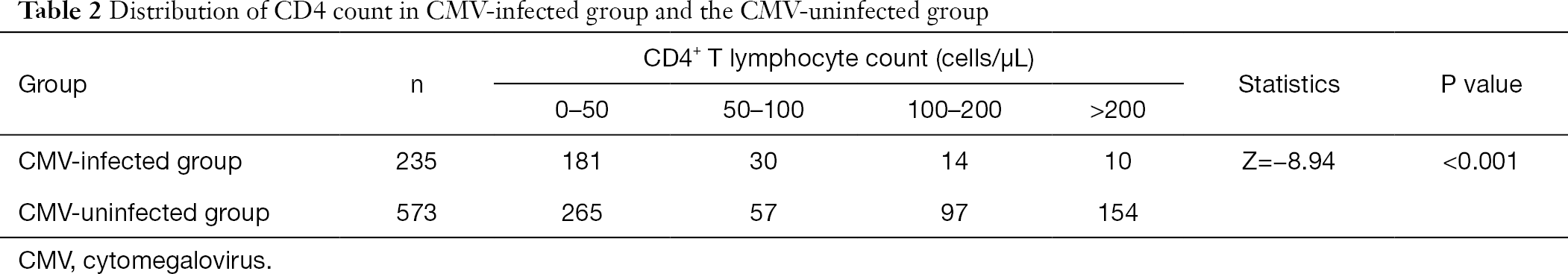
フルテーブル
異なるサンプルにおけるCMV-DNAの検出
これら808人の患者のうち、198人の患者は血漿および尿CMV-DNAおよび血漿抗−CMV−IgGおよびCMV−IgM抗体。 対データのカイ二乗解析を用いて,尿CMV-DNAおよび血漿CMV-DNAの血漿Cmv-Igm抗体とのペアワイズ比較を行った。 尿および血漿CMV-DNA検出の結果は、血漿CMV-IgG抗体アッセイ(P<0.001)の結果と有意に異なっていたが、血漿CMV-DNA検出の結果は、尿CMV-DNA検出(P>0.05)の結果と有意に異ならなかった(表3,4)。

全表
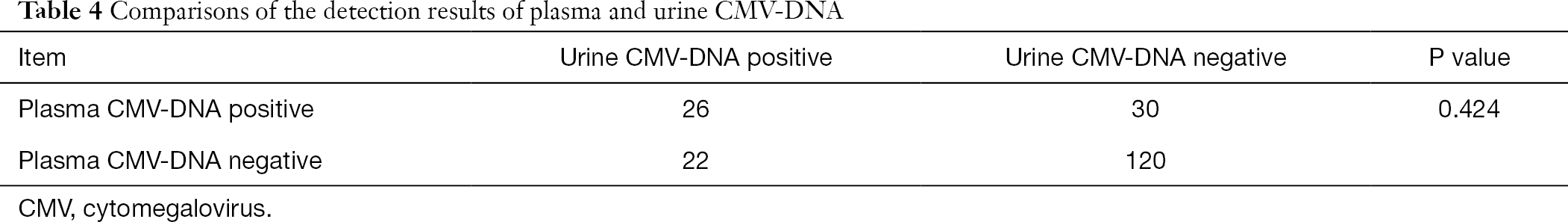
完全な表
議論
CMVはβ-ヘルペスウイルス群のメンバーであり、その厳密な種特異性およびヒト集団における広範な発生率によって特徴付けられる。 CMV血清価は、小児では約85%、成人では最大95%である。 我々の現在の研究では、CMV-IgGの陽性率は99.8%に達した。 CMVはほとんどの場合潜伏していますが、免疫不全の個体では、ウイルスは指数関数的に複製され、血液とともに体全体に広がり、CMVウイルス血症、さらには有機的なCMV病を引き起こします(8)。 CMV感染は、HIV/AIDS患者における一般的な日和見感染症の1つである。 CD4+Tリンパ球はHIVウイルスの標的細胞であり、その数はしばしばAIDSの経過を反映し、AIDS患者の免疫状態を評価するための指標としても使用され 本研究では、CMV感染、CD4カウント、およびHIV/AIDS患者808におけるHIV-RNAレベルを分析しました。 我々は、エイズ患者におけるCMVの陽性率は、CD4カウントの減少とHIVウイルス負荷の増加とともに増加したことがわかった。 また、我々の現在の研究では、CMV陽性患者の最大77.02%がCD4カウント<50細胞/μ lを有し、CD4<50細胞/μ lがHIV-CMV共感染の危険因子であることを示唆しており、Dengらの発見と一致している。 (9). CMV感染群のHIV-RNAの定量レベルはcmv非感染群のそれよりも高く,hiv-RNAウイルス量の高レベルがHIV/AIDS患者におけるCMV感染の別の危険因子であることを間接的に示唆した。したがって、HIV/AIDS患者は、日和見感染を予防するために免疫再構成を促進するために、できるだけ早くART治療を開始すべきであり、HCMVのスクリーニングは、<50細胞/μ lのCD4カウントを持つHIV/AIDS患者のために不可欠であることが推奨されている(2)。
また、CMV感染の臨床検出におけるウイルス核酸アッセイおよび免疫学的方法の値を評価しました。 中国および国際的な研究では、CMV-DNAはCMV感染の臨床症状および血清学的反応よりも早く現れることが示されている。 FQ-PCRは、現在、最も正確かつ迅速な微生物定量法であり、従来のPCRのいくつかの問題(例えば、増幅産物汚染および非定量化)を克服することができる(10)。 我々の現在の研究では、CMV-DNAの陽性率は5であった。70%(13/228)神経学的症状を有する228人の患者のCSFサンプルでは、血液脳関門および臓器感受性によって説明されるかもしれない血漿および尿サンプル 抗CMV-IgM抗体は、多くの場合、アクティブなウイルス感染のマーカーとして使用されます;しかし、抗CMV-IgM抗体の陽性率は、非HIV/AIDS集団で報告されたCMV感染の陽性率よりも低かった私たちのHIV/AIDS患者でのみ10.40%(84/808)であった(11)。 さらに,その陽性率は,免疫系の弱化またはHIV/AIDS患者におけるIgm抗体の生成の遅延によるものであると考えられる核酸検出の結果と一致しなかった。 従って、CMV−Igm抗体の検出は、HIV/AIDS患者におけるHCMVスクリーニングにおいて限られた役割を有する。 さらに、808人の患者におけるCMV感染の陽性率は、我々の現在の研究では29.05%(235/808)であり、これはLiらによって報告された21.85%よりわずかに高い。 この研究で収集されたサンプル(血漿、尿、およびCSFを含む)のより多様性に起因する可能性があります(12)。 CMV-DNAの陽性率は、尿中で25.57%、血漿中で26.01%であり、その差は統計的に有意ではなかった。 したがって、CD4+tリンパ球数が200細胞/μ l未満の場合、特に<50細胞/μ lの場合、血漿および尿中のCMV-DNAスクリーニングを行うことを推奨し、明らかな神経学的症状が存在する場合は、CSF中のCMV-DNAの検出が必要である。
結論
結論として、低CD4+tリンパ球数と高いHIV-1ウイルス量は、HIV/AIDS患者におけるCMV感染の危険因子である。 Fq−PCRによる尿または血漿CMV−DNAの検出は、HIV/AIDS患者におけるCMV感染のスクリーニングにおいて非常に有用であるが、血中CMV IggおよびCMV Igmレベルの検出は、 血液または尿CMV-DNAスクリーニングは、CMV感染を早期に予防および診断し、生活の質を向上させるために、AIDS患者に推奨されます。
謝辞
資金調達:福建省の主要臨床専門分野構築プログラムが後援
脚注
報告チェックリスト:著者はMDAR報告チェックリストを完了しました。 http://dx.doi.org/10.21037/apm-20-1352
データ共有声明:http://dx.doi.org/10.21037/apm-20-1352
利益相反:すべての著者はICMJE uniform disclosure form(http://dx.doi.org/10.21037/apm-20-1352で入手可能)に記入しています。 著者には、宣言する利益相反はありません。
倫理的声明:著者は、作業のあらゆる部分の正確性または完全性に関連する質問が適切に調査され、解決されることを保証する上で、作業のすべての面 人間の参加者を含むこの研究で行われたすべての手順は、ヘルシンキ宣言(2013年に改訂された)に従っていました。 この研究は、当センターの医療倫理委員会によって承認されました(承認番号。 KS2019-070-01)。 データは匿名であり、インフォームドコンセントの要件は放棄されました。
オープンアクセス声明:これは、クリエイティブ-コモンズ表示-非営利-NoDerivs4.0国際ライセンス(CC BY-NC-ND4.これは、変更や編集が行われず、元の作品が適切に引用されていることを厳密に条件とした記事の非商業的複製および配布を許可する(関連するDOIおよ 参照:https://creativecommons.org/licenses/by-nc-nd/4.0/。
- Yu X,Tong M,He G.妊娠中の女性の調節免疫細胞に対するサイトメガロウイルス感染の影響中国人。 専門は病理学、病理学。 2017;27:2103-6.
- 国立科学技術大プロジェクトは、第13次五カ年計画において日和見感染研究グループを支援している。 サイトメガロウイルス病に合併したエイズの臨床診断と治療に関する専門家のコンセンサス。 南西大学のジャーナル(自然科学版):1-17。
- Hodowanec AC,Pikis A,Komatsu TE,et al. 移植レシピエントにおけるCMV疾患の治療と予防:現在の知識と将来の視点。 J Clin Pharmacol2 0 1 9;5 9:7 8 4−9 8.
- 水島D,西島T,八代S,et al. HIV-1感染患者におけるサイトメガロウイルス終末臓器疾患に対する定量的血漿サイトメガロウイルスDNA PCRの診断有用性。 2015年(平成28年)6月8日現在の世帯数と人口は以下の通りである。:140-6.
- Michaelides A,Liolios L,Glare EM,et al. 肺移植後の末梢血白血球におけるヒトサイトメガロウイルス(HCMV)DNA負荷の増加はHCMV肺炎と相関する。 移植2001;72:141-7.
- 中国医師会のエイズグループ、神経科の感染。 HIV/AIDS診断と治療ガイドライン(第三版)。 感染症の中国ジャーナル2015;(10):577-93.
- Corrales I,Giménez E,Solano C,et al. 発生率とドナーとレシピエントCCR5、MCP-1、IL-10、およびTLR9遺伝子の一塩基多型による同種幹細胞移植患者におけるアクティブなサイトメガロウイルス感染 J Med Virol2015;87:248-55.
- Tagarro A,Del Valle R,Dominguez-Rodríguez S,et al. 先天性サイトメガロウイルス感染症の小児における成長パターン。 2019年(平成38年)12月30日から5月5日まで放送された。
- Deng X,Liu J,Zhang M,et al. サイトメガロウイルス感染と組み合わせたHIV/AIDSのウイルス学的および免疫学的特徴の分析。 病院感染の中国ジャーナル2019;29:2241-6。
- Kawano Y,Kawada J,Kamya Y,et al. 先天性サイトメガロウイルス感染症を有する循環ヒトおよびウイルス性マイクロrna sin患者の分析。 J Perinatol2016;36:1101-5.
- Li L,Gao S,Zhang T,et al. ヒトサイトメガロウイルス感染症のDNA検出とIgM検出の比較とそれらの組み合わせの適用値の議論。 実験診断の中国ジャーナル2015;(1):78-80。
- Li X,Cao L,Yu C,et al. エイズ患者におけるサイトメガロウイルスの感染に関する研究。 現代予防医学2012;39:2278-9.
(英語編集者:J.Gray)