酸、塩基、およびpH
|
|||||||||
酸とその共役塩基
酸のBronsted–Lowryの定義を覚えておいてください。 明らかに、私たちの前の例では、酢酸は、酢酸イオンの形成をもたらし、前方反応でH2Oにそのプロトンを寄付します。 しかし、逆反応では、酢酸イオンはh3O+からプロトンを受けてCH3COOHに戻る。 ブロンステッド・ローリーの定義から、塩基はプロトン受容体である。
|
従って、アセテートイオンは逆の反作用の基盤として機能し、あります 酢酸の共役塩基と呼ばれる。 酢酸と酢酸イオンは酸–塩基共役対として知られている。 興味深いことに、上記の反応には第二の酸–塩基共役対が存在する。 逆反応では、h3O+がプロトンを供与する(それを酸にする)一方、順反応では、H2Oがプロトンを受け入れる(それを塩基にする)ことに注意してくださ H2OとH3O+は共役酸–塩基対であり、H3O+は共役酸であり、H2Oは共役塩基である。
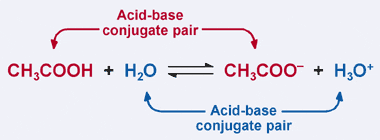
共役酸-塩基対では、共役酸は、対応する共役塩基よりも1つ以上のプロトンを有する。