산,염기 및 산도
|
|||||||||
산과 그 공액 염기
산의 브론스테드–로우 리 정의를 기억하십시오:산은 양성자 기증자입니다. 명확 하 게,우리의 이전 예에서 초 산 아세테이트 이온의 형성의 결과로 앞으로 반응에 물에 양성자를 기증 한다. 그러나,역 반응에서,아세테이트 이온은 물+에서 양성자를 받아 들여서 3 코로 되돌아 간다. 에서 브론스테드-로리 정의,베이스 이다 양성자 수용체.
|
따라서,아세테이트 이온은 역반응에 있는 기초로 행동하고,입니다 아세트산의 공액 염기라고. 아세트산과 아세테이트 이온은 산-염기 공액 쌍으로 알려져 있습니다. 흥미롭게도 위의 반응에는 두 번째 산–염기 공액 쌍이 있습니다. 역 반응에서 물+는 양성자(산으로 만들기)를 기부하는 반면,전진 반응에서는 물이 양성자(염기로 만들기)를 받아들이는 방법에 주목하십시오. 물 및 물+는 공액 산-염기 쌍이며,물+는 공액 산이고 물은 공액 염기이다.
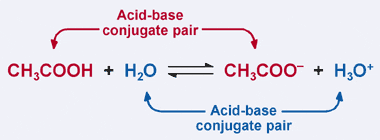
에 공액 산-염기 쌍,공액 산은 해당 공액 염기보다 하나 이상의 양성자를 가지고 있습니다.