12.4: Fordampning Og Kondensering
Fordampning
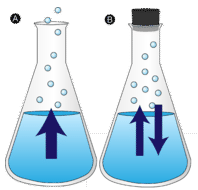
en dam med vann igjen uforstyrret til slutt forsvinner. De flytende molekylene rømmer inn i gassfasen, blir vanndamp. Fordampning er prosessen der en væske omdannes til en gass. Fordampning er omdannelsen av en væske til dens damp under væskens koketemperatur. Hvis vannet i stedet holdes i en lukket beholder, har vanndampmolekylene ikke mulighet til å flykte inn i omgivelsene, og vannstanden endres ikke. Som noen vannmolekyler blir damp, kondenserer et like antall vanndampmolekyler tilbake til flytende tilstand. Kondensering er tilstandsendringen fra en gass til en væske.
for at et flytende molekyl skal slippe ut i gasstilstanden, må molekylet ha nok kinetisk energi til å overvinne de intermolekylære tiltrekningskreftene i væsken. Husk at en gitt væskeprøve vil ha molekyler med et bredt spekter av kinetiske energier. Flytende molekyler som har denne bestemte terskel kinetisk energi unnslippe overflaten og bli damp. Som et resultat har de flytende molekylene som forblir nå lavere kinetisk energi. Når fordampning oppstår, reduseres temperaturen til gjenværende væske. Du har observert effekten av fordamping kjøling. På en varm dag absorberer vannmolekylene i svetten kroppsvarme og fordamper fra overflaten av huden din. Fordampningsprosessen etterlater den gjenværende svettekjøleren, som igjen absorberer mer varme fra kroppen din.
en gitt væske vil fordampe raskere når den blir oppvarmet. Dette skyldes at oppvarmingsprosessen resulterer i at en større brøkdel av væskens molekyler har den nødvendige kinetiske energien for å unnslippe væskens overflate. Figuren nedenfor viser den kinetiske energidistribusjonen av flytende molekyler ved to temperaturer. Antallet molekyler som har den nødvendige kinetiske energien til å fordampe, vises i det skyggefulle området under kurven til høyre. Den høyere temperaturvæsken \(\left (T_2 \ right)\) har flere molekyler som er i stand til å rømme inn i dampfasen enn den lavere temperaturvæsken \(\left (T_1 \ right)\).
på 29.029 fot \(\venstre( 8848 \: \tekst{m} \høyre)\) Er Mount Everest I Himalaya-området på grensen Mellom Kina og Nepal det høyeste punktet på jorden. Høyden gir mange praktiske problemer for klatrere. Oksygeninnholdet i luften er mye lavere enn på havnivå, noe som gjør det nødvendig å ta med oksygentanker sammen (selv om noen klatrere har nådd toppen uten oksygen). Et annet problem er at av kokende vann for matlaging mat. Selv om vann koker ved \(100^ \ text{o} \ text{C}\) på havnivå, er kokepunktet på Toppen Av Mount Everest bare rundt \(70^ \ text{o} \ text{C}\). Denne forskjellen gjør det svært vanskelig å få en anstendig kopp te (som definitivt frustrert Noen Av De Britiske klatrere).