Claisen Rearrangement
Claisen rearrangement (må ikke forveksles med Claisen kondens) er en kraftig karbon–karbonbindingsdannende kjemisk reaksjon oppdaget Av Rainer Ludwig Claisenin 1912. Oppvarming av en allylvinyleter vil initiere a-sigmatropisk omlegging for å gi en γ,δ-umettet karbonyl.
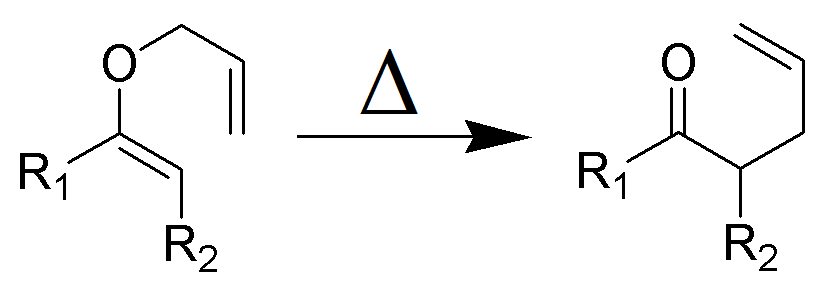
Figur 1: Wikimedia (Eget arbeid) – sigmatropisk omorganisering.
Claisen-omleggingen er en eksoterm, samordnet (bindingsspaltning og rekombinasjon) pericyklisk reaksjon. Woodward-Hoffmann-reglene viser en suprafacial, stereospesifikk reaksjonsvei. Kinetikken er av første orden, og hele transformasjonen går gjennom en svært ordnet syklisk overgangstilstand og er intramolekylær. Crossover eksperimenter eliminere muligheten for omorganisering skjer via en intermolekylær reaksjonsmekanisme og er i samsvar med en intramolekylær prosess.
det er betydelige løsningsmiddeleffekter observert i Claisen-omleggingen, hvor polare løsningsmidler har en tendens til å akselerere reaksjonen i større grad. Hydrogenbindende løsningsmidler ga de høyeste hastighetskonstanter. For eksempel gir etanol/vann løsningsmiddelblandinger hastighetskonstanter 10 ganger høyere enn sulfolan. Trivalente organoaluminiumreagenser, som trimetylaluminium, har vist seg å akselerere denne reaksjonen.
den første rapporterte Claisen omorganisering er-sigmatropic omorganisering av en allylfenyl eter til intermediate 1, som raskt tautomerizes til en orto-substituert fenol.
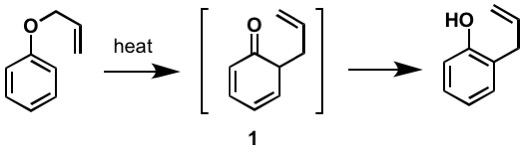
Figur 2: Av Kchemyoung (Eget arbeid) , Via Wikimedia Commons
Irland-Claisen rearrangement
Irland-Claisen rearrangement er reaksjonen av et allylisk karboksylat med en sterk base (som litiumdiisopropylamid) for å gi en γ,δ-umettet karboksylsyre. Omleggingen fortsetter via silylketen acetal, som dannes ved å fange litiumenolatet med klorotrimetylsilan. Som Bellus-Claisen (over), Irland-Claisen omorganisering kan skje ved romtemperatur og over. De e-og Z-konfigurerte silylketene-acetalene fører til henholdsvis anti-og syn-omorganiserte produkter. Det er mange eksempler På Enantioselective Irland-Claisen omarrangementer funnet i litteraturen for å inkludere kirale borreagenser og bruk av kirale hjelpestoffer.
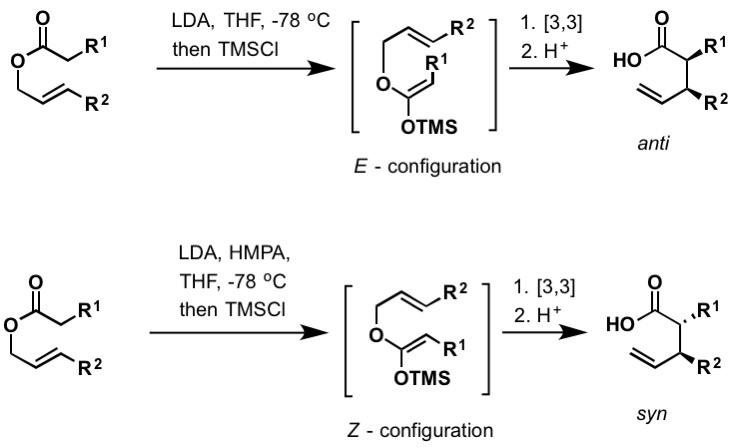
Figur 5: Bilde brukt med tillatelse (CC BY-SA 4.0; Kchemyoung)
Johnson-Claisen rearrangement
Johnson-Claisen rearrangement er reaksjonen av en allylisk alkohol med en ortoester til å gi en γ,δ-umettet ester. Svake syrer, som propionsyre, har blitt brukt til å katalysere denne reaksjonen. Denne omleggingen krever ofte høye temperaturer (100 til 200 °C) og kan ta alt fra 10 til 120 timer å fullføre. Imidlertid har mikrobølge assistert oppvarming i nærvær AV KSF-leire eller propionsyre vist dramatiske økninger i reaksjonshastighet og utbytter.
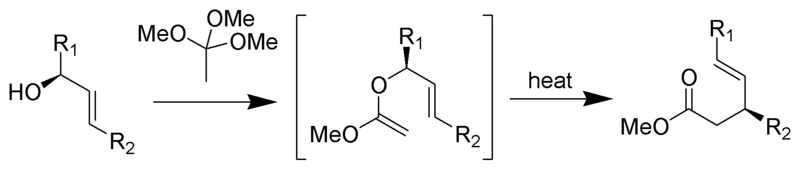
Mekanisme:
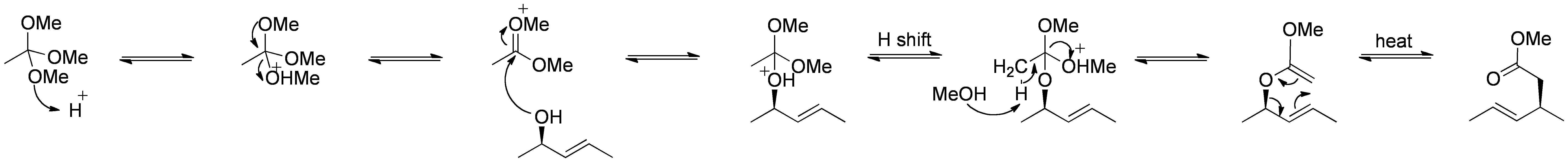
Av Selv Laget AV RAN 10 ( – ), via Wikimedia Commons
Foto-Claisen omorganisering
foto-Claisen omorganisering er nært knyttet til foto-Fries omorganisering, som går gjennom en lignende radikal mekanisme. Aryletere gjennomgå foto-Claisen omorganisering, mens foto-Fries omorganisering benytter arylestere.
Hetero-Claisens
Aza-Claisen
Et iminium kan tjene som en av de pi-bundne delene i omleggingen.
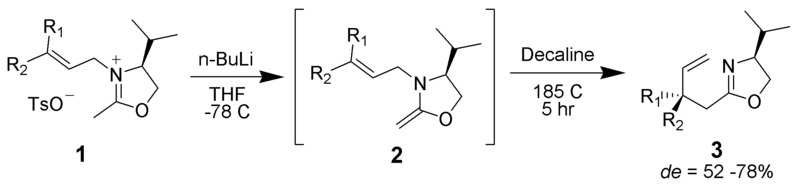
av ingen maskinlesbar forfatter gitt. ~ K antatt (basert på opphavsrettskrav). , Via Wikimedia Commons
Kromoksidasjon
Krom kan oksidere allylalkoholer til alfa-beta umettede ketoner på motsatt side av den umettede bindingen fra alkoholen. Dette er via en samordnet hetero-Claisen reaksjon, selv om det er mekanistiske forskjeller siden kromatomet har tilgang til d-shell orbitaler som tillater reaksjonen under et mindre begrenset sett av geometrier.
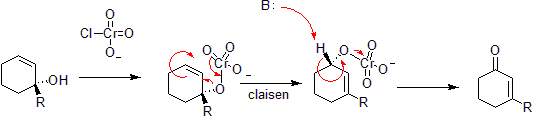
Ved den opprinnelige opplasteren Var Takometer på engelsk Wikipedia-Phosphorimidate Omorganisering Eller Staudinger-Claisen Reaksjon installerer en fosfitt i stedet for en alkohol og utnytter Staudinger reduksjon for å konvertere dette til en imine. Den etterfølgende Claisen drives av det faktum at En p = o dobbeltbinding er mer energisk gunstig enn En p = n dobbeltbinding.
.png?revision=1&size=bestfit&width=660&height=112)
Av Howcheng på en.wikipedia, Via Wikimedia Commons
Overman rearrangement
Overman rearrangement (oppkalt Etter Larry Overman) er En Claisen rearrangement av allylisk trikloracetimidater til allylisk trikloracetamider.
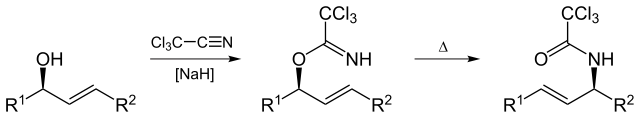
Ved Yikrazuul (Eget arbeid) , via Wikimedia Commons
Overman rearrangement gjelder for syntese av vicinol diamino comp fra 1,2 vicinal allylic diol.
Zwitterionic Claisen rearrangement
I Motsetning til typiske Claisen rearrangements som krever oppvarming, foregår zwitterionic Claisen rearrangements ved eller under romtemperatur. Acylammoniumioner er svært selektive For Z – enolater under milde forhold
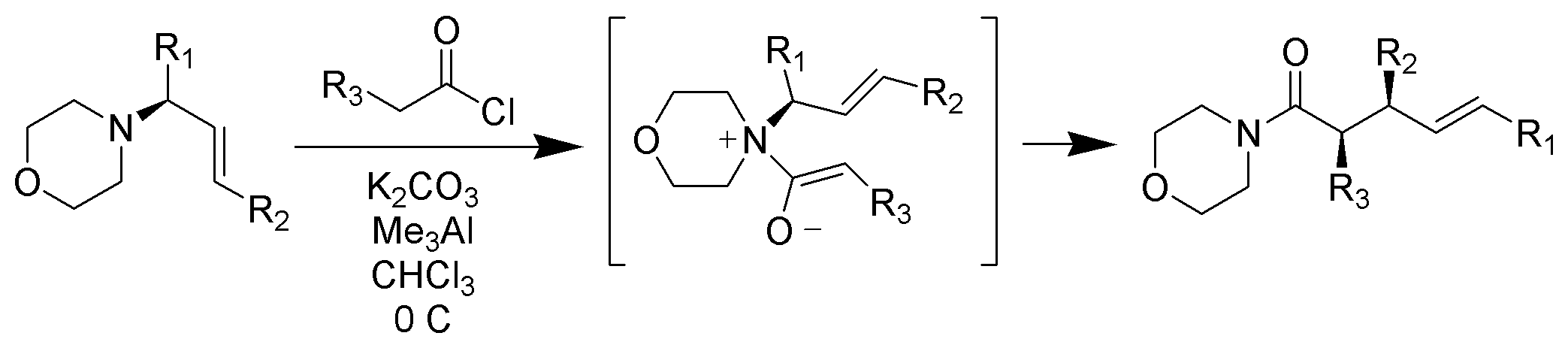
https://upload.wikimedia.org/wikiped…ent_Scheme.png
Claisen omorganisering i naturen
enzymet Chorismate mutase (EC 5.4.99.5) katalyserer Claisen omorganisering av chorismate ion til prefenat ion, et sentralt mellomprodukt i shikimic syre veien (biosyntetiske veien mot syntesen av fenylalanin og tyrosin).
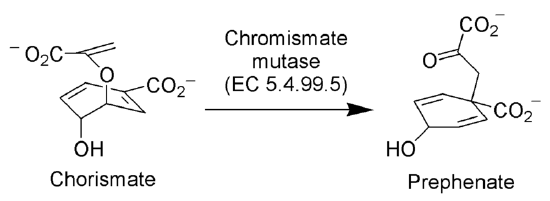
av ingen maskinlesbar forfatter gitt. ~ K antatt (basert på opphavsrettskrav). , Via Wikimedia Commons