7.5: Complex IV
Complex IV is de eindbestemming in de elektronentransportketen. Hier worden de elektronen die door de andere leden van het ademhalingssupercomplex zijn gereisd uiteindelijk aan O2 geleverd, waardoor het wordt gereduceerd tot water. Dat is een indrukwekkende prestatie, want tussen de eerste toevoeging van een elektron en de uiteindelijke afgifte van water moet een aantal reactieve zuurstofsoorten worden gevormd, maar de reactie wordt zo gecontroleerd dat de kans op celbeschadiging tot een minimum wordt beperkt. Tegelijkertijd worden meer protonen gepompt over het binnenste mitochondriale membraan.
- In Complex IV worden elektronen afgeleverd op hun eindbestemming, een molecuul van O2.
- de O2 wordt gereduceerd tot water.
oefening \(\Paginindex{1}\)
Schrijf een evenwichtige redox half-reactie om te laten zien hoeveel elektronen nodig zijn om een zuurstofmolecuul te reduceren tot water.
antwoord
O2 → H2O
O2 → 2 H2o (o gebalanceerd)
O2 + 4H+ → 2 H2o (h gebalanceerd)
O2 + 4e- + 4H+ → 2 H2o (gebalanceerd))
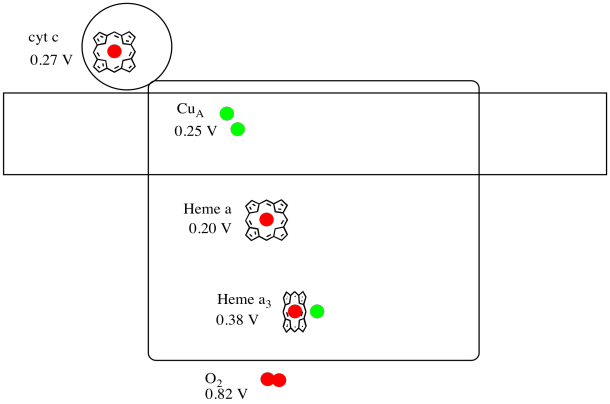
de Röntgenstructuur van Complex IV wordt hieronder getoond. Nogmaals, de matrix bevindt zich aan de onderkant van de afbeelding en de intermembrane ruimte is aan de bovenkant. Dat is waar de cytochroom c doceert, aan de top.
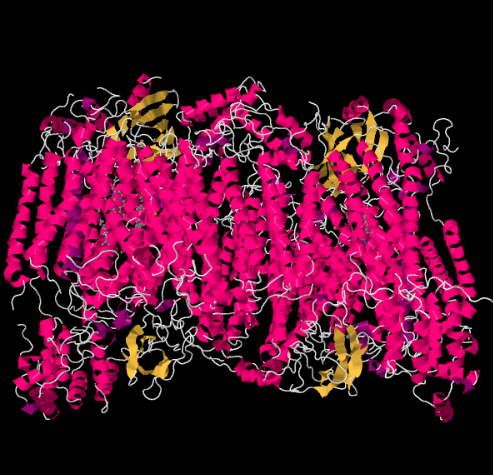
de mobiele elektronendrager cytochroom c bindt aan Complex IV en levert een elektron af aan een binucleaire koperplaats genaamd CuA. We kunnen die binucleaire koper site zien als we kijken in het eiwit, hieronder. Het is alleen gebonden aan het eiwit en niets anders, dus we zien alleen de twee koperionen bovenaan de foto. Dit paar koperatomen stuurt het elektron naar een heem, cytochroom a, die je hieronder en links kunt zien. Van daaruit gaat het elektron naar een andere binucleaire cluster, deze keer bestaande uit een heemgebonden ijzer (cytochroom a3) en een nabijgelegen koper (Welp). Deze binucleaire site zorgt voor de reductie van dioxygen tot water. In de structuur, is er een koolmonoxidemolecuul gebonden in de actieve plaats tussen cytochroom a3 en CuB. De koolstofatomen zijn aan het ijzer gehecht en de zuurstof aan het koper. Dat is waar het zuurstofmolecuul zich zou binden, wachtend om gereduceerd te worden tot water.
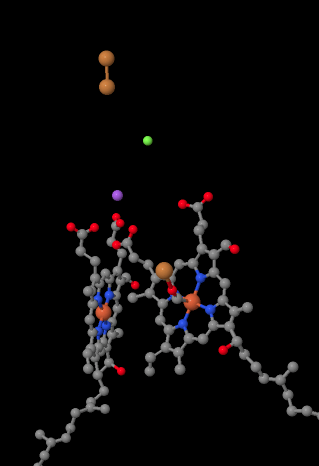
als je daarover nadenkt, betekent dit dat elektronen in de tegenovergestelde richting reizen van wat we zagen in de eerste drie complexen. In complexen I en II, werden elektronen geleverd uit de mitochondriale matrix en reisden omhoog naar de intermembrane ruimte, het stoppen bij een ubiquinon in het mitochondriale membraan. In Complex III, elektronen voortgezet in die “opwaartse” richting, van het mitochondriale membraan aan cytochroom c in de intermembrane ruimte. In Complex IV keren elektronen koers om en reizen terug naar de mitochondriale matrix. Vergeet niet, de mitochondriale matrix is n-gedoteerd door Proton pompen, dus deze elektronen reizen van de positieve kant van het membraan naar de negatieve kant. Dat moet moeilijk zijn.
- in Complex IV is het elektronentransport in de tegenovergestelde richting van de andere complexen.
- elektronen reizen van de intermembraanruimte naar de mitochondriale matrixzijde, tegen de ladingsgradiënt.
laten we nog eens kijken naar de belangrijke liganden voor het complex. Hieronder wordt een cartoon getoond. In de cartoon, wordt de O2 molecuul getoond bindend in die positie tussen heme a3 en de welp. Dat dinucleaire metaal is waar het zuurstofmolecuul wordt gereduceerd tot water.
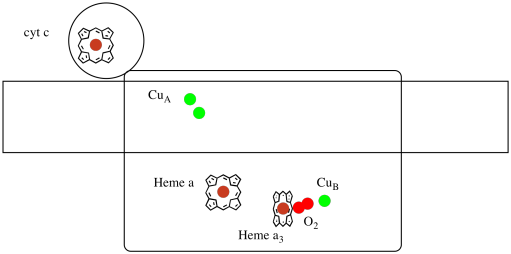
omdat vier elektronen nodig zijn om O2 tot H2O te reduceren, moeten vier cytochroom C-moleculen bij Complex IV binden voordat die reductie kan doorgaan. Het is waarschijnlijk dat de coördinatieomgeving van het zuurstofmolecuul — tussen twee metalen, in plaats van alleen gebonden aan één — het mogelijk maakt om sneller te worden gereduceerd tot water in plaats van reactieve zuurstofsoorten te vormen die in de cel blijven bestaan, zoals peroxiden.
oefening \(\Paginindex{2}\)
stel dat het ijzer in heme a3 begint in een gereduceerde Fe (II) toestand en het Welp begint in een gereduceerde Cu(I) toestand. Zorg voor een mechanisme voor de reductie van zuurstof naar water, met de toevoeging van vier elektronen en vier protonen. Gebruik Fe(II) als elektronendonor en lysine als protonendonor.
antwoord
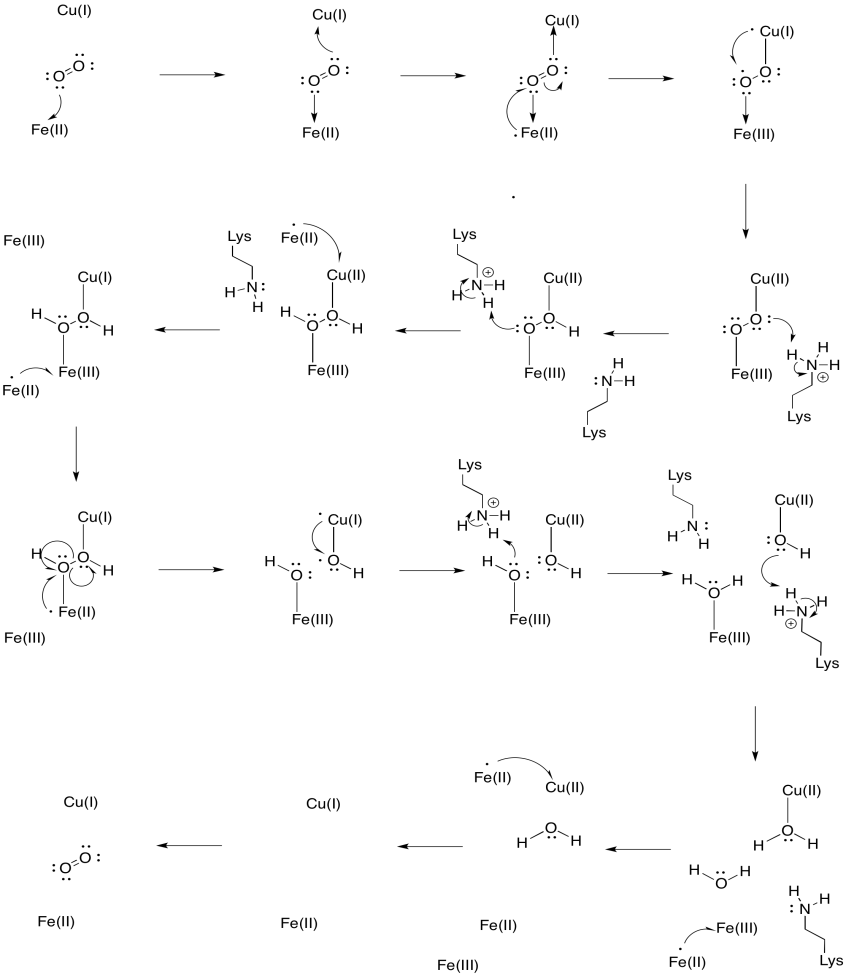
naast deze twee metalen, is er ook een gemodificeerd histidine-tyrosine conjugaat gebonden aan Welp. Men heeft voorgesteld dat deze tyrosine een andere bron van directe elektronen verstrekt die in vermindering kunnen worden gebruikt.
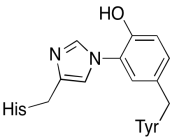
oefening \(\Paginindex{3}\)
laat zien waarom een tyrosine een bron kan zijn van zowel een proton als een elektron in biochemische processen.
antwoord
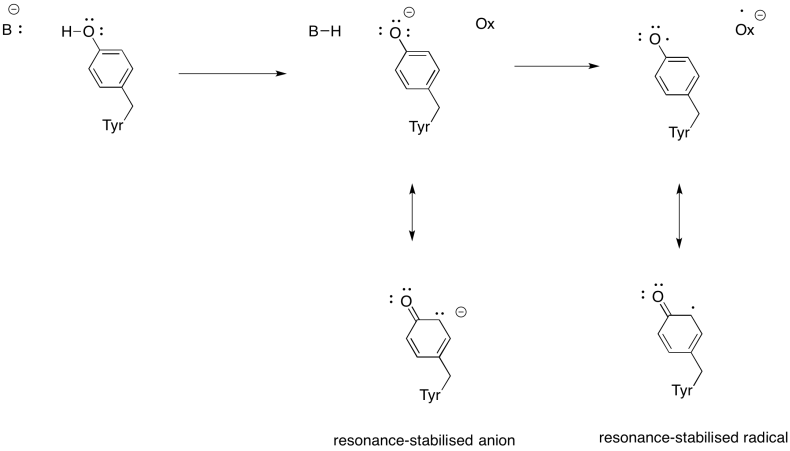
naast de noodzaak om zuurstof te verminderen tot water, Complex IV draagt ook bij aan de Proton gradiënt, pompen extra protonen over het mitochondriale membraan. Die taak brengt extra uitdagingen met zich mee. Een eenvoudig koppelingsmechanisme is niet mogelijk, omdat de elektronen in de tegenovergestelde richting bewegen. Het is echter dat het mechanisme conformational veranderingen in de proteã ne impliceert die aangezien de metalen oxydatiestaten veranderen voorkomen. Subtiele veranderingen in de coördinatieomgeving kunnen leiden tot verplaatsing van aminozuurresiduen in de buurt. Het is gemakkelijk voor te stellen dat als een bepaald aminozuur omhoog naar de intermembrane ruimte verschuift, het een proton mee kan trekken.
- Proton pompen en elektronentransport lopen in tegengestelde richtingen in Complex IV en moeten worden ontkoppeld.
- het pompen van protonen in Complex IV moet gebaseerd zijn op conformationele veranderingen.
oefening \(\Paginindex{4}\)
de Cua site bevat twee koperen, aangewakkerd door twee bruggencysteinen. Beide zijn gebonden door terminale histidines. Bovendien wordt het ene koper gebonden door een extra methionine, terwijl het andere wordt gebonden door een carbonyl uit de proteïne-ruggengraat.
- teken de koper op hun bindingsplaatsen.
- Beschrijf de geometrie van elk koper.
- als elk koper Cu(I) is, wat is dan de gecoördineerde elektronentelling van elk koper in het complex?
- als elk koper Cu(I) is, wat is de totale lading van het complex?
Antwoord a)
een)
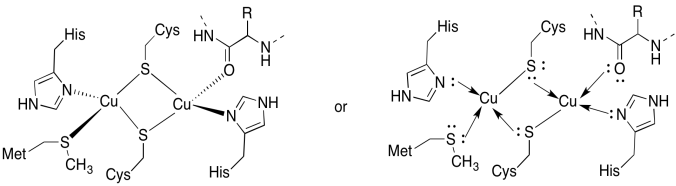
Antwoord b)
b) tetrahedral
Antwoord c)
c) Cu(I) = d10
4 donoren = 8 e-
totaal = 18e-
Antwoord d)
d) 2 x Cu(I) = 2+
2 x-Cys-S- = 2-
Alle anderen neutrale
Totaal = 0
Oefening \(\Pagina{5}\)
het koper in De CuB website is gebonden door twee histidines en de histidine-tyrosine toegevoegd.
- teken het koper op de bindingsplaats.
- Beschrijf de geometrie van het koper.
- als koper Cu(I) is, wat is dan het gecoördineerde aantal elektronen in het complex?
- als koper Cu(I) is, wat is de totale lading van het complex?
Antwoord a)
een)
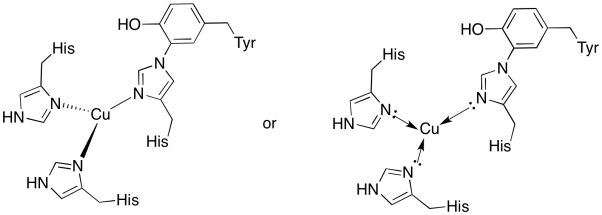
Antwoord b)
b) trigonale vlakke
Antwoord c)
c) Cu(I) = d10
3 donoren = 6 e-
totaal = 16 e-
Antwoord d)
d) Cu(I) = 1+
histidines neutrale
Totaal = 1+
Oefening \(\Pagina{6}\)
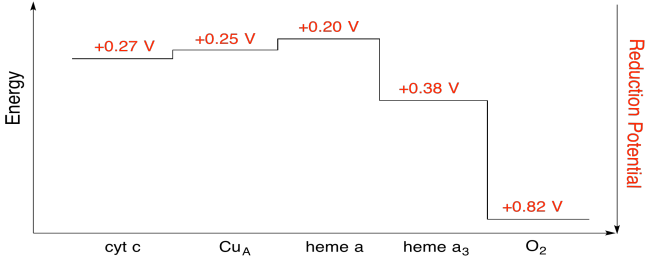
Het is moeilijk te meten is het reductiepotentieel van een individuele website binnen een eiwit. Nochtans, hebben de onderzoekers deze waarden kunnen schatten door EPR spectra onder diverse voorwaarden te meten. Uitgaande van het reductiepotentieel hieronder, teken een reactievooruitgang diagram voor transport van een elektron helemaal van cytochroom C naar moleculaire zuurstof.
 antwoord
antwoord
oefening \(\Paginindex{7}\)
met behulp van de waarden in de figuur hierboven, bereken de energieverandering wanneer een elektron wordt overgebracht van heme A naar heme a3.
antwoord
uitgaande van het reductiepotentieel zijn:
heme a(ox) + e- → heme a(red) Eored = 0,20 V
heme a3(ox) + e- → heme a3 (red) Eored = 0.38 V
Dan worden de mogelijke verschil voor de reactie, ΔEo = 0.38 – (0.20) V = 0.18 V.
De Faraday relatie ΔG = – n F ΔEo geeft
ΔG = – 1 x 96,485 J V-1 mol-1 x 0.13 V = 17,367 J mol-1 = 17.4 kJ mol-1
Naamsvermelding
Chris P Schaller, D. Ph., (College van Sint-Benedictus / Saint John ‘ s University)