Chloride ion kanalen en vervoerders: uit bijzonderheden van aard en bron van de ziekte van medicijnen
Geplaatst: 20 augustus 2013 | |
al Vroeg in hun undergraduate onderwijs, de student kennis met verschillende vormen van integraal membraan eiwit: receptoren, adhesie-eiwitten, ion-kanalen, ion pompen en ion vervoerders. Terwijl zij door hun studies vorderen, ontdekken zij dat discrete genfamilies en eiwitstructuren verantwoordelijk zijn voor deze verschillende eiwitklassen en er is nooit enige reden om te overwegen dat er enige ambiguïteit zou kunnen zijn in het toewijzen van een bepaald eiwit aan zijn aangewezen eiwitklasse.
dit voldoet aan vrijwel elk geval van de klas tot het onderzoekslab totdat we chloridekanalen overwegen. We weten dat ze bestaan, belangrijk zijn en goede drugstreefdoelen kunnen zijn in verschillende ziektegebieden, maar tot voor kort zijn ze in de therapeutiewereld enigszins gestigmatiseerd en uit de mode gebleven. Het ontbreken van selectieve liganden heeft helemaal niet geholpen. De enige uitzondering op dit is GABA geweest-een receptor die aan een intrinsiek chloridekanaal wordt gekoppeld dat op band van de remmende neurotransmitter GABA opent. Benzodiazepines hebben deze receptor versterkt sinds Valium in de jaren 1960 beschikbaar kwam, wat kalmerende en anticonvulsieve effecten heeft. Dit introduceert een belangrijk concept: er zijn verscheidene genfamilies en verschillende eiwittypes die als chloridekanalen kunnen worden beschreven.
dit is in tegenstelling tot wat we begrijpen van kation-selectieve ionenkanalen, waar er weinig flexibiliteit is in de eiwitstructuur die een porie kan vormen die selectief is voor kalium, natrium of calcium; de diversiteit van deze ionenkanalen wordt veroorzaakt door de variaties in de eiwitdomeinen die verschillen van de porie die het Open-sluitgedrag beïnvloeden. Om eerlijk te zijn, lijken er niet veel fysiologische redenen te zijn waarom een anionkanaal chloride-selectiviteit zou moeten vertonen, aangezien er weinig fysiologische rol is in het membraantransport van andere halogeniden of kleine anionen; elk anionkanaal zal standaard een chloridekanaal zijn vanuit fysiologisch oogpunt. Aan de andere kant, kalium, natrium en calcium membraanstromen spelen elk verschillende fundamentele rollen en selectieve membraandoorlaatbaarheid voor deze kationen is cruciaal voor de cellulaire functie en inderdaad het leven zelf.
GABA-A-receptoren zijn leden van de pentamerische ligand-gated ionenkanaalfamilies van de CYS-loop, die verscheidene types van prikkelende en remmende neurotransmitter-gated kanalen omvatten. Het cystic fibrosis transmembrane regulator (CFTR) eiwit is een nucleotide-geregeld chloride kanaal. Het is een lid van de diverse ATP-bindende cassettevervoerder (ABC) familie en is de enige die geen substraat over een membraan schijnt te vervoeren, maar eerder als chloridekanaal functioneert. De CLC-familie van voltage-gated chloridekanalen komt uit een andere verschillende genfamilie voort en heeft een algemene structuur uniek onder membraanproteã nen. Deze familie van eiwitten heeft vele verrassingen gebracht in de afgelopen 30 jaar en leden van deze familie zullen hier worden geïntroduceerd en ook hoe ze kunnen worden beschouwd als drug targets.
andere spannende ontwikkelingen vanuit het chloridekanaalveld zijn naar voren gekomen na de moleculaire identificatie van eiwitten die ten grondslag liggen aan calcium-geactiveerde chloride (ClCa) kanalen. Functioneel, hebben wij over hun fysiologische rollen gekend enige tijd, maar recente moleculaire identificatie van de kanaalproteã nen heeft de ontwikkeling van moleculaire en farmacologische hulpmiddelen toegestaan om hun activiteit te onderzoeken en te veranderen. Dit overzicht richt zich op het farmacologische potentieel van het richten van ClCa-kanalen en CLC-eiwitten; hun functie en subcellulaire lokalisatie zijn samengevat in Figuur 1.
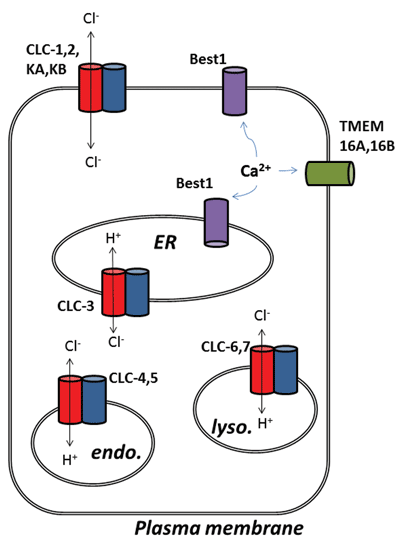
figuur 1
een inleiding tot CLC-eiwitten
de negen leden van deze eiwitfamilie zijn CLC-1 tot 7, CLC-KA en KB. De oprichter, CLC-1, is het voltage-gated chloride kanaal van skeletspieren en zal hieronder worden besproken. Veel functionele studies zijn uitgevoerd op een homoloog met de eretitel CLC-0, geïsoleerd van het electroplax elektrisch orgel, waardoor de straal zijn aquatische slachtoffers kan verdoven. Reconstructie van CLC-0 in lipide bilagen en elektrofysiologische registratie van stromingen die door enkele ionenkanalen stromen onthulde een intrigerende eigenschap. Gewoonlijk, wanneer het opnemen van stroom van een klein Flard van membraan die één enkel ionenkanaal bevat, merkt men schommelingen tussen twee stroomamplitudes op:één die het gesloten kanaal vertegenwoordigt en de andere die de stroom door het open kanaal vertegenwoordigt. De fluctuaties weerspiegelen overgangen tussen open en gesloten kinetische toestanden. Met CLC-0, echter, was het duidelijk dat de enige ionenkanaalproteã ne uit twee gelijkwaardige poriën bestond die onafhankelijk konden openen1. Dit kanaal werd daarom beschreven als een dubbele loop (Figuur 2). Het was dus geen grote verrassing dat de kristalstructuren van homologen van enterische bacteriën onthulden dat het eiwitcomplex een dimeer was, waarbij elke subeenheid een iongeleidende pathway2 bezat (Figuur 2).
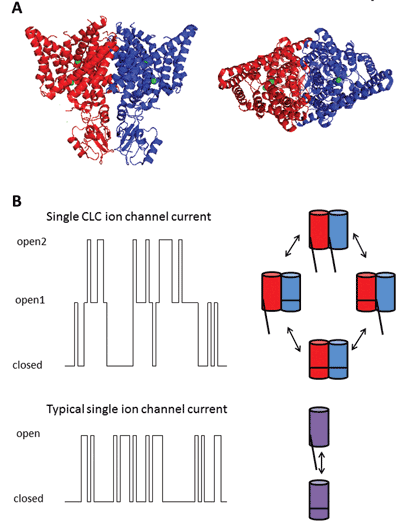
Figuur 2
de tweede verrassing kwam toen gedetailleerde functionele experimenten werden uitgevoerd op CLC-ec1 van E. coli. In plaats van te functioneren als een chloride kanaal, zoals zijn lang verloren familielid in gewervelde skeletspieren, is CLC-ec1 een 2CL-/H+ exchange transporter, of antiporter, met strikte 2:1 exchange stoichiometrie3. Dit eiwit is belangrijk voor de overleving van enterische bacteriën in lage pH4 en zal waarschijnlijk een chloridegradiënt exploiteren om de cellulaire pH op een aanvaardbaar niveau te houden. Prokaryotische CLC ‘ s kunnen daarom het doelwit zijn van remmers voor de behandeling van pathogene E. coli-of Salmonella-infectie4. De ontdekking van ionenwisselingsgedrag stimuleerde op natuurlijke wijze verdere inspanningen om te bepalen of een van deze chloride-voor-proton uitwisseling bestond in zoogdierclc ‘s, in de veronderstelling dat CL–/H+ uitwisseling de ware functie van archetypische CLC’ s zou kunnen zijn en die geïdentificeerd als chloridekanalen slechts uitzonderingen op de regel zouden kunnen zijn. Dit lijkt het geval te zijn omdat er sterk bewijs is dat CLC-3 tot en met CLC-7 functioneren als 2CL- / h+ exchange transporters, voornamelijk woonachtig in intracellulaire organellen, terwijl CLC-1, CLC-2, KA en KB echte plasmamembraan chloride-geleidende ionenkanalen 5-9 zijn. Omdat de archetypische CLC-eigenschap uitwisseltransport is, die over alle vormen van cellulair leven wordt gevonden, kan de laatste subklasse van eiwitten, de bonafide chloridekanalen, daarom worden beschouwd als ‘gebroken’ chloridetransporters, die de koppeling van chloridetransport aan de beweging van een tweede substraat ion hebben verloren.
CLC-1
deze grondlegger van de CLC-familie is het voltage-gated chloride kanaal van skeletspieren en dient om de membraanpotentiaal te regelen en het membraan opnieuw te polariseren na actiepotentialen om de spier te ontspannen. In de meeste weefsels zouden we verwachten dat kaliumkanalen deze rol spelen, wat ze doen in hart-en gladde spieren, evenals het reguleren van membraan exciteerbaarheid in andere celtypen. Het transversale tubulus systeem is een uitbreiding van het plasmamembraan (sarcolemma) en dringt door in het contractiele Weefsel. Het is van cruciaal belang voor de snelle verspreiding van elektrische activiteit door de spier en orkestreert snelle en gecontroleerde samentrekking. Kalium efflux van de spiercellen in de beperkte ruimte van de T-tubule zou de extracellulaire kaliumconcentratie verhogen en deze iongradiënt doen instorten, wat zou leiden tot langdurige membraandepolarisatie. Met chloridekanalen die de overheersende repolariserende rol spelen, wordt dit voorkomen. Verlies van functiemutaties in CLC-1 leiden tot myotonie bij de mens, geiten en muizen (voor een recente beoordeling Zie 10) en wordt gekenmerkt door verminderde spierontspanning, consistent met het verlies van een repolariserende membraanstroom.
met expressie beperkt tot skeletspieren, kan CLC-1 een aantrekkelijk doelwit zijn voor geneesmiddelen die spiercontractie onder controle houden door de CLC-1-functie te verhogen of te verlagen en daardoor respectievelijk de spier exciteerbaarheid te verminderen of te verhogen. Verbindingen die de CLC-1-functie verhogen, zouden myotonie kunnen behandelen, in het bijzonder in gevallen waarin zij gedeeltelijk verlies van chloridekanaalactiviteit zouden kunnen compenseren. Remming van CLC-1 kan de drempel voor spiercontractie verlagen en kan nuttig zijn in gevallen van spierzwakte of degeneratieve ziekten zoals spierdystrofie.
CLC-2
het naar binnen gerichte chloridekanaal, CLC-2, heeft een enigszins wijdverbreide weefseldistributie. Het kan worden gevonden in centrale neuronen waar het neuronale activiteit reguleert 11-13. In astrocyten wordt het subcellulaire targeting op celverbindingen gereguleerd door een interactie met GlialCAM (MLC1), mutaties waarbij dit targeting wordt verstoord en megalencefalische leuko-encefalopathie14 wordt veroorzaakt. Recente therapeutische belangen betrekken CLC-2 expressie in darmslijmvlies en Long bronchiolen waar het een rol speelt in intestinale en Long secreties, respectievelijk. Lubiprostone, een medicijn dat klinisch wordt gebruikt om constipatie te verlichten, werd voorgesteld om zijn effect uit te oefenen door CLC-2 te activeren, maar dit effect is controversieel. Terwijl deze samenstelling CLC-2 kanalen in sommige studies activeert, in andere reguleert het de handel van CLC-2 en verhoogt CFTR functie via prostaglandine receptor activation15, 16. Er blijft echter voldoende bewijs dat de toenemende CLC – 2-functie van de luchtwegen een alternatieve chlorideweg in cystische fibrosis kan leveren17.
CLC-KA / KB
deze chloridekanalen worden met name uitgedrukt in renale epithelie en dragen bij tot de permeabiliteit van celmembranen voor passieve chlorideflux. Zij spelen een belangrijke rol in de opgaande ledemaat en distale tubuli van het nefron, die een basolaterale route voor chloride reabsorptie verstrekken, na transport van de primaire urine via het apicale membraan. Het clckb-gen, dat codeert voor CLC-KB, is een van de vijf genen die ten grondslag liggen aan het Bartter-syndroom. Verlies-van-functie veranderingen in CLC-KB resulteren in defecte chloride reabsorptie en zo leidt tot een zout-wasting stoornis, die wordt geassocieerd met polyurie. Een van de belangrijkste kenmerken van individuen die worden beïnvloed door CLC-KB mutaties (Bartter ‘ s type III) is lage bloeddruk. Een ernstigere vorm van de ziekte wordt veroorzaakt door mutaties in het bsnd-gen (Bartter ‘ s type IV), dat codeert voor Barttin, een bijkomend eiwit dat belangrijk is voor het transport van zowel CLC-KA als KB naar de plasmamembrane18. Deze vorm van de wanorde omvat ook zintuiglijke doofheid, die door het verlies van handel van zowel CLC-KA als KB aan epitheliaale membranen in binnenoor wordt verondersteld worden veroorzaakt. Vermoedelijk kan verlies van CLC-KA Of KB activiteit, maar niet beide, worden getolereerd door het auditieve systeem. Dit suggereert dat selectieve remmers voor CLC-KA of CLC-KB, of gedeeltelijke remming van beide, kunnen werken als een nieuw lisdiureticum met de mogelijkheid om de bloeddruk te verlagen en met weinig bijwerkingen. Dit heeft geleid tot de studie van hun farmacologie en de ontwikkeling van nieuwe remmers met een lage micromolaire affiniteit19, die diuretische effecten hadden bij toediening aan rats20. Aan de andere kant kunnen geneesmiddelen die CLC-KB-kanalen activeren de resterende activiteit van defecte kanalen bij bartters type III-patiënten versterken.
CLC-7
van de subklasse 2CL- / h+ exchange transporter is CLC-7 Een veelbelovend doelwit voor geneesmiddelwerking en de remming ervan kan gunstig zijn bij osteoporose. Nogmaals, deze indicatie ontleent zijn oorsprong aan waarnemingen van menselijke ziekte veroorzaakt door verlies-van-functie mutaties in CLC-7, die osteropetrosis21 veroorzaken. In deze wanorde, is het bot remodelleren door osteoclasten deficiënt, die om door gebrekkige zure en enzymsecretie wordt verondersteld te worden veroorzaakt. Dit leidt tot dicht bot, dat,indien gereproduceerd door een CLC-7-remmer, de ontbinding van bot kan verminderen en daarom het skelet van osteoporosepatiënten22, 23 kan versterken. In proof-of-concept-studies verminderde farmacologische remming van de verzuring 24 of verstoring van de CLC-7-functie door antibondies25 de botresorptie. De remming van CLC-7 kan echter niet zonder complicaties zijn omdat studies bij mensen en muizen suggereren dat het gebrek aan CLC-7-functie ook geassocieerd kan worden met neuronale opslag en degeneratiestoornissen vanwege verminderde lysosomale functie26.
loss-of-function humane mutaties – lessons from CFTR
het is de moeite waard om hier even stil te staan bij het feit dat sommige van de Therapeutische indicaties voor nieuwe op CLC gerichte geneesmiddelen gericht zijn op de behandeling van stoornissen die verschillend zijn en aan de andere kant van het spectrum dan die welke worden veroorzaakt door een defecte CLC-functie. Naast de hierboven beschreven, Dent ‘ s i ziekte is een X-gebonden nierziekte die wordt veroorzaakt door het verlies van CLC – 5 functie (zie27 voor een recent overzicht). Allen zijn zeldzame geërfde wanorde en een belangrijk eiwitdefect impliceert of verminderde eiwitactiviteit of het verkeer naar het doelmembraan. In feite, veroorzaken vele individuele veranderingen ER-behoud en een gebrek aan eiwitrijping. Een parallel zou met cystic fibrosis kunnen worden gemaakt, met de meeste beà nvloede individuen die de er-behouden ΔF508 verandering bezitten. Recente en gestratificeerde benaderingen van de behandeling van cystische fibrose zijn het resultaat van een dual-protonged aanval om mutant eiwit folding (CF correctoren) te corrigeren en/of de activiteit van plasma membraan CFTR chloride kanalen (CF potentiatoren) te verhogen. Met de potentiatorklass28, die effectief zijn bij patiënten met mutaties die de CFTR-activiteit verminderen zonder verlies van eiwitbiosynthese of handel (bv. G551D), is succes aan het worden, maar de effectiviteit van vouwcorrectoren (die in de meeste gevallen vereist is) moet nog worden vastgesteld29. Hoewel de ziekten geassocieerd met verlies van CLC-functie zijn allemaal zeldzame genetische aandoeningen, kunnen we op een dag in staat zijn om mensen met myotonie, Bartter ‘ s syndroom, de ziekte van Dent en osteopetrose, evenals cystische fibrose te behandelen met geneesmiddelen die de werkelijke oorzaak van hun aandoening te corrigeren.
Calcium-geactiveerde chloridekanalen
ten slotte zal melding worden gemaakt van calcium-geactiveerde chloridekanalen (ClCa), die duidelijk gedefinieerde fysiologische rollen hebben in een aantal celtypen, maar hun moleculaire identificatie leed enkele valse en stotterde starts. Het verhaal gaat over vier soorten eiwitten: leden van CLCA, Bestrophin, Tweety en tmem16 genfamilies. In alle gevallen resulteerde hun recombinante overexpressie in de vorming van membraanchloridestromen die worden gestimuleerd door verhoging van de intracellulaire calciumconcentratie en, in verschillende mate, membraandepolarisatie. De reis voor CLCA kwam tot een einde toen men vond dat dit een eiwit was dat werd afgescheiden, maar waarschijnlijk ook de membraanuitdrukking van CLCA-kanalen endogeen aan het uitdrukkingssysteem30 opreguleerde. Tweety en Bestrofine proteã nen vertonen niet alle eigenschappen van ClCa-kanalen die in belangrijke weefsels worden bestudeerd, hoewel Best1 verantwoordelijk lijkt voor een component van ClCa in sensorische neuronen31 en ook een belangrijke regulator kan zijn van calciumafgifte uit het endoplasmatisch reticulum32,33. Drie onafhankelijke studies stelden TMEM16A (ook wel Ano1 genoemd) voor als kandidaat voor een belangrijke component, zo niet in zijn geheel, voor een calcium-geactiveerde chloridekanaal34-36. Vele latere studies, vergemakkelijkt door de generatie van moleculaire hulpmiddelen, hebben dit ondersteund. TMEM16A is belangrijk voor het reguleren van membraan exciteerbaarheid in vasculaire gladde spier, is upregulated in een diermodel van pulmonale hypertensie en tonus kan worden verminderd door kanaalrehibition37, 38. In sensorische neuronen koppelt TMEM16A de aanwezigheid van inflammatoire mediatoren aan membraanhyperexcitatie en de remming van TMEM16A heeft antinociceptieve effecten39. In dierlijke modellen van astma, wordt de uitdrukking van dit bijzondere chloridekanaal verhoogd, en zijn remming kan gunstige gevolgen hebben40. Het wordt ook gevonden in interstitiële cellen van Cajal van de darm en kanaalfunctie is vereist voor de ritmische samentrekking van gladde spieren in de darmwand41. Voorts kan de activering van TMEM16A een alternatieve weg voor epitheliale chloridesecretie in cystic fibrosis42 verstrekken. Hoewel er nog enige discussie is over de precieze functie van de rest van de tmem16-familie, is de ClCa-functie ook toegeschreven aan TMEM16B (Ano2), waarvan wordt gedacht dat deze ten grondslag ligt aan het CLCA-kanaal in olfactorische haarcelen43,44. Er kunnen ook rollen voor deze klasse van ionenkanaal in de biologie van de kankercel zijn en zijn remming kan celproliferation45-48 verhinderen.
slotopmerkingen
dit overzicht heeft de verschillende rollen van chloride geleidende of transporterende eiwitten aan het licht gebracht en hoe hun disfunctie gekoppeld is aan menselijke stoornis of ziekteachtige symptomen in diermodellen. Er is een ernstig gebrek aan farmacologische reagentia die membraanhandel van chloridekanalen en transporters remmen, activeren of verbeteren. Er wordt vooruitgang geboekt met medicijnen die de defecte functie van CFTR bij cystische fibrose omkeren, wat hopelijk zal resulteren in medicijnen die specifiek zijn voor de verschillende soorten erfelijke mutatie. De Inhibitors en activators van tmem16a calcium-geactiveerde chloridekanalen42,49 blijken nuttige laboratoriumhulpmiddelen te zijn en nieuwe samenstellingen zouden efficiënte drugs kunnen maken, vooral als zij weefsel-specifieke gevolgen kunnen leveren. Moleculen specifiek voor bepaalde CLC ‘ s zijn waarschijnlijk de meest ongrijpbare. Het begrijpen van de structurele basis van voltage-gated CLC activation50 zou eiwitdomeinen kunnen identificeren die door rationeel structuur-gebaseerd drugontwerp targetable zijn. Dergelijke instrumenten zullen ons in staat stellen om een aantal van de nieuwe therapeutische ideeën die hier zijn herzien en gepresenteerd op de proef te stellen.
biografie van de auteur

Jon Lippiat promoveerde op de structuur, functie en farmacologie van kaliumkanalen aan de Universiteit van Leicester. Hij studeerde pancreatische bètacelfunctie en diabetes aan de Universiteit van Oxford voor zijn benoeming tot docent farmacologie aan de Universiteit van Leeds. Zijn onderzoek omvat het ophelderen van de structurele en fysiologische eigenschappen van verschillende types van ionenkanaal en transporter en hun potentiële targeting door nieuwe farmacologische reagentia.
uitgave
uitgave 4 2013
gerelateerde onderwerpen
chloridekanalen, drug Targets, ionenkanalen