Cytomegalovirus (CMV) – infectie bij HIV/AIDS-patiënten en diagnostische waarden voor CMV-DNA-detectie in verschillende monstertypen
- Inleiding
- methoden
- proefpersonen
- inclusie en uitsluiting
- reagentia en apparatuur
- HIV-RNA-kwantificering
- CD4 + T lymfocytentelling
- CMV-DNA-kwantificering
- CMV-antilichaamtest
- studiemethoden
- nucleïnezuurdetectie
- detectie van T-lymfocyten subgroepen
- detectie van immuunantilichamen
- statistische analyse
- resultaten
- algemene gegevens
- positieve percentages CMV-DNA, CMV-IgG en CMV-IgM
- correlatie tussen CMV-infectie en CD4+ T-lymfocytentelling
- detectie van CMV-DNA in verschillende monsters
- Discussie
- conclusies
- Dankbetuigingen
- voetnoot
Inleiding
Cytomegalovirus (CMV) is een veel voorkomend herpesvirus dat wijdverspreid is over menselijke populaties. CMV-infectie veroorzaakt meestal geen symptomen en treft voornamelijk de speekselklieren, nieren en andere organen. Echter, virale replicatie kan optreden bij immunogecompromitteerde patiënten en kan bijdragen aan de schade aan organen en hun functies. Opportunistische infecties komen vaker voor en zijn ernstiger bij HIV/AIDS-patiënten. CMV-virusinfectie komt vaak voor bij deze patiënten en kan meerdere organen/systemen aantasten, waaronder de ogen, longen, het zenuwstelsel en het spijsverteringsstelsel. Vele studies hebben de virologische en immunologische kenmerken van eenvoudige CMV-infectie (1) onderzocht, met name die welke bij vrouwen en kinderen worden gevonden. De immunologische kenmerken van CMV-infectie zijn echter vrij uniek bij reeds immuungecompromitteerde HIV/AIDS-patiënten. Er zijn verschillen in klinische kenmerken, behandelingsmaatstaven en prognostische factoren tussen HIV-patiënten met CMV-infectie en patiënten met CMV-infectie alleen (2). De richtlijn van China aanbevolen dat onmiddellijk antivirale therapie van CMV en ART nodig zijn bij HIV / AIDS patiënten met complicaties (retinitis, longontsteking, CMV encefalitis, enteritis, enz.) wanneer CMV-infectie wordt vastgesteld. Vanwege de niet-specificiteit van klinische symptomen veroorzaakt door CMV-infectie, is laboratoriumonderzoek de belangrijkste basis voor de diagnose van CMV-infectie. De meest twee veelgebruikte klinische methoden zijn CMV-virusreplicatie en serumimmunologische methoden, waaronder de detectie van CMV IgG, CMV IgM en CMV-antigeen PP65 (2) bij patiënten met een verminderde immuunfunctie is de productie van CMV-antilichaam verzwakt of vertraagd, wat kan leiden tot vals-negatief en de snelheid van gemiste diagnose kan verhogen, daarom is PCR-detectie van CMV-DNA grotendeels de standaardmethode geworden voor de diagnose van CMV-infectie en monitoring van de behandeling (3). Daisuke Mizushima et al. gemeld dat plasma CMV-DNA-PCR een belangrijke waarde heeft voor de diagnose van zowel CMV-retinitis als alle CMV-EOD bij patiënten met gevorderde HIV-1-infectie (4). CMV-DNA PCR kan in een verscheidenheid van steekproeftypes zoals plasma, urine, cerebrospinale vloeistof, waterig humor, uitwerpselen, enz.worden ontdekt. (5). Nochtans, hebben weinig artikelen de betekenis en de waarde van CMV-DNA PCR opsporing in steekproeven buiten plasma geanalyseerd en besproken. In de huidige studie hebben we retrospectief de laboratoriumtesten geanalyseerd (waaronder CMV-DNA, CMV antilichaam, CD4 + T lymfocyten telling, HIV viral load, etc.) in 808 HIV / AIDS patiënten die in ons centrum werden behandeld van 2017 tot 2019 om de CMV co-infectie en de sterke en zwakke punten van verschillende detectiemethoden te begrijpen. We presenteren het volgende artikel / geval in overeenstemming met de mdar reporting checklist (beschikbaar op http://dx.doi.org/10.21037/apm-20-1352).
methoden
proefpersonen
in totaal werden 808 HIV/AIDS-patiënten die tussen januari 2017 en oktober 2019 in ons centrum waren opgenomen, ingeschreven. Bij elke patiënt werden HIV-RNA, CD4+ T lymfocytentelling, CMV-DNA en verwante antilichamen gemeten. De diagnose van HIV-infectie was gebaseerd op de HIV/AIDS diagnose en behandeling richtlijnen (derde editie) (6), en alle patiënten werden bevestigd als HIV-infectie door de Fuzhou Municipal Centers for Disease Control (CDC) of de lokale CDC die de patiënt behandeld. De diagnose van CMV-infectie was gebaseerd op de volgende criteria: (I) CMV-DNA-positief in plasma, alveolaire spoelvloeistof, urine, cerebrospinale vloeistof (CSF) en / of andere lichaamsvloeistoffen; (II) CMV-immunoglobuline M (IgM) – positief in serum; (III) een oftalmologische diagnose van CMV-retinitis; (IV) CMV longontsteking vooral manifesteren als koorts, hoesten, slijm en benauwdheid; CMV-DNA-positief in de alveolaire lavage vloeistof; (V) CMV-enteritis of oesofagitis vooral manifesteren als dysfagie/slikproblemen pijn, diarree of buikpijn, en effectieve diagnostische anti-CMV behandeling; (VI) de CMV encefalitis manifesteren als zenuwstelsel symptomen en CMV-DNA-positief in LIQUOR of hersenweefsel; (VII) CMV hepatitis manifesteren als koorts, abnormale leverfunctie, en een onaangenaam gevoel in de lever gebied, en CMV-DNA-positief in leverbiopsie. Een diagnose van CMV-infectie werd gesteld als aan een van de bovenstaande criteria, met uitzondering van punt II), werd voldaan of als aan punt II) plus een ander criterium werd voldaan (7).
alle procedures die in dit onderzoek met menselijke deelnemers werden uitgevoerd, waren in overeenstemming met de Verklaring van Helsinki (herziene versie van 2013). De studie werd goedgekeurd door de medische ethische commissie van ons centrum (goedkeuring nr. KS2019-070-01). De gegevens zijn anoniem en daarom werd afgezien van de vereiste geïnformeerde toestemming.
inclusie en uitsluiting
inclusiecriteria: patiënten met HIV/AIDS die voor het eerst het Mengchao Hepatobiliary Hospital van de Fujian Medical University bezochten en binnen 14 dagen de detectie van HIV-RNA, CMV-DNA, CMV-IgG-antilichaam, CMV-IgM-antilichaam en CD4+ T-lymfocyten voltooiden. Sluit HIV / AIDS-gevallen uit die de bovenstaande testpunten niet kunnen voltooien wegens onvoldoende steekproefgrootte.
reagentia en apparatuur
HIV-RNA-kwantificering
Fluorescerende kwantitatieve real-time polymerasekettingreactie (PCR) (FQ-PCR) werd uitgevoerd op het MX3000P QPCR-systeem (Agilent, USA) door gebruik te maken van de HIV-RNA-kwantificeringskit geproduceerd door QiaGen (Shenzhen, China).
CD4 + T lymfocytentelling
het gebruikte instrument was de FACSCalibur flow cytometer (BD Biosciences, USA) en de gebruikte reagenskit was Bd Multitest CD3/CD4/CD8/CD45 (BD Biosciences, USA).
CMV-DNA-kwantificering
FQ-PCR werd uitgevoerd op het MX3000P QPCR-systeem (Agilent, USA) om de CMV-DNA-spiegels in plasma, urine en CSF te detecteren. De gebruikte kit werd geproduceerd door Sansure Biotech (Hunan, China).
CMV-antilichaamtest
chemiluminescentie-immunoassay werd uitgevoerd om anti-CMV-IgG-en IgM-antilichamen te detecteren op de cobas e601-analysator (Roche Diagnostics, Duitsland) met de ondersteunende kits (Roche Diagnostics, Duitsland).
studiemethoden
nucleïnezuurdetectie
nadat de HIV / AIDS-patiënten in ons ziekenhuis waren opgenomen, werd 3 mL nuchtere ethyleendiaminetetra-azijnzuur (EDTA)-anticoagulated volbloed monster verzameld en vervolgens gecentrifugeerd bij 3.000 r/min gedurende 5 minuten om 200 µL plasma te oogsten voor HIV-RNA en CMV-DNA detectie. Bij alle patiënten werd ‘ s ochtends 5 mL urinemonster verzameld en grondig gemengd, waarna 200 µL werd geoogst voor CMV-DNA-detectie. Voor patiënten met neurologische symptomen werd 1 mL liquor verkregen voor CMV-DNA detectie. Volgens de detectielimiet en de positieve beoordelingsnorm van CMV-DNA-kit en HIV-RNA-kit. De monsters werden als positief beschouwd als de CMV-DNA-waarde hoger was dan 400 kopieën/mL, of als de HIV-RNA-waarde hoger was dan 500 kopieën / mL.
detectie van T-lymfocyten subgroepen
bij HIV / AIDS patiënten werd 3 mL EDTA-anticoagulated vasten volbloed monster verzameld bij opname en vervolgens grondig gemengd voor T-lymfocyten subgroepen detectie op een BD FACSCalibur flow cytometer met behulp van de ondersteunende reagentia.
detectie van immuunantilichamen
bij HIV / AIDS-patiënten werd bij opname 3 mL van het nuchtere bloedmonster verzameld, gedurende 5 minuten gecentrifugeerd met 3.000 r/min in een serumbuis met gelafscheider en vervolgens getest op de machine.
alle bovengenoemde tests werden strikt uitgevoerd volgens de reagensinstructies in de handleiding van de fabrikant en de standaardwerkvoorschriften van de werktuigen.
statistische analyse
statistische analyse werd uitgevoerd met behulp van SPSS 21.0-software. De normaal gedistribueerde meetgegevens worden weergegeven met behulp van gemiddelde ± standaarddeviatie ( x ±SD) en niet-normaal gedistribueerde gegevens worden uitgedrukt als mediaan (25-75 percentielen). De telgegevens worden uitgedrukt in percentages en percentages. De vergelijking van de niet-normaal verspreide meetgegevens tussen twee groepen werd uitgevoerd met behulp van een niet-parametrische rank sum test, terwijl de telling gegevens werden vergeleken met behulp van de Chi-kwadraat test. Een p-waarde van <0,05 werd statistisch significant geacht.
resultaten
algemene gegevens
de algemene gegevens van 808 HIV/AIDS-patiënten zijn samengevat in Tabel 1. Het geslacht en de leeftijd lieten geen significant verschil zien tussen de CMV-groep en de niet-CMV-groep. De absolute CD4-telling in de met CMV geïnfecteerde groep was significant lager dan die in de niet met CMV geïnfecteerde groep (Z=-8,87, P<0,001) en de HIV-RNA-spiegel was significant hoger in de met CMV geïnfecteerde groep dan in de niet met CMV geïnfecteerde groep (Z=-3,207, P<0,05) (Tabel 1).
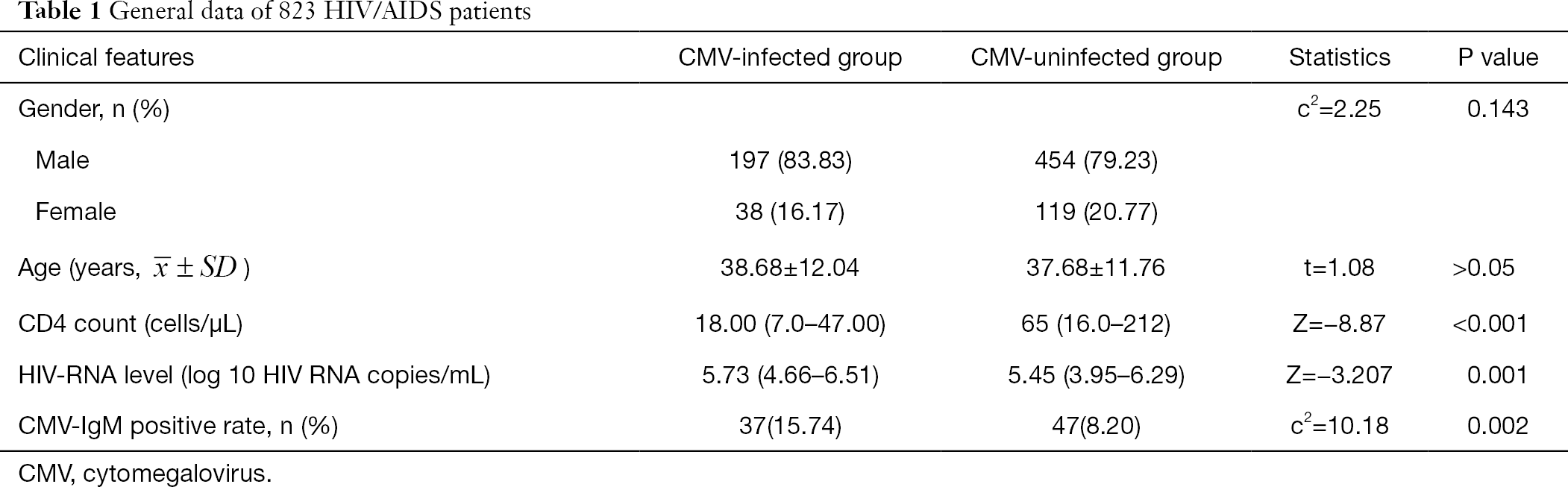
volledige tabel
positieve percentages CMV-DNA, CMV-IgG en CMV-IgM
het totale positieve percentage CMV-DNA was 29,08% (235/808); specifiek was het 5,70% (13/228) in CSF 26,01% (77/296) in plasma en 25,75% (180/699) in urine. Het positieve tarief van CMV-IgG was 99,8% (806/808), en het positieve tarief van CMV-IgM was 10,40% (84/808).
correlatie tussen CMV-infectie en CD4+ T-lymfocytentelling
na groepering van de CD4 + T-lymfocytentelling, vonden we dat het percentage patiënten dat met het cytomegalovirus was geïnfecteerd bij lage frequentie van CD4+ T-lymfocytentelling groter was dan dat van niet-CMV-geïnfecteerde patiënten. De incidentie van CMV-infectie nam toe met de afname van het aantal CD4 (Tabel 2).
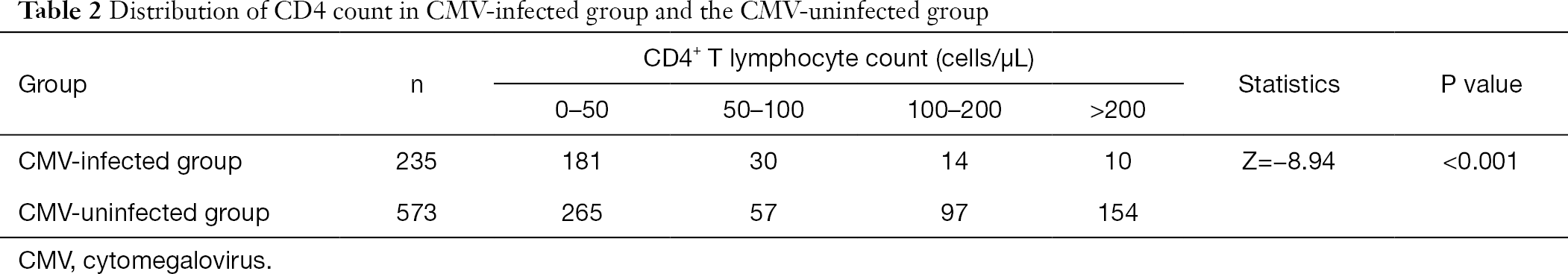
volledige tabel
detectie van CMV-DNA in verschillende monsters
van deze 808 patiënten ontvingen 198 patiënten ook tests voor plasma en urine CMV-DNA en plasma anti-CMV-IgG en CMV-IgM antilichamen. Door gebruik te maken van de Chi-kwadraat analyse voor gepaarde data, voerden we paarsgewijze vergelijkingen uit van respectievelijk urine CMV-DNA en plasma CMV-DNA met plasma CMV-IgM antilichaam. Er werd vastgesteld dat de resultaten van CMV-DNA-detectie in urine en plasma significant verschilden van die van CMV-IgG-antilichaamtest in plasma (P<0,001), terwijl het resultaat van CMV-DNA-detectie in plasma niet significant verschilde van die van CMV-DNA-detectie in urine (P>0,05) (tabel 3,4).

Volledige tabel
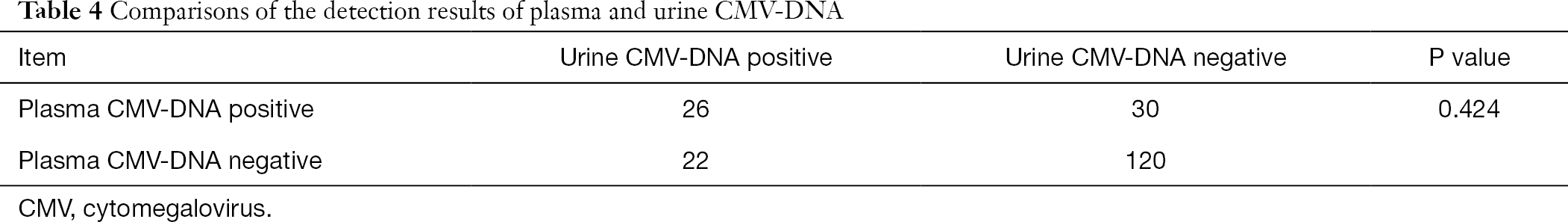
Volledige tabel
Discussie
CMV is een lid van de β-herpes virus groep en wordt gekenmerkt door de strikte soorten specificiteit en de wijdverbreide incidentie in menselijke populaties. CMV-seroprevalentie is ongeveer 85% bij kinderen en tot 95% bij volwassenen. In onze huidige studie bereikte het positieve percentage CMV-IgG 99,8%. CMV is in de meeste gevallen latent, maar bij immuungecompromitteerde personen vermenigvuldigt het virus zich exponentieel en verspreidt het zich door het lichaam met het bloed, waardoor CMV-viremie en zelfs organische CMV-ziekte worden veroorzaakt (8). CMV-infectie is een van de vaak voorkomende opportunistische infecties bij HIV/AIDS-patiënten. CD4 + T-lymfocyten zijn de doelcellen van het HIV-virus, en hun tellingen kunnen vaak het verloop van AIDS weerspiegelen en kunnen ook worden gebruikt als indicator voor het evalueren van de immune status van AIDS-patiënten. Deze studie analyseerde de CMV-infectie, CD4-telling en het HIV-RNA-niveau bij 808 patiënten met HIV/AIDS. We vonden dat het positieve percentage CMV bij AIDS-patiënten steeg met de afname van CD4-telling en met de toename van HIV viral load. Ook in onze huidige studie had tot 77,02% van de CMV-positieve patiënten een CD4-telling van < 50 cellen/µL, wat suggereert dat CD4 <50 cellen / µL een risicofactor is voor HIV-CMV co-infectie, wat consistent is met de bevinding van Deng et al. (9). Het kwantitatieve niveau van HIV-RNA in de met CMV geïnfecteerde groep was hoger dan dat in de niet met CMV geïnfecteerde groep, wat er indirect op wees dat hoge niveaus van HIV-RNA viral load een andere risicofactor was voor CMV-infectie bij HIV/AIDS-patiënten .Daarom wordt aanbevolen dat patiënten met HIV/AIDS zo snel mogelijk een ART-behandeling starten om immuunreconstitutie te bevorderen om opportunistische infecties te voorkomen en screening op HCMV is essentieel voor HIV/AIDS-patiënten met een CD4-telling van <50 cellen/µL (2).
we evalueerden ook de waarden van virale nucleic zuur assays en immunologische methoden in de klinische detectie van CMV infectie. Studies in China en internationaal hebben aangetoond dat CMV-DNA eerder verschijnt dan de klinische symptomen en serologische reacties van CMV-infecties. FQ-PCR is momenteel de nauwkeurigste en snelle microbiële kwantificeringsmethode en kan sommige problemen van traditionele PCR (b.v., verontreiniging van het versterkingsproduct en niet-kwantificering) overwinnen (10). In onze huidige studie was het positieve percentage CMV-DNA 5.70% (13/228) in de CSF-monsters van 228 patiënten met neurologische symptomen, wat veel lager was dan die in plasma-en urinemonsters, wat kan worden verklaard door de bloed-hersenbarrière en gevoeligheid voor organen. Het anti-CMV-IgM antilichaam wordt vaak gebruikt als een marker van actieve virale infectie; echter, het positieve percentage van het anti-CMV-IgM antilichaam was slechts 10,40% (84/808) in onze HIV/AIDS patiënten, wat lager was dan het positieve percentage van CMV infectie gemeld in de niet-HIV/AIDS populaties (11). Bovendien was het positieve percentage slecht afgestemd op de resultaten van de detectie van nucleïnezuur, wat te wijten zou kunnen zijn aan het verzwakte immuunsysteem of aan de vertraagde aanmaak van IgM-antilichamen bij HIV/AIDS-patiënten. Daarom speelt de detectie van CMV-IgM antilichaam een beperkte rol bij HCMV screening bij HIV/AIDS patiënten. Bovendien was het positieve percentage CMV-infecties bij 808 patiënten 29,05% (235/808) in onze huidige studie, wat iets hoger is dan de 21,85% die door Li et al., en kan het gevolg zijn van de grotere verscheidenheid aan monsters (waaronder plasma, urine en CSF) die in dit onderzoek zijn verzameld (12). Het positieve percentage CMV-DNA was 25,57% in urine en 26,01% in plasma, het verschil was niet statistisch significant. Daarom raden wij aan CMV-DNA-screening in plasma en urine uit te voeren wanneer het aantal CD4+ T lymfocyten lager is dan 200 cellen/µL, in het bijzonder wanneer <50 cellen/µL; daarnaast is detectie van CMV-DNA in CSF vereist als er duidelijke neurologische symptomen aanwezig zijn.
conclusies
concluderend zijn lage CD4 + T lymfocyten en hoge HIV-1 viral load risicofactoren voor CMV-infectie bij HIV/AIDS-patiënten. Detectie van CMV-DNA in urine of plasma door FQ-PCR is zeer waardevol bij de screening van CMV-infectie bij HIV/AIDS-patiënten, terwijl de detectie van CMV IgG-en CMV IgM-spiegels in het bloed een beperkte klinische waarde heeft. CMV-DNA-screening in bloed of urine wordt aanbevolen voor AIDS-patiënten om CMV-infectie vroegtijdig te voorkomen en te diagnosticeren en hun levenskwaliteit te verbeteren.
Dankbetuigingen
financiering: gesponsord door Key Clinical Specialty Discipline Construction Program van Fujian, P. R. C.
voetnoot
rapportage Checklist: de auteurs hebben de mdar rapportage checklist voltooid. Beschikbaar op http://dx.doi.org/10.21037/apm-20-1352
Gegevensuitwisselingsverklaring: beschikbaar op http://dx.doi.org/10.21037/apm-20-1352
belangenconflicten: alle auteurs hebben het icmje uniform disclosure form ingevuld (beschikbaar op http://dx.doi.org/10.21037/apm-20-1352). De auteurs hebben geen belangenconflicten aan te geven.
ethische verklaring: de auteurs zijn verantwoordelijk voor alle aspecten van het werk door ervoor te zorgen dat vragen met betrekking tot de juistheid of integriteit van enig deel van het werk naar behoren worden onderzocht en opgelost. Alle procedures die in dit onderzoek met menselijke deelnemers werden uitgevoerd, waren in overeenstemming met de Verklaring van Helsinki (zoals herzien in 2013). De studie werd goedgekeurd door de medische ethische commissie van ons centrum (goedkeuring nr. KS2019-070-01). De gegevens zijn anoniem en daarom werd afgezien van de vereiste geïnformeerde toestemming.
Open Access verklaring: Dit is een open Access artikel gedistribueerd in overeenstemming met de Creative Commons Attribution-NonCommercial-NoDerivs 4.0 International License (CC BY-NC-ND 4.0), die de niet-commerciële replicatie en verspreiding van het artikel mogelijk maakt met de strikte voorwaarde dat er geen wijzigingen of wijzigingen worden aangebracht en dat het oorspronkelijke werk naar behoren wordt geciteerd (inclusief links naar zowel de formele publicatie via de relevante DOI en de licentie). Zie: https://creativecommons.org/licenses/by-nc-nd/4.0/.
- Yu X, Tong M, He G. effecten van cytomegalovirus infectie op regulerende immuuncellen bij zwangere Chinese vrouwen. Journal of Nosocomiology. 2017;27:2103-6.
- de National Science and Technology Major Project helpt opportunistic infection Research Group tijdens het 13e vijfjarenplan. Deskundige consensus over klinische diagnose en behandeling van AIDS gecompliceerd met cytomegalovirus ziekte . Journal of Southwest University (Natural Science Edition): 1-17 .
- Hodowanec AC, Pikis A, Komatsu te, et al. Behandeling en preventie van CMV-ziekte bij transplantatieontvangers: huidige kennis en toekomstperspectieven. J Clin Pharmacol 2019; 59: 784-98.
- Mizushima D, Nishijima T, Yashiro s, et al. Diagnostisch Nut van kwantitatieve plasma cytomegalovirus DNA PCR voor cytomegalovirus end-orgaan ziekten in patiënten met hiv-1 infectie. J Acquir Immune Defic Syndr 2015; 68:140-6.
- Michaelides A, Liolios L, Glare EM, et al. Verhoogde DNA-belasting van humaan cytomegalovirus (HCMV) in perifere bloed leukocyten na longtransplantatie correleert met HCMV pneumonitis. Transplantatie 2001; 72: 141-7.
- the infection of neurology, AIDS group of Chinese medical association. Richtlijnen voor de diagnose en behandeling van HIV/AIDS (derde editie). Chinese Journal of Infectious Diseases 2015; (10): 577-93.
- Corrales I, Giménez E, Solano C, et al. Incidentie en dynamiek van actieve cytomegalovirusinfectie bij allogene stamceltransplantatiepatiënten volgens enkelvoudige nucleotidepolymorfismen in donor-en recipiente CCR5 -, MCP-1 -, IL-10-en TLR9-genen. J Med Virol 2015; 87: 248-55.
- Tagarro A, Del Valle R, Dominguez-Rodríguez S, et al. Groeipatronen bij kinderen met een aangeboren Cytomegalovirus-infectie. Pediatr Infecteren Dis J 2019; 38: 1230-5.
- Deng X, Liu J, Zhang M, et al. Analyse van virologische en immunologische kenmerken van HIV / AIDS gecombineerd met cytomegalovirus infectie. Chinese Journal of Hospital Infection 2019; 29: 2241-6.
- Kawano Y, Kawada J, Kamya Y, et al. Analyse van circulerende humane en virale microRNA sin patiënten met congenitale cytomegalovirus infectie. J Perinatol 2016; 36: 1101-5.
- Li l, Gao S, Zhang T, et al. Vergelijking van DNA-detectie en IgM-detectie van infectie met het humaan cytomegalovirus en bespreking van hun gecombineerde Toepassingswaarde. Chinese Journal of Experimental Diagnostics 2015; (1): 78-80.
- Li x, Cao L, Yu C, et al. Studie naar de infectie van cytomegalovirus bij AIDS-patiënten. Moderne Preventieve Geneeskunde 2012;39:2278-9.
(Editor: J. Gray)