infecția cu citomegalovirus (CMV) la pacienții cu HIV/SIDA și valorile diagnostice ale detectării CMV-ADN pe diferite tipuri de probe
- Introducere
- metode
- subiecți
- includere și excludere
- reactivi și echipamente
- cuantificarea ARN HIV
- numărarea limfocitelor CD4+ T
- cuantificarea ADN-CMV
- testul anticorpilor CMV
- metode de studiu
- detectarea acidului Nucleic
- detectarea subgrupurilor de limfocite T
- detectarea anticorpilor imuni
- analiza statistică
- rezultate
- date generale
- rate pozitive ale ADN-ului CMV, CMV-IgG și CMV-IgM
- corelația dintre infecția cu CMV șicd4+ numărul de limfocite T
- detectarea ADN-ului CMV în diferite probe
- discuție
- concluzii
- mulțumiri
- notă de subsol
Introducere
citomegalovirusul (CMV) este un herpesvirus comun care este răspândit în rândul populațiilor umane. Infecția cu CMV nu provoacă de obicei simptome și afectează în principal glandele salivare, rinichii și alte organe. Cu toate acestea, replicarea virală poate apărea la pacienții imunocompromiși și poate contribui la deteriorarea organelor și a funcțiilor acestora. Infecțiile oportuniste sunt mai frecvente și mai severe la pacienții cu HIV/SIDA. Infecția cu virusul CMV este frecventă la acești pacienți și poate afecta mai multe organe/sisteme, inclusiv ochii, plămânii, sistemul nervos și sistemul digestiv. Multe studii au explorat caracteristicile virologice și imunologice ale infecției simple cu CMV (1), în special cele găsite la femei și copii. Cu toate acestea, caracteristicile imunologice ale infecției cu CMV sunt destul de unice la pacienții cu HIV/SIDA deja imunocompromiși. Există diferențe în ceea ce privește caracteristicile clinice, măsurile de tratament, factorii de prognostic între pacienții HIV cu infecție cu CMV și cei cu infecție cu CMV în monoterapie (2). Ghidul Chinei a recomandat ca terapia antivirală imediată a CMV și ART să fie necesară la acei pacienți cu HIV/SIDA cu complicații (retinită, pneumonie, encefalită CMV, enterită etc.) când este identificată infecția cu CMV. Din cauza nespecificității simptomelor clinice cauzate de infecția cu CMV, examenul de laborator este baza principală pentru diagnosticarea infecției cu CMV. Cele mai utilizate două metode clinice pe scară largă sunt replicarea virusului CMV și metodele imunologice serice, inclusiv detectarea IgG CMV, IgM CMV și antigen CMV PP65 (2) la pacienții cu funcție imună afectată, producția de anticorpi CMV este slăbită sau întârziată, ceea ce poate duce la fals negativ și poate crește rata de diagnosticare ratată, prin urmare, detectarea PCR a ADN-ului CMV a devenit în mare măsură metoda standard pentru diagnosticarea infecției CMV și monitorizarea tratamentului (3). Daisuke Mizushima și colab. a raportat că PCR plasmatic CMV-ADN are o valoare importantă în diagnosticul atât pentru retinita CMV, cât și pentru toate CMV-EOD la pacienții cu infecție avansată cu HIV-1 (4). CMV-ADN PCR poate fi detectat într-o varietate de tipuri de probe, cum ar fi plasmă, urină, lichid cefalorahidian, umor apos, fecale etc. (5). Cu toate acestea, puține articole au analizat și discutat semnificația și valoarea detectării PCR CMV-ADN în alte probe decât plasma. În studiul de față am analizat retrospectiv testele de laborator (incluzând ADN-ul CMV, anticorpul CMV, numărul limfocitelor T CD4+, încărcătura virală HIV etc.) la 808 pacienți cu HIV / SIDA care au fost tratați în centrul nostru din 2017 până în 2019 pentru a înțelege coinfecția CMV și punctele forte și punctele slabe ale mai multor metode de detectare. Prezentăm următorul articol / caz în conformitate cu lista de verificare a raportării MDAR (disponibilă la http://dx.doi.org/10.21037/apm-20-1352).
metode
subiecți
un total de 808 pacienți HIV/SIDA internați în centrul nostru în perioada ianuarie 2017-octombrie 2019 au fost înrolați. La fiecare pacient s-au măsurat ARN HIV, numărul limfocitelor T CD4+, ADN-ul CMV și anticorpii înrudiți. Diagnosticul infecției cu HIV s-a bazat pe ghidul de diagnostic și tratament HIV/SIDA (ediția a treia) (6) și toți pacienții au fost confirmați ca fiind infectați cu HIV de către centrele municipale Fuzhou pentru Controlul Bolilor (CDC) sau CDC local care a tratat pacientul. Diagnosticul infecției cu CMV s-a bazat pe următoarele criterii: (I) CMV-ADN pozitiv în plasmă, lichid de lavaj alveolar, urină, lichid cefalorahidian (LCR) și/sau alte fluide corporale; (II) ser CMV-imunoglobulină M (IgM) pozitivă; (III) un diagnostic oftalmologic al retinitei CMV; (IV) pneumonia CMV se manifestă în principal ca febră, tuse, flegmă și senzație de constricție toracică; CMV-ADN pozitiv în lichidul de lavaj alveolar; (V) enterita CMV sau esofagita se manifestă în principal ca disfagie/durere de înghițire, diaree sau durere abdominală și tratament anti-CMV diagnostic eficient; (VI) encefalita CMV se manifestă ca simptome ale sistemului nervos și CMV-ADN pozitiv în LCR sau țesutul cerebral; (VII) hepatita CMV se manifestă ca febră, funcție hepatică anormală și disconfort în zona ficatului și CMV-ADN pozitiv în biopsia hepatică. S-a pus diagnosticul de infecție cu CMV dacă a fost îndeplinit oricare dintre criteriile de mai sus, cu excepția punctului (II) sau dacă punctul (II) plus orice alt criteriu a fost îndeplinit (7).
toate procedurile efectuate în acest studiu care au implicat participanți umani au fost în conformitate cu declarația de la Helsinki (revizuită în 2013). Studiul a fost aprobat de Comitetul de etică medicală al centrului nostru (aprobarea nr. KS2019-070-01). Datele sunt anonime și, prin urmare, s-a renunțat la cerința consimțământului informat.
includere și excludere
criterii de includere: pacienții cu HIV / SIDA care au vizitat pentru prima dată Spitalul hepatobiliar Mengchao al Universității Medicale Fujian și au finalizat detectarea ARN HIV, ADN CMV, anticorp CMV-IgG, anticorp CMV-IgM și limfocite T CD4+ în decurs de 14 zile. Excludeți cazurile de HIV / SIDA care nu pot finaliza elementele de testare de mai sus din cauza dimensiunii insuficiente a eșantionului.
reactivi și echipamente
cuantificarea ARN HIV
reacția în lanț a polimerazei fluorescente cantitative în timp real (PCR) (FQ-PCR) a fost efectuată pe sistemul QPCR Mx3000p (Agilent, SUA) prin utilizarea kitului de cuantificare a ARN HIV produs de QiaGen (Shenzhen, China).
numărarea limfocitelor CD4+ T
instrumentul utilizat a fost Citometrul de flux FACSCalibur (bd Biosciences, SUA), iar kitul de reactiv utilizat a fost bd MULTITEST CD3/CD4/CD8/CD45 (bd Biosciences, SUA).
cuantificarea ADN-CMV
FQ-PCR a fost efectuată pe sistemul QPCR Mx3000p (Agilent, SUA) pentru a detecta nivelurile de ADN-CMV în plasmă, urină și LCR. Kitul folosit a fost produs de Sansure Biotech (Hunan, China).
testul anticorpilor CMV
imunotestul Chemiluminescenței a fost efectuat pentru a detecta anticorpii anti-CMV-IgG și IgM pe analizorul Cobas e601 (Roche Diagnostics, Germania) cu kiturile de susținere (Roche Diagnostics, Germania).
metode de studiu
detectarea acidului Nucleic
după ce pacienții cu HIV/SIDA au fost internați în spitalul nostru, s-au recoltat 3 mL de probă de sânge integral anticoagulant cu acid etilendiaminotetraacetic (EDTA) în condiții de repaus alimentar și apoi s-au centrifugat la 3000 r/min Timp de 5 minute pentru a recolta 200 ilqq de plasmă pentru detectarea ARN HIV și ADN CMV. La toți pacienții, s-au colectat 5 mL de probă de urină dimineața și s-au amestecat bine, iar apoi s-au recoltat 200 de centicli pentru detectarea ADN-ului CMV. Pentru pacienții cu simptome neurologice, s-a obținut 1 mL de LCR pentru detectarea ADN-ului CMV. Conform limitei de detecție și a standardului de judecată pozitivă a kitului CMV-ADN și a kitului HIV-ARN. Probele au fost considerate pozitive dacă valoarea ADN-CMV a fost peste 400 copii/mL sau dacă nivelul ARN HIV a fost peste 500 copii/mL.
detectarea subgrupurilor de limfocite T
la pacienții cu HIV/SIDA, la internare s-au colectat 3 mL de probă de sânge integral anticoagulant EDTA în condiții de repaus alimentar și apoi s-au amestecat bine pentru detectarea subgrupurilor de limfocite T pe un Citometru de flux bd FACSCalibur utilizând reactivii auxiliari.
detectarea anticorpilor imuni
la pacienții cu HIV/SIDA, 3 mL de probă de sânge de repaus alimentar au fost colectate la admitere, centrifugate la 3.000 r/min Timp de 5 minute într-un tub seric cu separator de gel și apoi testate pe mașină.
toate încercările de mai sus au fost efectuate strict în conformitate cu instrucțiunile reactivului din manualul producătorului și cu procedurile standard de operare ale instrumentelor.
analiza statistică
analiza statistică a fost efectuată utilizând software-ul SPSS 21.0. Datele de măsurare distribuite în mod normal sunt prezentate utilizând deviația standard medie de la ora X la ora X la ora X, iar datele distribuite în mod normal sunt exprimate ca mediane ( 25-75 percentile). Datele de numărare sunt exprimate în procente și rate. Comparația datelor de măsurare non-distribuite în mod normal între două grupuri a fost efectuată utilizând un test de sumă de rang neparametric, în timp ce datele de numărare au fost comparate folosind testul Chi-pătrat. O valoare P <0,05 a fost considerată semnificativă statistic.
rezultate
date generale
datele generale ale 808 pacienți cu HIV/SIDA sunt rezumate în tabelul 1. Sexul și vârsta nu au arătat nicio diferență semnificativă între grupul CMV și grupul non-CMV. Numărul absolut de CD4 în grupul infectat cu CMV a fost semnificativ mai mic decât cel din grupul neinfectat cu CMV (Z=-8,87, P<0,001), iar nivelul ARN HIV a fost semnificativ mai mare în grupul infectat cu CMV decât în grupul neinfectat cu CMV (Z=-3,207, P<0,05) (Tabelul 1).
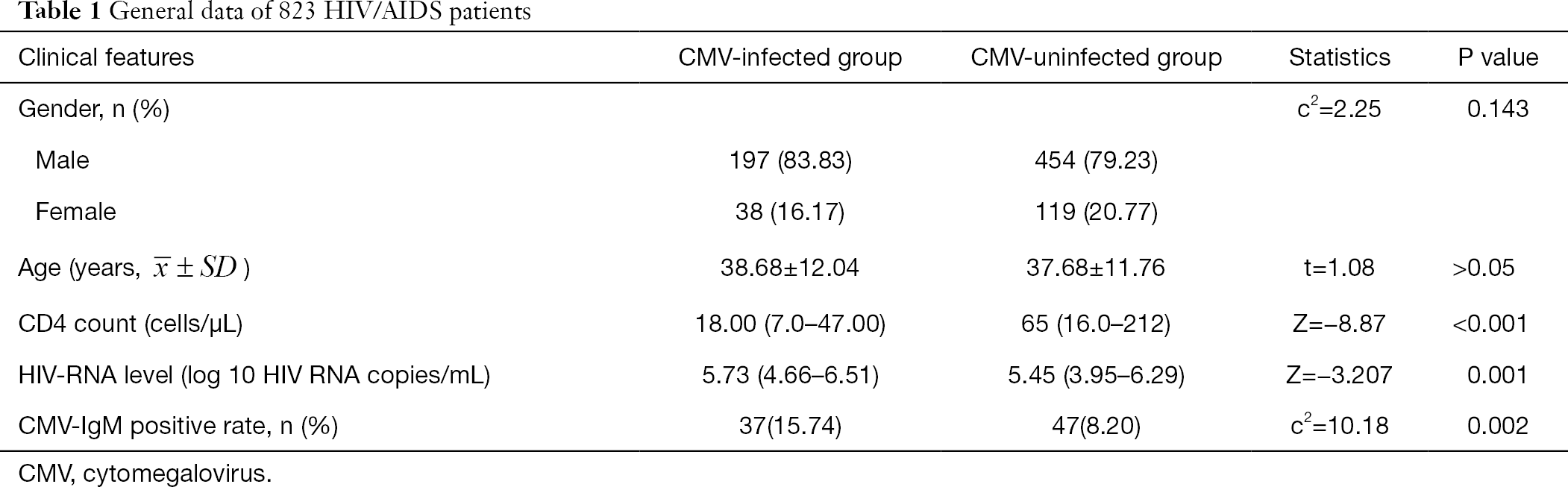
Tabelul complet
rate pozitive ale ADN-ului CMV, CMV-IgG și CMV-IgM
rata generală pozitivă a ADN-ului CMV a fost de 29,08% (235/808); mai exact, a fost de 5,70% (13/228) în LCR 26,01% (77/296) în plasmă și 25,75% (180/699) în urină. Rata pozitivă a CMV-IgG a fost de 99,8% (806/808), iar rata pozitivă a CMV-IgM a fost de 10,40% (84/808).
corelația dintre infecția cu CMV șicd4+ numărul de limfocite T
după gruparea numărului de limfocite T CD4+, am constatat că proporția pacienților infectați cu citomegalovirus la Frecvență scăzută a limfocitelor T CD4+ a fost mai mare decât cea a pacienților care nu au fost infectați cu CMV. Incidența infecției cu CMV a crescut odată cu scăderea numărului de CD4 (Tabelul 2).
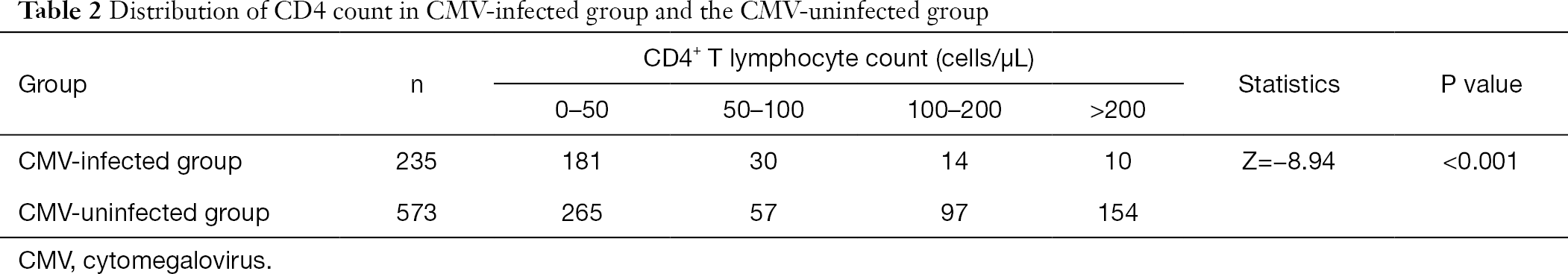
Tabelul complet
detectarea ADN-ului CMV în diferite probe
dintre acești 808 pacienți, 198 de pacienți au primit, de asemenea, teste pentru ADN-ul CMV-anticorpi CMV-IgG și CMV-IgM. Folosind analiza Chi-square pentru date pereche, am efectuat comparații perechi de ADN CMV-urină și ADN CMV-plasmă cu anticorp CMV-IgM plasmatic, respectiv. S-a constatat că rezultatele detectării ADN-ului CMV în urină și plasmă diferă semnificativ de cele ale testului anticorpilor CMV-IgG în plasmă (P<0,001), în timp ce rezultatul detectării ADN-ului CMV în plasmă nu a fost semnificativ diferit de cel al detectării ADN-ului CMV în urină (P>0,05) (tabelele 3,4).

Tabelul complet
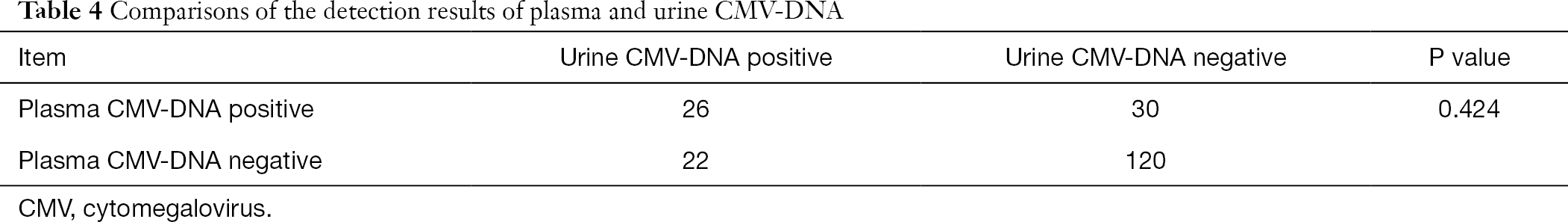
Tabelul complet
discuție
CMV este un membru al grupului de virusuri herpetice din grupul de virusuri herpetice și se caracterizează prin specificitatea strictă a speciilor și incidența pe scară largă la populațiile umane. Seroprevalența CMV este de aproximativ 85% la copii și până la 95% la adulți. În studiul nostru actual, rata pozitivă a CMV-IgG a ajuns la 99,8%. CMV este latent în majoritatea cazurilor, dar la persoanele imunocompromise, virusul se reproduce exponențial și se răspândește în tot corpul cu sângele, provocând viremia CMV și chiar boala CMV organică (8). Infecția cu CMV este una dintre infecțiile oportuniste comune la pacienții cu HIV/SIDA. Limfocitele T CD4 + sunt celulele țintă ale virusului HIV, iar numărul lor poate reflecta adesea evoluția SIDA și poate fi, de asemenea, utilizat ca indicator pentru evaluarea stării imune a pacienților cu SIDA. Acest studiu a analizat infecția CMV, numărul CD4 și nivelul ARN HIV la 808 pacienți cu HIV/SIDA. Am constatat că rata pozitivă a CMV la pacienții cu SIDA a crescut odată cu scăderea numărului de CD4 și cu creșterea încărcăturii virale HIV. De asemenea, în studiul nostru actual, până la 77,02% dintre pacienții cu CMV pozitiv au avut un număr de CD4 de <50 celule/ilftl, sugerând că CD4 <50 celule/ilftl este un factor de risc pentru coinfecția HIV-CMV, ceea ce este în concordanță cu constatarea lui Deng și colab. (9). Nivelul cantitativ al ARN HIV în grupul infectat cu CMV a fost mai mare decât cel din grupul neinfectat cu CMV, ceea ce a sugerat indirect că nivelurile ridicate ale încărcăturii virale cu ARN HIV au fost un alt factor de risc al infecției cu CMV la pacienții cu HIV/SIDA .Prin urmare, se recomandă ca pacienții cu HIV/SIDA să inițieze tratamentul ART cât mai curând posibil pentru a promova reconstituirea imună pentru a preveni infecțiile oportuniste, iar screeningul pentru HCMV este esențial pentru pacienții cu HIV/SIDA cu un număr de CD4 de <50 celule/unktil (2).
am evaluat, de asemenea, valorile testelor de acid nucleic viral și metodele imunologice în detectarea clinică a infecției cu CMV. Studiile efectuate în China și la nivel internațional au arătat că ADN-ul CMV apare mai devreme decât simptomele clinice și reacțiile serologice ale infecțiilor cu CMV. FQ-PCR este în prezent cea mai precisă și rapidă metodă de cuantificare microbiană și este capabilă să depășească unele probleme ale PCR tradiționale (de exemplu, contaminarea produsului de amplificare și necantificarea) (10). În studiul nostru actual, rata pozitivă a ADN-ului CMV a fost de 5.70% (13/228) în probele LCR de 228 de pacienți cu simptome neurologice, care a fost mult mai mică decât cea din probele de plasmă și urină, care ar putea fi explicată prin bariera hematoencefalică și sensibilitatea organelor. Anticorpul anti-CMV-IgM este adesea utilizat ca marker al infecției virale active; cu toate acestea, rata pozitivă a anticorpului anti-CMV-IgM a fost de numai 10,40% (84/808) la pacienții noștri cu HIV/SIDA, care a fost mai mică decât rata pozitivă a infecției CMV raportată la populațiile non-HIV/SIDA (11). În plus, rata sa pozitivă a avut un acord slab cu rezultatele detectării acidului nucleic, care s-ar putea datora sistemului imunitar slăbit sau datorită generării întârziate de anticorpi IgM la pacienții cu HIV/SIDA. Prin urmare, detectarea anticorpilor CMV-IgM are un rol limitat în screeningul HCMV la pacienții cu HIV/SIDA. Mai mult, rata pozitivă a infecției cu CMV la 808 pacienți a fost de 29,05% (235/808) în studiul nostru actual, care este puțin mai mare decât 21,85% raportat de Li și colab., și se poate datora varietății mai mari de probe (inclusiv plasmă, urină și LCR) colectate în acest studiu (12). Rata pozitivă a ADN-ului CMV a fost de 25,57% în urină și 26,01% în plasmă, diferența nu a fost semnificativă statistic. Prin urmare, recomandăm ca screeningul ADN-CMV în plasmă și urină să fie efectuat atunci când numărul limfocitelor T CD4+ este mai mic de 200 celule/ilft, în special atunci când <50 celule/ilft; în plus, detectarea ADN-CMV în LCR este necesară dacă sunt prezente simptome neurologice evidente.
concluzii
în concluzie, numărul scăzut de limfocite T CD4+ și încărcătura virală HIV-1 ridicată sunt factori de risc pentru infecția cu CMV la pacienții cu HIV/SIDA. Detectarea ADN-ului CMV în urină sau plasmă prin FQ-PCR este extrem de valoroasă în screeningul infecției CMV la pacienții cu HIV/SIDA, în timp ce detectarea nivelurilor de IgG CMV și IgM CMV din sânge are o valoare clinică limitată. Screeningul CMV-ADN din sânge sau urină este recomandat pacienților cu SIDA pentru a preveni și diagnostica infecția CMV devreme și pentru a le îmbunătăți calitatea vieții.
mulțumiri
finanțare: sponsorizat de Programul cheie de construcție a disciplinei clinice de specialitate din Fujian, P. R. C.
notă de subsol
Lista de verificare a raportării: autorii au completat lista de verificare a raportării MDAR. Disponibil la http://dx.doi.org/10.21037/apm-20-1352
Declarație privind schimbul de date: disponibil la http://dx.doi.org/10.21037/apm-20-1352
conflicte de interese: toți autorii au completat formularul de divulgare uniformă ICMJE (disponibil la http://dx.doi.org/10.21037/apm-20-1352). Autorii nu au conflicte de interese de declarat.
declarație etică: autorii sunt responsabili pentru toate aspectele lucrării, asigurându-se că întrebările legate de acuratețea sau integritatea oricărei părți a lucrării sunt investigate și rezolvate în mod corespunzător. Toate procedurile efectuate în acest studiu care au implicat participanți umani au fost în conformitate cu declarația de la Helsinki (revizuită în 2013). Studiul a fost aprobat de Comitetul de etică medicală al centrului nostru (aprobarea nr. KS2019-070-01). Datele sunt anonime și, prin urmare, s-a renunțat la cerința consimțământului informat.
declarație de acces deschis: acesta este un articol cu acces deschis distribuit în conformitate cu licența internațională Creative Commons Attribution-NonCommercial-NoDerivs 4.0 (CC BY-NC-ND 4.0), care permite replicarea și distribuirea necomercială a articolului cu condiția strictă că nu se fac modificări sau modificări și că lucrarea originală este citată în mod corespunzător (inclusiv link-uri către publicația formală prin intermediul DOI relevant și al licenței). A se vedea: https://creativecommons.org/licenses/by-nc-nd/4.0/.
- Yu X, Tong M, He G. efectele infecției cu citomegalovirus asupra celulelor imune de reglementare la femeile gravide din China. Jurnalul de Nosocomiologie. 2017;27:2103-6.
- proiectul național Major de știință și tehnologie ajută grupul de cercetare a infecțiilor oportuniste în timpul celui de-al 13-lea Plan cincinal. Consensul experților privind diagnosticul clinic și tratamentul SIDA complicat cu boala citomegalovirusului . Jurnalul Universității Southwest (ediția științelor naturale): 1-17 .
- Hodowanec AC, Pikis A, Komatsu TE și colab. Tratamentul și prevenirea bolii CMV la beneficiarii de Transplant: cunoștințe actuale și perspective viitoare. J Clin Pharmacol 2019; 59: 784-98.
- Mizushima D, Nishijima T, Yashiro S și colab. Utilitatea diagnostică a ADN-ului citomegalovirusului plasmatic cantitativ PCR pentru bolile organelor finale ale citomegalovirusului la pacienții cu infecție cu HIV-1. J Acquir Immune Defic Syndr 2015; 68:140-6.
- Michaelides a, Liolios L, Glare EM și colab. Creșterea încărcării ADN a citomegalovirusului uman (HCMV) în leucocitele din sângele periferic după transplantul pulmonar se corelează cu pneumonita HCMV. Transplant 2001; 72: 141-7.
- infecția de Neurologie, SIDA grup de Asociația Medicală Chineză. Ghid de diagnostic și tratament HIV/SIDA (ediția a treia). Jurnalul chinez de Boli Infecțioase 2015; (10):577-93.
- Corrales I, Gimcinccnez E, Solano C, și colab. Incidența și dinamica infecției active cu citomegalovirus la pacienții cu transplant de celule stem alogene în funcție de polimorfismele nucleotidice unice la genele CCR5, MCP-1, IL-10 și tlr9 ale donatorului și primitorului. J Med Virol 2015; 87:248-55.
- Tagarro A, Del Valle R, Dominguez-Rodr si colab. Modele de creștere la copiii cu infecție congenitală cu citomegalovirus. Pediatr Infect Dis J 2019; 38:1230-5.
- Deng X, Liu J, Zhang M, și colab. Analiza caracteristicilor virologice și imunologice ale HIV / SIDA combinate cu infecția cu citomegalovirus. Jurnalul chinez al infecției spitalicești 2019; 29:2241-6.
- Kawano Y, Kawada J, Kamya Y și colab. Analiza pacienților cu păcat microARN uman și viral circulant cu infecție congenitală cu citomegalovirus. J Perinatol 2016; 36: 1101-5.
- Li L, Gao s, Zhang T, și colab. Compararea detectării ADN și detectarea IgM a infecției cu citomegalovirus uman și discutarea valorii lor combinate de aplicare. Jurnalul chinez de diagnosticare experimentală 2015; (1): 78-80.
- Li x, cao L, Yu C, și colab. Studiu privind infecția cu citomegalovirus la pacienții cu SIDA. Medicină Preventivă Modernă 2012;39:2278-9.
(Editor în limba engleză: J. Gray)