25.6: Coenzym B12- Vitamin B12
Cobalamin oder Vitamin B12 ist das größte und komplexeste aller Arten von Vitaminen. Die Entdeckung von Cobalamin wurde gemacht, als Wissenschaftler nach einem Heilmittel für perniziöse Anämie suchten, eine anämische Krankheit, die durch das Fehlen eines intrinsischen Faktors im Magen verursacht wird. Cobalamin wurde untersucht, gereinigt und in kleine rote Kristalle gesammelt, und seine Kristallisationsstruktur wurde während eines Röntgenanalyseexperiments bestimmt, das vom Wissenschaftler Hodkin durchgeführt wurde. Eine Molekülstruktur von Cobalamin ist einfach, enthält jedoch viele verschiedene Sorten und Komplexe, wie in Abbildung 1 gezeigt. Die Untersuchung der molekularen Struktur des Vitamins hilft Wissenschaftlern, besser zu verstehen, wie der Körper Vitamin B12 zum Aufbau roter Blutkörperchen und zur Vorbeugung von perniziösen Anämiesyndromen verwendet.
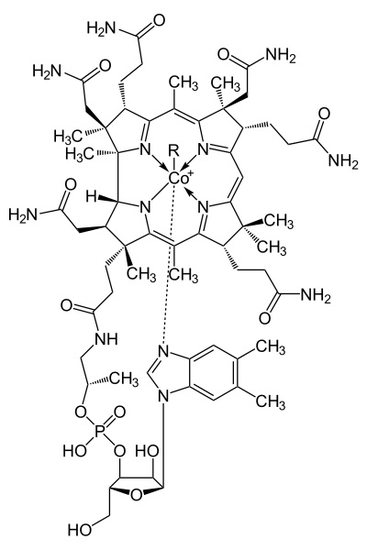
Abbildung 1
Die Metalloenzymstruktur von Cobalamin zeigt einen Corrinring mit Kobalt, dem einzigen Metall im Molekül, das durch vier koordinierte Stickstoffbindungen aus vier Pyrrolgruppen direkt in der Mitte der Struktur positioniert ist. Diese vier Untereinheitsgruppen sind gleichmäßig auf derselben Ebene direkt gegenüber voneinander getrennt. Sie sind auch durch eine C-CH 3 -Methylenverbindung auf den anderen Seiten, durch eine C-H auf einer Seite und durch zwei direkt zusammenkommende Pyrrole miteinander verbunden. Zusammen bilden sie einen perfekten Corrin-Ring, wie in Abbildung 2 gezeigt. Der fünfte Ligand, der mit Kobalt verbunden ist, ist ein Stickstoff, der aus dem 5,6-Dimethyl-Benzimidazol stammt. Es präsentiert sich als eine axial verlaufende gerade nach unten aus dem Kobalt direkt unter dem Corrin-Ring. Dieses Benzimidazol ist auch mit einem Zucker mit fünf Kohlenstoffatomen verbunden, der sich schließlich an eine Phosphatgruppe bindet und dann zum Rest der Struktur zurückkehrt. Da das Kobalt ganz nach unten gestreckt ist, ist die Bindung zwischen dem Kobalt und dem 5,6-Dimethylbenzimidazol schwach und kann manchmal durch verwandte Moleküle wie ein 5-Hydrozyl-Benzimidazol, ein Adenin oder eine andere ähnliche Gruppe ersetzt werden. In der sechsten Position über dem Corrin-Ring kann sich das aktive Zentrum von Kobalt direkt mit mehreren verschiedenen Arten von Liganden verbinden. Es kann sich mit CN verbinden, um ein Cyanocobalamin zu bilden, mit einer Methylgruppe, um ein Methylcobalamin zu bilden, mit einer 5′-Desoxy-Adenosygruppe, um ein Adenosylcobalamin zu bilden, und OH, Hydroxycobalamin. Kobalt ist immer bereit, von 1 + zu 2+ und 3+ zu oxidieren, um mit diesen damit verbundenen R-Gruppen übereinzustimmen. Zum Beispiel enthält Hydroxocobalamin Kobalt mit einer Ladung von 3+, während Methyladenosyl ein Kobalt mit einer Ladung von 1 + enthält.
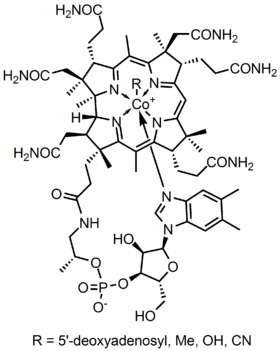
Abbildung 2
Die Punktgruppenkonfiguration von Cobalamin ist C4v. Um diese Symmetrie zu bestimmen, muss man sehen, dass sich die Struktur viermal drehen kann und schließlich in ihre ursprüngliche Position zurückkehrt. Darüber hinaus gibt es keine Sigma-h-Ebene und keine senkrechte C2-Ebene. Da es jedoch Sigma-v-Ebenen gibt, die die Moleküle in gleichmäßige Teile schneiden, ist es klar zu bestimmen, dass die Struktur von Cobalamin ein C Ist4v. Da Kobalt das Mittelmetall des Moleküls ist, trug Cobalamin eine verzerrte oktaedrische Konfiguration. Die Verbindung, die Kobalt mit dem 5,6-Dimethylbenzimidazol verbindet, ist bis zum Boden gespannt. Sein Abstand ist um ein Vielfaches länger als der Abstand vom Kobalt und der darüber angebrachten R-Gruppe. Dies kann manchmal auch als tetragonale Struktur bezeichnet werden. Die gesamte Form ähnelt insgesamt einem Oktaeder, aber die beiden axialen Gruppen sind unterschiedlich und in ungleiche Abstände voneinander getrennt. Da es im System nur ein Metalloenzymzentrum gibt, wird die eben erwähnte Punktgruppe und Konfiguration auch der gesamten Struktur zugeordnet. Da die Metallocoenzymstruktur ausgedehnt wird, ist sie ziemlich schwach koordiniert und kann auseinander brechen oder durch andere Gruppen ersetzt werden, wie oben erwähnt.
Wissenschaftler haben gezeigt, dass sowohl IR- als auch Raman-Spektroskopie verwendet wurden, um die Struktur des Moleküls zu bestimmen. Dies wird durch Beobachtung der Zeichentabellen der Punktgruppe C4v, der Punktgruppensymmetrie von Cobalamin, bestimmt. Auf der IR-Seite kann man sehen, dass es Gruppen wie drz, (x, y), (rz, ry) gibt. Andererseits gibt es auf der Raman–Seite Gruppen wie x-Quadrat + y-Quadrat, z-Quadrat, x-Quadrat – y-Quadrat, xy, xz, yz. Die Raman-Seite zeigte, dass es Streckmoden im Molekül gab und bezieht sich auf die Streckung der 5,6-Dimethylbenzimidazolschicht, die direkt unterhalb des Kobaltmetalls verbunden war. Die Dehnung ist in Abbildung 3 zu sehen.
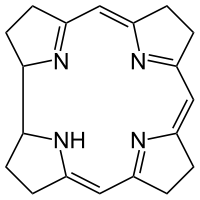
Abbildung 3
Cobalamin-Enzyme können verschiedene Arten von Reaktionen katalysieren. Eine davon ist die Reaktion intramolekularer Umlagerungen. Während dieser Umlagerung wird Coenzym gegen die beiden Gruppen ausgetauscht, die an benachbarte Kohlenstoffatome gebunden sind. Eine andere Reaktion beinhaltet die Übertragung der Methylgruppe in bestimmten Methylierungsreaktionen, wie die Umwandlung von Homocystein in Methionin, Biosysnthese von Cholin und Thymin usw. Diese Wechselwirkungen können den biologischen Körpern vorteilhafte Werte bringen.
Cobalamin hat viele positive Wirkungen in Bezug auf biologische Existenzen. Sie spielen eine Rolle bei der Aufrechterhaltung eines gesunden Körpersystems und helfen bei der Produktion des genetischen Materials des Körpers. Cyanocobalamin, eine Art von Cobalamin, arbeitet, um die Bildung von roten Blutkörperchen zu erzeugen und viele verschiedene Schäden im Nervensystem zu heilen. Cobalamin spielt auch eine wichtige Rolle im Stoffwechsel von Fettsäuren, die für die Aufrechterhaltung von Myelin essentiell sind. Studien haben gezeigt, dass Menschen mit Vitamin-B12-Mangel unregelmäßige Zerstörung der Myelinengesundheit aufdecken, was zu Elektrolyse und Tod führt. Einige der anderen Symptome des Mangels an Cobalamin sind schlechtes Wachstum, megaloblastisches Knochenmark, Veränderungen des Gastrointestinaltrakts, Leukoopenie und hypersegmentierte Nutrophills, degenerative Veränderungen des Rückenmarks und des Nervensystems sowie die Ausscheidung von Methylmalonsäure und Homocystin im Urin.
Im Laufe der Jahre hat sich gezeigt, dass Vitamin B12 für die Funktion des Nervensystems und die Produktion roter Blutkörperchen essentiell ist. Eine Studie, die von Forschern der National Institutes of Health am Trinity College Dublin durchgeführt wurde, ergab, dass ein Mangel an Vitamin B12 das Risiko eines Neuralrohrdefekts bei Kindern erhöhen könnte (Miller). Durch die Untersuchung der Struktur und Funktion von Cobalamin können Wissenschaftler daher experimentieren und Vitamin B12 in ihren Labors bilden und der Gemeinschaft als Ganzes dienen.