3.3 Conformación de Ciclohexano
Conformaciones de Ciclohexano
Una estructura plana para el ciclohexano es claramente improbable. Los ángulos de unión serían necesariamente 120º, 10,5 º más grandes que el ángulo tetraédrico ideal. Además, cada enlace carbono-carbono en tal estructura sería eclipsado. El ángulo resultante y las tensiones eclipsantes desestabilizarían severamente esta estructura. Si se levantan dos átomos de carbono en lados opuestos del anillo de seis miembros del plano del anillo, se puede eliminar gran parte de la deformación angular.
Esta estructura de barco todavía tiene dos enlaces eclipsados y un apiñamiento estérico severo de dos átomos de hidrógeno en la “proa” y la “popa” del barco. Este apiñamiento estérico a menudo se denomina obstáculo estérico. Al torcer la conformación del barco, el obstáculo estérico se puede aliviar parcialmente, pero el conformador del barco giratorio aún conserva algunas de las tensiones que caracterizan al conformador del barco. Finalmente, al levantar un carbono por encima del plano anular y el otro por debajo del plano, se forma un conformador de silla relativamente libre de tensiones. Esta es la estructura predominante adoptada por las moléculas de ciclohexano.
las Investigaciones relativas a las conformaciones del ciclohexano fueron iniciados por H. Sachse (1890) y E. Mohr (1918), pero no fue hasta 1950 que un tratamiento completo de las múltiples consecuencias de interconvertir presidente confórmeros y las diferentes orientaciones de pendiente de los bonos fue aclarada por D. H. R. Barton (Premio Nobel en 1969 junto con O. Hassel). La siguiente discusión presenta algunas de las características esenciales de este análisis conformacional.
Al examinar cuidadosamente una conformación de silla de ciclohexano, encontramos que los doce hidrógenos no son estructuralmente equivalentes. Seis de ellos se encuentran alrededor de la periferia del anillo de carbono, y se denominan ecuatoriales. Los otros seis están orientados por encima y por debajo del plano aproximado del anillo (tres en cada ubicación), y se denominan axiales porque están alineados paralelos al eje de simetría del anillo.
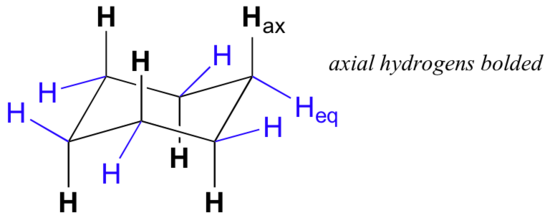
En la figura de arriba, los hidrógenos ecuatoriales son de color azul, y los hidrógenos axiales están en negrita. Dado que hay dos conformaciones de silla equivalentes de ciclohexano en equilibrio rápido, los doce hidrógenos tienen un 50% de carácter ecuatorial y un 50% de carácter axial. La siguiente figura ilustra cómo convertir un modelo molecular de ciclohexano entre dos conformaciones de sillas diferentes; esto es algo que debe practicar con modelos. Observe que un ‘giro de anillo’ hace que los hidrógenos ecuatoriales se vuelvan axiales, y viceversa.
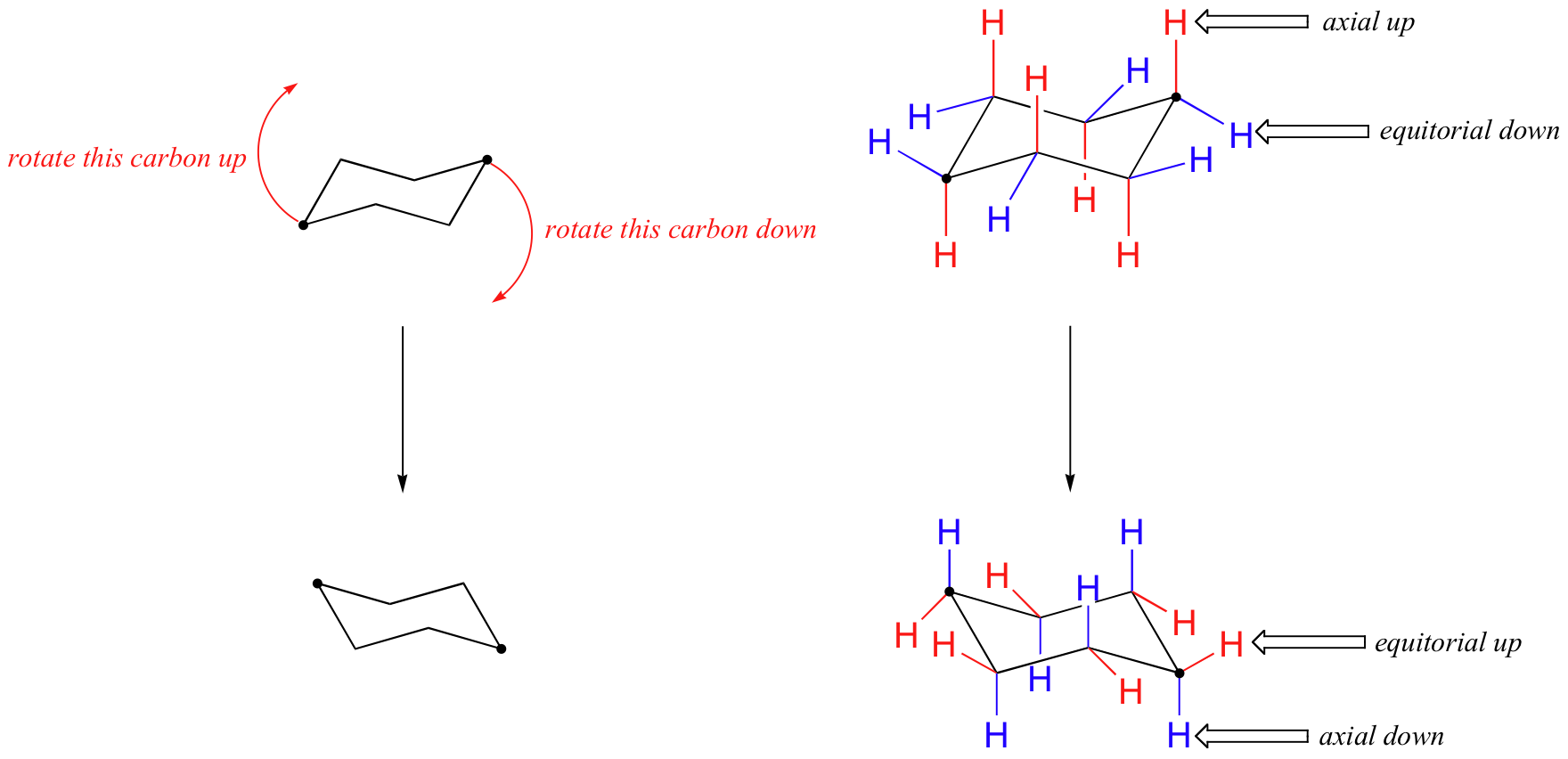
Debido a que los enlaces axiales son paralelos entre sí, los sustituyentes más grandes que el hidrógeno generalmente sufren un mayor apiñamiento estérico cuando están orientados axiales en lugar de ecuatoriales. En consecuencia, los ciclohexanos sustituidos adoptarán preferentemente conformaciones en las que los sustituyentes más grandes asumen orientación ecuatorial.
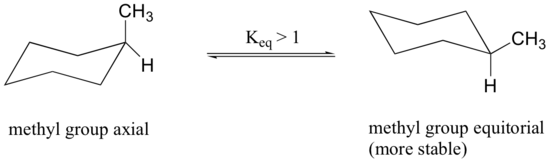
Cuando el grupo metilo en la estructura anterior ocupa una posición axial, sufre apiñamiento estérico por los dos hidrógenos axiales ubicados en el mismo lado del anillo.

La conformación en la que el grupo metilo es ecuatorial es más estable, y por lo tanto el equilibrio se encuentra en esta dirección.
El obstáculo estérico relativo experimentado por diferentes grupos sustituyentes orientados en una ubicación axial versus ecuatorial en ciclohexano puede determinarse por el equilibrio conformacional del compuesto. La constante de equilibrio correspondiente está relacionada con la diferencia de energía entre los conformadores, y la recopilación de tales datos nos permite evaluar la tendencia relativa de los sustituyentes a existir en una ubicación ecuatorial o axial.Se puede examinar una tabla de estos valores de energía libre (a veces denominados valores A) haciendo clic aquí.
Mirando los valores de energía en esta tabla, está claro que el “tamaño” aparente de un sustituyente (en términos de su preferencia por la orientación ecuatorial sobre la axial) está influenciado por su ancho y longitud de enlace al ciclohexano, como lo demuestra el hecho de que un grupo vinílico axial está menos obstaculizado que el etilo y el yodo ligeramente menos que el cloro.
Hemos señalado anteriormente que los cicloalcanos que tienen dos o más sustituyentes en átomos de carbono de anillos diferentes existen como un par (a veces más) de estereoisómeros configuracionales. Ahora debemos examinar la forma en que las conformaciones de anillos favorables influyen en las propiedades de los isómeros configuracionales. Recuerde, estereoisómeros configuracionales son estables y no fácilmente interconvierten, mientras que los isómeros conformacionales que normalmente se interconvierten rápidamente. Al examinar las posibles estructuras para los ciclohexanos sustituidos, es útil seguir dos principios:
(i) Las conformaciones de sillas son generalmente más estables que otras posibilidades.
(ii) Los sustituyentes de los conformadores de sillas prefieren ocupar posiciones ecuatoriales debido al mayor obstáculo estérico de las ubicaciones axiales.
Las siguientes ecuaciones y fórmulas ilustran cómo la presencia de dos o más sustituyentes en un anillo de ciclohexano perturba la interconversión de los dos conformadores de silla de maneras que se pueden predecir.
En el caso de los ciclohexanos 1,1-disustituidos, uno de los sustituyentes debe ser necesariamente axial y el otro ecuatorial, independientemente del conformador de silla que se considere. Dado que los sustituyentes son los mismos en el 1,1-dimetilciclohexano, los dos conformadores son idénticos y están presentes en igual concentración. En el 1-t-butil-1-metilciclohexano, el grupo t-butilo es mucho más grande que el metilo, y el conformador de silla en el que el grupo más grande es ecuatorial se verá favorecido en el equilibrio( > 99%). En consecuencia, el grupo metilo en este compuesto es casi exclusivamente axial en su orientación.
En los casos de compuestos disustituidos de 1,2, 1,3 y 1,4, el análisis es un poco más complejo. Siempre es posible tener ambos grupos ecuatoriales, pero si esto requiere una relación cis o una relación trans depende de la ubicación relativa de los sustituyentes. A medida que contamos alrededor del anillo de carbono #1 a #6, el enlace superior de cada carbono cambia su orientación de ecuatorial (o axial) a axial (o ecuatorial) y hacia atrás. Es importante recordar que las uniones en un lado dado de una conformación de anillo de silla siempre se alternan de esta manera. Por lo tanto, debe quedar claro que para el cis-1,2-disustitución, uno de los sustituyentes deben ecuatorial y el otro axial; en el isómero trans ambos pueden ser ecuatoriales. Debido a la naturaleza alterna de los enlaces ecuatoriales y axiales, la relación opuesta es cierta para la disubstitución 1,3 (cis es todo ecuatorial, trans es ecuatorial/axial).
Finalmente, 1,4-disustitución vuelve a la 1,2-patrón:
El análisis anterior no es algo que usted debe tratar de memorizar: más bien, siéntase cómodo dibujando ciclohexano en la conformación de la silla, con enlaces apuntando en las direcciones correctas para sustituyentes axiales y ecuatoriales. Si puede dibujar una estructura correctamente en la conformación de la silla, siempre debe poder determinar qué posiciones son axiales y cuáles ecuatoriales.