25.6: koentsyymi B12 – Vitamiini B12
kobalamiini eli B12-vitamiini on kaikista Vitamiinilajeista suurin ja monimutkaisin. Kobalamiinin löytö tehtiin, kun tutkijat etsivät parannuskeinoa pernisiööiseen anemiaan, aneemiseen sairauteen, joka johtuu vatsan sisäisen tekijän puuttumisesta. Kobalamiinia tutkittiin, puhdistettiin ja kerättiin pieniksi punaisiksi kiteiksi, ja sen kiderakenne määritettiin tutkija Hodkinin johtamassa Röntgenanalyysikokeessa. Kobalamiinin molekyylirakenne on yksinkertainen, mutta sisältää kuitenkin paljon erilaisia lajikkeita ja komplekseja kuten kuvassa 1. Vitamiinin molekyylirakenteen tutkiminen auttaa tutkijoita ymmärtämään paremmin, miten elimistö hyödyntää B12-vitamiinia punasolujen rakentamisessa ja pernisiööisten anemiaoireyhtymien ehkäisemisessä.
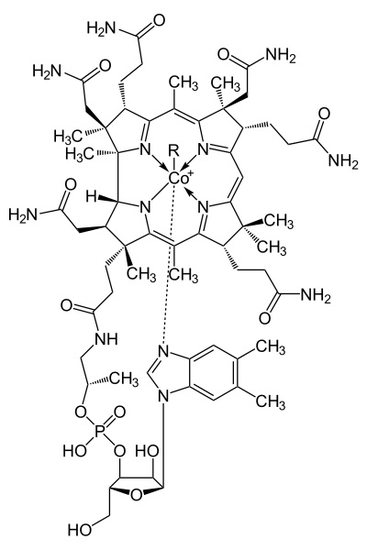
Kuva 1
kobalamiinin metalloentsyymirakenne esittää korriinirenkaan, jossa molekyylin ainoana metallina on koboltti, joka on sijoitettu suoraan rakenteen keskelle neljällä koordinoidulla typpisidoksella neljästä pyrroliryhmästä. Nämä neljä alayksikköä erotetaan tasaisesti samalla tasolla, suoraan vastakkain. Ne ovat myös yhteydessä toisiinsa C-CH3-metyleenisidoksella toisilla sivuilla, C-H: lla toisella puolella ja kahdella suoraan yhteen tulevalla pyrrolilla. Yhdessä ne muodostavat täydellisen korriinirenkaan, kuten kuvassa 2 esitetään. Viides kobolttiin liitetty ligandi on typpi, joka tulee 5,6-dimetyylibentsimidatsolista. Se esiintyy aksiaalina, joka kulkee koboltista suoraan korrin renkaan alle. Tämä bentsimidatsoli on myös yhteydessä viiden hiilen sokeriin, joka lopulta kiinnittyy fosfaattiryhmään ja kiinnittyy sitten takaisin muuhun rakenteeseen. Koska aksiaali on venytetty alas asti, koboltin ja 5,6-dimetyylibentsimidatsolin välinen sidos on heikko ja se voidaan joskus korvata sukulaismolekyyleillä, kuten 5-hydrosyylibentsimidatsolilla, adeniinilla tai muulla vastaavalla ryhmällä. Kuudennessa asemassa Korriinirenkaan yläpuolella koboltin aktiivinen kohta voi liittyä suoraan useisiin erityyppisiin ligandeihin. Se voi liittyä CN: ään muodostaen Syanokobalamin, Metyyliryhmään muodostaen metyylikobalamiinin, 5′-deoksi-adenosy-ryhmään muodostaen adenosyylikobalamiinin ja Oh, Hydroksikobalamiinin. Koboltti on aina valmis hapettumaan 1+ – muutoksesta 2+: ksi ja 3+: ksi vastatakseen näihin siihen kytkeytyviin R-ryhmiin. Esimerkiksi Hydroksokobalamiini sisältää kobolttia, jolla on 3+ varaus, kun taas Metyyliadenosyyli sisältää kobolttia, jolla on 1+ varaus.
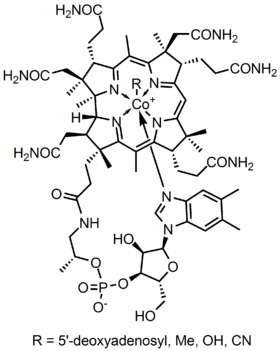
kuva 2
kobalamiinin pisteryhmäkonfiguraatio on c4v. tämän symmetrian määrittämiseksi on nähtävä, että rakenne pystyy kiertämään itseään neljä kertaa ja saapuu lopulta takaisin alkuperäiseen asentoonsa. Lisäksi ei ole sigma h-tasoa eikä kohtisuoraa C2-kirvestä. Koska on kuitenkin olemassa Sigma v-tasoja, jotka leikkaavat molekyylit parillisiin osiin, on selvää, että kobalamiinin rakenne on c4v. kobalamiinin ollessa molekyylin keskusmetalli, Kobalamiinilla oli vääristynyt oktaedrinen konfiguraatio. Aksiaali, joka yhdistää koboltin 5,6-dimetyylibentsimidatsoliin, venyy pohjaan asti. Sen etäisyys on useita kertoja pidempi kuin etäisyys koboltista ja sen yläpuolella olevasta kiinnittyneestä R-ryhmästä. Tätä voidaan joskus kutsua myös tetragonaaliseksi rakenteeksi. Koko muoto kokonaisuudessaan muistuttaa oktaedriä, mutta kaksi aksiaalista ryhmää ovat erilaisia ja ne on erotettu toisistaan epätasaisiin etäisyyksiin. Koska järjestelmässä on vain yksi metalloenzyme-keskus, juuri mainittu pisteryhmä ja konfiguraatio osoitetaan myös koko rakenteelle. Koska metallokoentsyymirakenne venyy, se on melko heikosti koordinoitunut ja se voidaan hajottaa tai korvata muilla edellä mainituilla ryhmillä.
tutkijat ovat osoittaneet, että molekyylin rakenteen selvittämiseen käytettiin sekä IR-että Raman-spektroskopiaa. Tämä määritetään tarkkailemalla pisteryhmän c4v merkistötauluja, kobalamiinin pisteryhmän symmetriaa. IR-puolella voidaan nähdä, että on olemassa ryhmiä, kuten drz, (x, y), (rz, ry). Toisaalta Ramanin puolella on ryhmiä, kuten x square +y square, z square, x square – y square, xy, xz, yz. Ramanin puoli osoitti, että molekyylissä oli venymätiloja ja se liittyy suoraan Kobolttimetallin alapuolelle liittyneen 5,6 dimetyylibentsimidatsolin aksiaalin venymiseen. Venytys näkyy kuvassa 3.
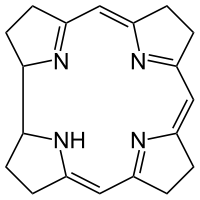
kuva 3
Kobalamiinientsyymit voivat katalysoida muutamia erityyppisiä reaktioita. Yksi niistä on Intramolekulaaristen uudelleenjärjestelyjen reaktio. Tämän uudelleenjärjestelyn aikana koentsyymi vaihtuu kahteen vierekkäisiin hiiliatomeihin kiinnittyneeseen ryhmään. Toisessa reaktiossa metyyliryhmä siirretään tietyissä metylaatioreaktioissa, kuten homokysteiinin muuntumisessa metioniiniksi, koliinin ja tymiinin biosysnteesissä jne. Nämä vuorovaikutukset voivat tuoda hyödyllisiä arvoja biologisille elimille.
Kobalamiinilla on monia biologisten olemassaolojen kannalta suotuisia vaikutuksia. Niillä on rooli ylläpitää tervettä kehon järjestelmä ja auttaa tukemaan tuotantoa kehon geneettisiä materiaaleja. Syanokobalamiini, yksi kobalamiinityyppi, toimii punasolujen muodostuksen aikaansaamiseksi ja parantaa monia erilaisia vaurioita hermostossa. Kobalamiinilla on myös tärkeä rooli myeliinin ylläpidolle välttämättömien rasvahappojen aineenvaihdunnassa. Tutkimukset ovat osoittaneet, että ihmiset, joilla on B12-vitamiinin puutos, paljastavat myeliinin Healthin epäsäännöllisen tuhoutumisen, mikä johtaa parlyysiin ja kuolemaan. Joitakin muita oireita puute kobalamiinin ovat huono kasvu, megaloblastinen luuytimen, ruoansulatuskanavan muutokset, Leukoopenia ja hyper-segmentoitu nutrophills, rappeuttavat muutokset selkäytimen ja hermoston ja erittyminen metyylimalonihappo ja homokystiini virtsaan.
kautta vuosien B12-vitamiini on osoittautunut välttämättömäksi hermoston toiminnalle ja punasolujen tuotannolle. Dublinin Trinity Collegen National Institutes of Healthin tutkijoiden tekemä tutkimus osoitti, että B12-vitamiinin puutos saattaa lisätä hermostoputkien vian riskiä lapsilla (Miller). Siksi kobalamiinin rakennetta ja toimintaa tutkimalla tutkijat voivat kokeilla ja muodostaa B12-vitamiinia laboratorioissaan ja palvella koko yhteisöä.