Fibrinolysis / Revista Española de Cardiología
johdanto
eteis-Kammiojohtumisongelmat ovat yleinen akuutin sydäninfarktin (AMI) komplikaatio, johon liittyy huonompi seinä. Nämä komplikaatiot liittyvät lisääntyneeseen kuolleisuuteen,1-7 ja ovat siten merkki huonommasta ennusteesta. Pre-trombolyyttisellä kaudella edenneen eteis-kammiokatkoksen (toisen tai kolmannen asteen) ilmaantuvuus inferior wall AMI: ssa oli noin 19%.5 vaikka tämä on fibrinolyyttisen hoidon aloittamisen jälkeen vähentynyt 11-12%: iin 1,3,8,9: ään, se on edelleen yksi tärkeimmistä komplikaatioista. Fibrinolyyttisen hoidon teho on sitä suurempi, mitä aikaisemmin se annetaan.10-13 inferior wall AMI täydellinen atrioventrikulaarinen lohko (CAVB), dilemma siitä, istutetaanko väliaikainen sydämentahdistin–toimintatapa, joka saattaa viivästyttää alussa fibrinolyyttinen hoito-on usein edessä. Implantaatioon liittyy myös verenvuotoriski pistoskohdassa.
kirjallisuudessa on tietoa CAVB: n esiintymistiheydestä ja kehittymisestä inferior wall AMI: ssa pre-trombolyyttisenä aikana, mutta CAVB: n kestoa fibrinolyysihoitoa saaneilla potilailla ei ole raportoitu.1,6,8 tämän työn tarkoituksena oli analysoida CAVB: n kehittymistä ja ominaisuuksia potilailla, joille oli myönnetty fibrinolyyttistä hoitoa huonompi AMI, ja verrata tuloksia potilaisiin, jotka eivät saaneet tällaista hoitoa.
potilaat ja menetelmät
1. tammikuuta 1992 ja 31.tammikuuta 2002 välisenä aikana sydänyksikköön otettiin 1134 peräkkäistä potilasta, joilla oli huonompi AMI-seinä. Näistä 552 tuotiin suoraan laitokseemme; loput ohjattiin muista keskuksista. 449 potilasta saapui kuuden tunnin kuluessa fibrinolyysin alkamisesta, ja 282 potilasta (64%) sai trombolyyttistä hoitoa. Tästä ryhmästä 39: llä (13,8%) oli CAVB (ryhmä A). Trombolyyttistä hoitoa ei annettu jäljelle jääneille 167 potilaalle (ts. näistä 449; 36%), koska sähköiset kriteerit eivät täyttyneet, koska tällainen hoito oli selvästi vasta-aiheinen, tai iän tai viiveen vuoksi saada lopullinen diagnoosi AMI, jne. Näistä 167: stä, joille ei tehty fibrinolyysiä, 13: lla (8%) todettiin CAVB (ryhmä B, kontrolli). CAVB: n kehittymistä vertailtiin näissä kahdessa hoitoryhmässä.
fibrinolyyttisen hoidon kriteerit olivat: rintakipu, joka kesti yli 30 minuuttia, ST-segmentin nousu ≥1 mm kahdesta peräkkäisestä johtimesta, 0, 04 s EKG: ssä (EKG). Osallistuminen oikean kammion diagnosoitiin Sähköiset (ST segmentin nousu V3R tai V4R), ja kliiniset ja ekokardiografiset (laajeneminen ja muutos supistuvuuden) kriteerit.
seuraavat muuttujat kirjattiin sekä ryhmässä A että ryhmässä B: potilaiden ominaisuudet, CAVB: n kronologia ja kesto, kivun alkamisen ja päivystysosastolle saapumisen välinen aika, fibrinolyyttisen hoidon aloitusaika, CAVB: n erityishoito, entsyymipiikit ja sairaalakuolleisuus.
tilastollinen analyysi
SPSS® software v. 11.0 for Windows käytettiin kaikissa tilastollisissa analyyseissä. Muuttujien jakauma analysoitiin Kolmogorov-Smirnov-testin avulla. Opiskelijan t-testiä käytettiin analysoimaan jatkuvia kvantitatiivisia muuttujia, jotka osoittivat normaalijakauman (Ikä, CK – ja CK-MB-piikit, aika CAVB: n esittämiseen ja aika fibrinolyyttisen hoidon aloittamiseen); tulokset ilmaistaan keskiarvona±keskihajonta. Mann-Whitney-testiä käytettiin vertailemaan kvantitatiivisia muuttujia, joiden jakaumat eivät olleet normaaleja (kuten cavb: n kesto); arvot ilmaistaan mediaaneina ja kvartiilien välisinä vaihteluväleinä. Dikotomisia muuttujia (sukupuoli, sepelvaltimoiden riskitekijät, angina pectoris, aiempi sydäninfarkti jne.) verrattiin χ2-testin avulla. Merkitsevyys oli p
tulokset
Potilasominaisuudet
A-ryhmän 39 potilaan keski-ikä oli 61±12 vuotta. Näistä potilaista 35 (89%) oli miehiä. Kontrolliryhmän (ryhmä B) keski-ikä oli 67±12 vuotta; 9 (69%) oli miehiä (p=NS). Taulukossa 1 esitetään kaikki kirjatut potilasominaisuudet.
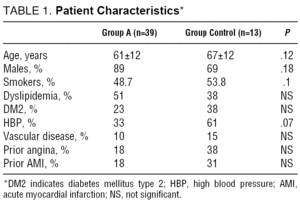
akuutin sydäninfarktin ominaisuudet
ryhmässä A 16%: lla potilaista, joilla oli Killip-luokan III-IV AMI; ryhmässä B 54%: lla potilaista, joilla oli AMI, oli nämä ominaisuudet (P=.02) (Taulukko 2).
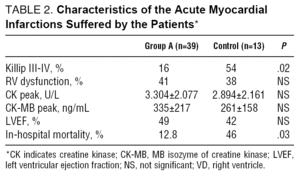
oikea kammio oli mukana 17: llä A-ryhmän potilaalla (41%), vaikka vain 12: lla (30%) oli merkittävä kliininen jälkiseuraus. Kaikilla potilailla entsyymiarvot olivat koholla. CK: n huippu oli 3,304±2.077 U/L ja CK-MB-piikki 335±117 ng/mL.
oikea kammio oli mukana 5 B-ryhmän potilaalla (38%). CK-huippu oli 2, 894±2, 161 U/l ja CK-MB-huippu 261±158 ng/mL. 2 ryhmän välillä ei havaittu merkittäviä eroja. Troponiinipitoisuuksien määrittäminen ei ollut tavanomainen käytäntö suurimman osan tutkimusajanjaksosta, joten näitä tietoja ei ole osoitettu.
fibrinolyyttinen hoito
keskimääräinen aika kivun alkamisen ja päivystykseen saapumisen välillä oli A-ryhmässä 80±53 min ja 137±73 min (P=.004) B-ryhmän osalta. Keskimääräinen aika kivun alkamisen ja fibrinolyyttisen hoidon aloittamisen välillä ryhmässä A oli 151±67 minuuttia. Trombolyyttisinä aineina käytettiin streptokinaasia (73%: ssa tapauksista), kudoksen plasminogeeniaktivaattoria (19%: ssa tapauksista) tai muita aineita (8%: ssa tapauksista).
eteis-Kammiokatkoksen ominaisuudet ja hoito
A-ryhmän 39 potilaasta 15: llä (38%) todettiin CAVB: tä saapuessaan ensimmäisen EKG: n mukaan. Ryhmässä B CAVB oli havaittavissa 8 potilaan (62%) EKG: n aloitusvaiheessa (p=NS). Ryhmän a 24 jäljellä olevasta potilaasta CAVB: n aloitusajan mediaani kivun alkamisen jälkeen oli 150 min (vaihteluväli 45-48 h). 84%: ssa tapauksista CAVB ilmaantui ensimmäisten 3 tunnin aikana kivun alkamisen jälkeen. Kahdella potilaalla CAVB ilmaantui 48 tunnin kuluttua kivun alkamisesta, eikä sitä edeltänyt rintakipu tai ST-segmentin kohoaminen uudelleen.
A-ryhmässä CAVB: n keston mediaani oli 75 min (P25 15 min, P75 120 min) (vaihteluväli 10 min-48 h); b-ryhmässä CAVB: n keston mediaani oli 1440 min (P25, 15 min, P75 5760 min) (vaihteluväli 15 min-9 päivää) (p=.004). Kun fibrinolyysi aloitettiin, CAVB palautui nopeasti sinusrytmiin. Salpauksen keston mediaani trombolyysin aloittamisesta oli 45 min (vaihteluväli 5-48 h). Jos CAVB: tä ei oteta huomioon potilaana, jolla cavb kesti 48 tuntia, fibrinolyysin alkamisen jälkeisen tukoksen keskimääräinen kesto oli 51 minuuttia. A-ryhmän potilaista 69%: lla CAVB: n kesto oli
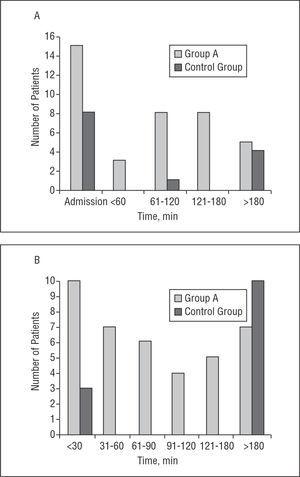
Kuva 1. A: Aika CAVB: n esittämiseen kivun alkamisen jälkeen (minuuttia). B: CAVB: n kesto (minuuttia). CAVB osoittaa täydellistä eteis-kammiokatkosta.
hoitava lääkäri teki päätökset potilaiden farmakologisesta hoidosta ja väliaikaisen sydämentahdistimen asentamisesta (Sociedad Española de Cardiología ei ollut antanut ohjeita AMI: n hoidosta ennen vuotta 1999). A-ryhmässä 18 potilasta (46%) sai atropiinia ja 3 potilasta (16, 6%) palautui sinusrytmiin. Kuusi potilasta (15%) sai dopamiinia, joista 4:llä (66%) sinusrytmi palautui 1: 1 johtumisella lyhyessä ajassa. Vain 2 potilasta sai isoproterenolia suonensisäisesti äärimmäisen bradykardian hoitoon (p=NS), mutta vain 1 potilaalla CAVB palautui sinusrytmiin. Kahdeksalle näistä potilaista (61%) annettiin dopamiinia ja kahdelle isoproterenolia (p=NS).
A-ryhmässä 17 potilasta (43%) istutettiin laskimoon alustavalla sähköiskumittarilla, kun taas B-ryhmässä 11 potilasta (84,6%) tarvitsi tätä toimenpidettä (P=.01). A-ryhmän 39 potilaasta 12: lla (30%) CAVB: tä esiintyi matala verenpaine (systolinen verenpaine
kaikilla A-ryhmän potilailla, hoitoon pääsy oli mahdollista reisilaskimon (useimmiten oikean) kautta. Neljälle edellä mainituista 17 potilaasta (23%) sydämentahdistin asennettiin ennen fibrinolyyttistä hoitoa. B-ryhmässä yhteys saatiin oikean sisäisen kaulalaskimon kautta neljällä potilaalla ja reisilaskimon kautta muilla.
CAVB: n kehittyminen
suurimmalla osalla A-ryhmän potilaista tilapäinen sydämentahdistin poistettiin 48 tunnin kuluttua, kun sinusrytmi ja 1:1 johtuminen oli saatu korjattua ja se säilyi vähintään 24 tuntia. yksikään potilas ei tarvinnut pysyvää sydämentahdistinta. Sinusrytmin palautumiseen kuluneessa ajassa ei havaittu merkitsevää eroa niiden potilaiden välillä, joiden hemodynaaminen tila oli heikentynyt cavb: llä, ja niiden potilaiden välillä, jotka sietivät blokkia paremmin. Ryhmässä B CAVB: n pitkä kesto (5 potilaalla se kesti yli 4 päivää) edellytti elektrokatetrin pitämistä paikallaan pidempään (yhdellä potilaalla 10 päivää). Yhdelle potilaalle piti asentaa pysyvä sydämentahdistin.
yhdellä A-ryhmän potilaista, joilla oli kammiotakykardia (VT), ilmeni kammiovärinä (VF) alustavan elektrokatetrin implantaation aikana. Tämä liittyi todennäköisesti toimenpiteeseen, koska se alkoi samaan aikaan, kun elektrodin ja kolmiliuskaventtiilin välinen kosketus tapahtui. Sähköinen defibrillaatio (200 J) oli tehokas eikä potilaalla esiintynyt kliinisiä seurauksia. Kaksi A-ryhmän potilasta (11.7%) osoitti suurta reisiluun hematoomaa, joka vaati verensiirron, koska hematokriittiarvo laski enemmän kuin 10 pistettä lähtötilanteen hematokriittiarvosta. Molemmissa tapauksissa hematooma ratkaistiin konservatiivisella hoidolla ilman kirurgista salaojitusta. Yhdelläkään B-ryhmän potilaista ei esiintynyt komplikaatioita, jotka johtuivat väliaikaisen sydämentahdistimen (P=NS) asennuksesta.
sairaalakuolleisuus oli A-ryhmässä 12, 8% (n=5) ja 46% (n=6; P=.03) ryhmässä B. ryhmässä A 3 potilasta kuoli tulenkestävään kardiogeeniseen sokkiin ja kaksi sähkömekaaniseen dissosiaatioon. Kaikki olivat kuoleman hetkellä sinusrytmissä. Ryhmässä B 4 potilasta kuoli tulenkestävään kardiogeeniseen sokkiin (kaikki ratkaisemattomilla CAVB: llä kuoleman hetkellä), 1 VF: n takia, joka degeneroitui asystoleksi, ja 1 septisen sokin akuutin peritoniitin takia (otettuaan talteen sinusrytmin).
keskustelu
useissa tutkimuksissa on analysoitu CAVB: n esiintyvyyttä ja sen vaikutusta ennusteeseen potilailla, joilla on huonompi sydäninfarkti, sekä pre-trombolyyttisessä era5: ssä että myöhemmin, kun fibrinolyysistä oli tullut tavanomainen toimenpide.1-9,14 fibrinolyyttistä hoitoa saavien potilaiden CAVB: n ominaisuuksista ja kestosta on kuitenkin vain vähän tietoa, eikä näissä tapauksissa noudatettavasta hoitotavasta ole juurikaan tietoa. Tähän asti McNeaill et al8: n työhön osallistui suurin potilasryhmä (n=21). Nykyisessä työssä A-ryhmä koostui kuitenkin 39 potilaasta, joilla kaikilla oli cavb: n komplisoima alempiarvoinen ami. Tämä oli huomattavaa 43%: lla näistä potilaista EKG: n aloitusvaiheessa. Suurin osa sai fibrinolyyttisen hoidon kahden tunnin kuluessa hoidon alkamisesta. Samanlaisia esitystietoja on kirjattu muissakin tutkimuksissa, 1,6 ja 8, mukaan lukien TIMI II-tutkimus1, jossa 54%: lla potilaista todettiin CAVB: tä sisäänottohetkellä,ja Melgarejon ym.tutkimuksessa 6, jossa 67%: lla potilaista todettiin CAVB: tä sisäänottohetkellä tai seuraavan tunnin aikana.
vaikka CAVB: n ilmaantuvuus oli sama molemmissa nykyisissä ryhmissä, se kesti merkitsevästi lyhyemmin potilailla, jotka saivat fibrinolyysiä (ryhmä A) kuin potilailla, jotka eivät saaneet fibrinolyysiä (ryhmä B) (mediaani 75 min verrattuna 1440 min; P=.004). Vaikka tässä tutkimuksessa oli vain vähän potilaita, tämä havainto on kliinisesti merkittävä, koska se tukee ajatusta siitä, että trombolyysiä tulisi yrittää potilailla, joilla on huonompi AMI ja CAVB keinona ratkaista nopeasti tämä komplikaatio. Jos nopeaa resoluutiota voidaan odottaa, voidaan välttää aggressiivisempien tekniikoiden käyttöä, kuten alustavan elektrokatetrin asentamista (joka ei ole riskitön).
tässä tutkimuksessa fibrinolyyttisen hoidon jälkeen CAVB palautui nopeasti ja sinusrytmi ja 1:1 johtuminen palautui reilussa tunnissa noin puolella potilaista ja alle kahdessa tunnissa 69 prosentilla. Nämä tiedot ovat yhtäpitäviä Mcneaillin ja muiden potilaiden (8) kanssa,jotka ilmoittivat CAVB: n palautuneen 52%: lla potilaista 2 tunnin kuluessa trombolyysin aloittamisesta, sekä Tami-tutkimuksen (14) kanssa,jossa CAVB: n todettiin kestävän keskimäärin 2, 5 tuntia ja alle 12 tuntia 75%: lla potilaista.
nykyisillä potilailla atropiinin (Sociedad Española de Cardiología guidelines-ohjeiden luokan I käyttöaihe)15 annolla saavutettiin CAVB:n palautuminen ja 1: 1 johtuminen 16 potilaalla.6% A-ryhmän potilaista ja 33% B-ryhmän potilaista. Nämä eivät ole arvostamattomia tuloksia, kun otetaan huomioon tällaiseen hoitoon liittyvät harvat haittavaikutukset; mielestämme atropiinihoitoa tulisi aina aluksi yrittää, ellei selviä vasta-aiheita ole. Dopamiinin tai isoproterenolin antamista ei ole mainittu edellä mainituissa ohjeissa, eikä niiden käyttöä ole mainittu muissa tutkimuksissa. Nykyisessä työssä dopamiinia annettiin vain pienelle joukolle potilaita, mutta sinusrytmi saavutettiin 66 prosentilla A-ryhmän potilaista. Tämä lääke voi olla hyötyä huonompi seinä AMI oireenmukainen CAVB, erityisesti keskuksissa, joissa väliaikaisia tahdistimia ei voida istuttaa. Dopamiini ja isoproterenoli voivat lisätä kammion pakorytmin tiheyttä ja aiheuttaa lievää kliinistä ja hemodynaamista paranemista. Nykyisen ja muiden tutkimusten8 tulokset osoittavat kuitenkin, että ne vain harvoin palaavat cavb omasta.
suurimmalla osalla fibrinolyysiä saaneista potilaista CAVB oli suhteellisen hyvin siedetty. Vain 30 prosentilla potilaista hemodynaaminen tila heikkeni merkittävästi (hypotensio ja vaikea bradykardia), eikä atropiinille saatu vastetta. Nämä potilaat saivat alustavan sähköiskumittarin, ja heidän kliininen tilanteensa parani sydämentahdistimen aiheuttaman sykkeen nousun myötä.
fibrinolyysin teho inferior wall AMI: n hoidossa on osoitettu,10,11,16 hyöty on sitä suurempi mitä aikaisemmin tämä hoito aloitetaan.12,13 alustavan elektrokatetrin istuttaminen voi viivästyttää fibrinolyyttisen hoidon aloittamista–viive voi olla pidempi potilailla, joita alun perin hoidettiin pienissä sairaaloissa ja jotka sitten ohjataan suurempiin keskuksiin väliaikaisen sydämentahdistimen asentamista varten. Trombolyyttinen hoito on luultavasti tehokkain CAVB17: n palautumisessa; viivästynyt aloitus voi viivästyttää eteis-kammiosolmun reperfuusiota, jonka iskemia voi hypoteettisesti liittyä CAVB: n fysiologiaan.1 Tämän seurauksena CAVB: n kesto olisi pidempi.
tässä tutkimuksessa väliaikaiset tahdistimet asennettiin 43%: lle A-ryhmän potilaista (17 potilasta 39: stä). Näin hoidettujen määrä vaihtelee kuitenkin suuresti samankaltaisten tutkimusten välillä, esimerkiksi melgarejon ym. tekemässä tutkimuksessa 6 58% potilaista sai väliaikaisen pacemake r: n, kun taas Mcneaillin ym.tutkimuksessa vain 17% sai saman.8 kahdellatoista A-ryhmän 17 potilaastamme (30%) esiintyi vaikeaa bradykardiaa ja hypotensiota, mikä viittaa siihen, että elektrokatetrin asentaminen oli suositeltavaa. Kuitenkin tämän tutkimuksen tulokset osoittavat, että tällainen hoitojakso muiden 5 on kyseenalainen. Väliaikaisen sydämentahdistimen kiinnittäminen oli tarpeen useammin B-ryhmän potilailla, jotka eivät saaneet trombolyyttistä hoitoa (84, 6% verrattuna 43%: iin; P=.01). Tässä ryhmässä suurella enemmistöllä havaittiin huomattavaa hemodynaamista heikkenemistä (hypotensio ja vaikea bradykardia), ja CAVB: n kesto oli huomattavasti pidempi.
Transvenoottinen ohimenevä sydämen stimulaatio fibrinolyyttistä hoitoa saaneella tai pian saatavalla potilaalla ei ole Maksuton. Tässä tutkimuksessa 2 potilaalle (11, 8%) kehittyi reisiluun hematooma (ratkaistu paikallisella paineella), joka vaati verensiirron. McNeaill et al8 eivät raportoineet tätä komplikaatiota, vaikka Melgarejo et al6 raportoivat, että 3, 6%: lla heidän potilaistaan oli sama sairaus. Vaikka suurin trombolyyttinen vaikutus ei ole sama kuin elektrokatetrin kiinnittäminen, verenvuotoriski jatkuu noin 24-48 tunnin ajan toimenpiteen jälkeen, koska koadjuvanttihoito hepariinilla ja aggregaatiota estävillä lääkkeillä aiheuttaa vaikutuksia.
alustavan elektrokatetrin asentamiseen liittyy myös potentiaalisesti tappavien rytmihäiriöiden riski noin 3, 6%: ssa tapauksista.6 ryhmässä A yhdellä potilaalla (5,8%) oli VT, joka degeneroitui VF: ksi elektrokatetrin kiinnittymisen aikana; tämä tapahtui elektrodin joutuessa kosketuksiin kolmiliuskaventtiilin kanssa. Tilanne ratkaistiin defibrillaatiolla. Vaarana on myös, että sähköshokki puhkaisee kammion. Jotkut tutkimukset arvioivat tämän tapahtuvan 4%: ssa tapauksista,18, mutta se voisi olla yleisempää potilailla, joilla on AMI mukana oikean kammion, koska kudos on vähemmän kestävä. Yhdelläkään potilaalla ei ollut tätä komplikaatiota tässä tutkimuksessa, eikä kenelläkään ollut tällaista vaikutusta Melgarejo et al6-tai McNeaill et al-tutkimuksissa.8
toinen vaihtoehto transvenoottiselle sähkövatkaimelle on transkutaanisen tahdistimen käyttö. Tämä on kuitenkin erittäin kivulias tekniikka ja vaatii yleensä voimakasta analgesiaa, ehkä jopa farmakologista sedaatiota, joka voi aiheuttaa potilaan heikkenemisen. Sen vuoksi sitä tulisi käyttää vain, jos hemodynaaminen tila heikkenee (hypotensio ja vaikea bradykardia) ja kun infrastruktuuri ei riitä väliaikaisen, transvenoottisen elektrokatetrin välittömään asentamiseen.
Tutkimuksen rajoitukset
tämä työ on havainnoiva tutkimus, jossa vertailuryhmä on pieni (potilaat, joille on otettu sydäninfarkti, johon liittyi alempi seinämä viimeisten 6 tunnin aikana, jota vaikeuttaa CAVB, ja jotka eivät saaneet fibrinolyyttistä hoitoa). Vuoden 2000 jälkeen kaikki AMI-potilaat ovat saaneet trombolyysia tai pallolaajennusta ensimmäisen 6 tunnin aikana, ellei kyseessä ole selkeästi vasta-aiheinen hoito. Silti tutkimus on kliinisesti kiinnostava, koska se antaa tietoa CAVB: n kestosta potilailla, jotka ovat fibrinolyysiä-juuri nämä tapaukset herättävät suurimmat epäilyt siitä, mitä terapeuttista kurssia tulisi noudattaa. Johtopäätösten arvoa korostaa kuitenkin jo se, että merkittäviä tuloksia saatiin, vaikka määrät olivat pieniä.
kliiniset seuraamukset
ottaen huomioon nykyiset ja muiden tekijöiden tulokset, CAVB: n kesto inferior wall AMI: ssa on lyhyt, kun sitä hoidetaan fibrinolyysillä. Tämä komplikaatio kestää trombolyysissä huomattavasti lyhyemmän ajan kuin silloin, kun ei seurata reperfuusiohoitoa. Edellä mainittuun sairauteen liittyvä kuolleisuus on myös pienempi, kun tällaista hoitoa tarjotaan. Siksi fibrinolyyttistä hoitoa tulisi antaa cavb-hoidon alkuvaiheessa.
tässä tutkimuksessa trombolyyttinen hoito johti siihen, että vähemmän potilaita tarvitsi väliaikaisen sydämentahdistimen. CAVB: n lyhyen keston vuoksi sydämen tilapäinen stimulaatio laskimoyhteyden kautta tulisi varata potilaille, joilla on huono hemodynaaminen toleranssi (potilaat, joilla on CAVB ja matalat kammiotaajuudet, hypotensio ja/tai kardiogeeninen sokki), koska tämä tekniikka ei ole vapaa komplikaatioista.
kiitokset
tekijät kiittävät Josep Lupón ja Jorge López Ayerbe keskuksestamme apunaan tilastoanalyysissä.