Opas sidekalvon kasvaimiin
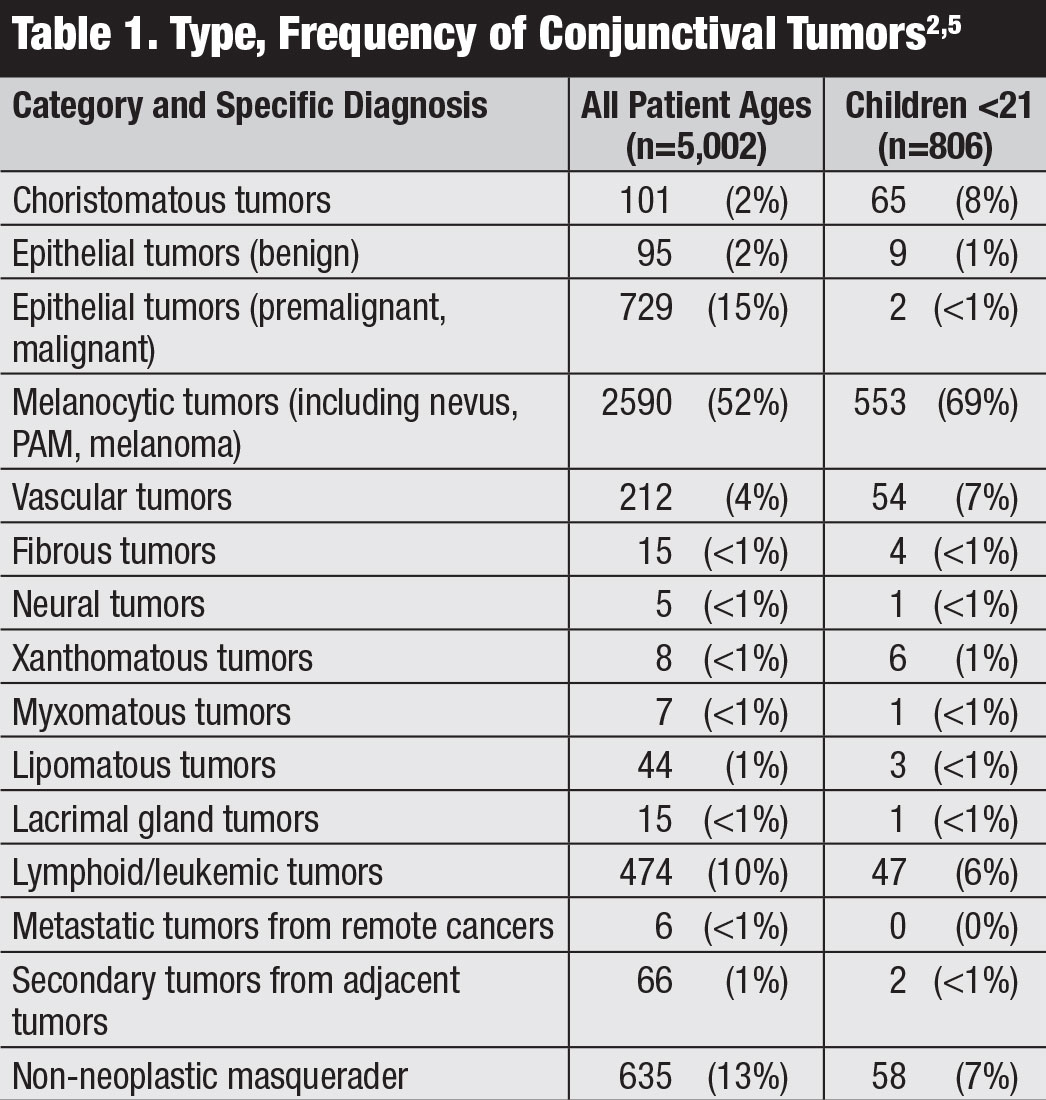
sidekalvon kasvaimiin sisältää hyvän-ja pahanlaatuisten kasvainten kirjon.1-5 tyypit eroavat iän ja rodun, systeemisen immuunitilanteen ja pitkäaikaisen altistuksen perusteella. Laaja tutkimus, jossa oli 5 002 tapausta silmän onkologiakeskuksesta, paljasti, että 52% oli hyvänlaatuisia, 18% oli premalignantteja ja 30% pahanlaatuisia (Taulukko 1).1,2 vaikka tämä raportti oli peräisin silmän onkologiakeskuksesta ja maligniteetit saattavat olla yliedustettuina, on tärkeää, että kliinikot ymmärtävät erilaisia sidekalvon kasvaimia.
viisi yleisintä kasvainta olivat luovi (23%), okulaariset neoplasiat (ossn, 14%), primaarinen hankittu melanoosi (PAM, 12%), melanooma (12%) ja imukasvain (9%).5 pahanlaatuisia kasvaimia havaittiin useimmin aikuisilla ja niitä olivat melanooma (12%), okasolusyöpä (SCC, 9%), lymfooma (7%), Kaposin sarkooma (<1%), etäpesäke (<1%) ja muut.1 sidekalvon kasvaimia lapsilla osoittaa maligniteetti vain 3% ajasta.5
tämä katsaus yleisimpiin sidekalvon kasvaimiin valmistaa sinua hoitamaan niitä asianmukaisesti, joko toimistossasi tai lähetteellä.
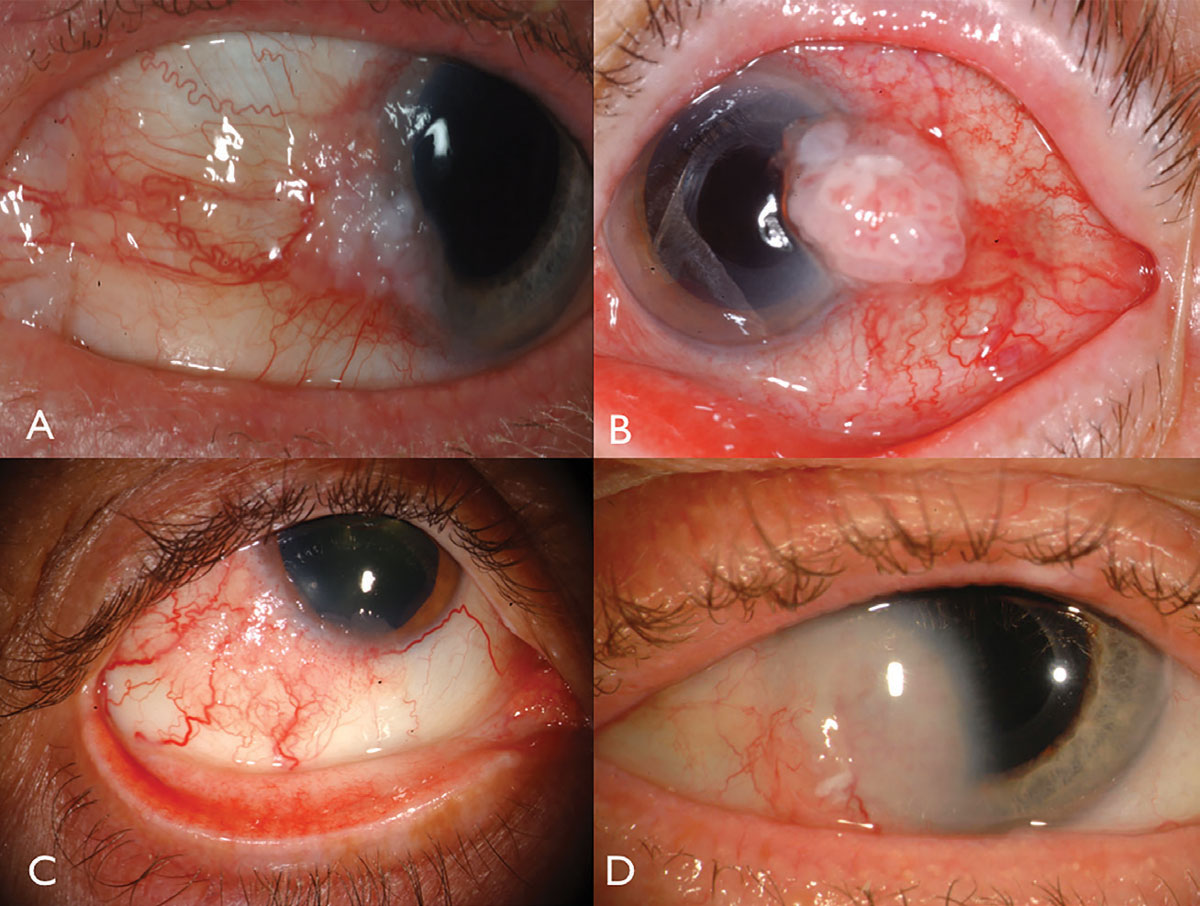
Kuva. 1. Limbaali OSSN: leukoplakia ja sarveiskalvo (a), huomattava luontainen verisuonisto ja syöttöalukset (B), HIV-potilaalla (C) ja syvä sarveiskalvon invaasio, joka vaatii resektiota ja plakin sädehoitoa (D). Klikkaa kuvaa suuremmaksi.
Ossn: n yleinen kliininen termi sisältää maligniteettien kirjon, joka vaihtelee lievistä epiteelikudosmuutoksista, kuten sidekalvon intraepiteelisistä neoplasioista (CIN), vaikeampaan invasiiviseen karsinoomaan, joka tunkeutuu kellarikalvon läpi substantiapropriaan, kuten okasolusyöpään.
kliiniset ominaisuudet. Sidekalvon ossn klassisesti esiintyy vanhemmilla valkoihoisilla miehillä, erityisesti niillä, joilla on krooninen altistuminen auringolle. Yhdysvalloissa sidekalvon SCC on viisi kertaa yleisempää miehillä ja valkoihoisilla. Afrikassa sidekalvon SCC on kuitenkin lähes yhtä yleinen miehillä ja naisilla, ja se esiintyy nuorempana kuin Yhdysvalloissa.
okulaarin pinnan levyepiteelit esiintyvät yleensä yksipuolisena, vaskularisoituneena hyytelömäisenä massana, joka sijaitsee auringolle altistuneessa sidekalvossa nenän tai ohimon limbus-alueella (Kuva 1). Leukoplakia, laajentuneet syöttöalukset ja viereisen sarveiskalvon epiteelin vaahtomainen tunkeutuminen voi esiintyä ja voi harvoin tunkeutua maapallolle tai kiertoradalle.
klikkaa taulukkoa suuremmaksi.
altistavat tekijät. OSSN: n tärkeimpiä ympäristötekijöitä ovat krooninen auringolle altistuminen ja tupakansavulle altistuminen. Kaksi keskeistä isännälle altistavaa tekijää ovat vaalea iho ja taustalla oleva ihmisen immuunikatovirus (HIV) ja ihmisen papilloomavirus.6 potilaat, joilla on immuunipuutos, erityisesti ne, joilla on HIV, ovat vaarassa OSSN ja voi olla pitkälle edenneitä, kahdenvälisiä ja invasiivisia kasvaimia.1 Tämä näkyy erityisesti Afrikassa, jossa HIV on yleistä ja OSSN esiintyy sekä miehillä että naisilla ja nuoremmalla iällä.6 muut immuunisäätelyhäiriöt voivat altistaa potilaan OSSN: lle, mukaan lukien elinsiirron immunosuppressio, ekseema/atopia, silmän sikatrinen pemfigoidi, xeroderma pigmentosum ja autoimmuunisairaudet.7
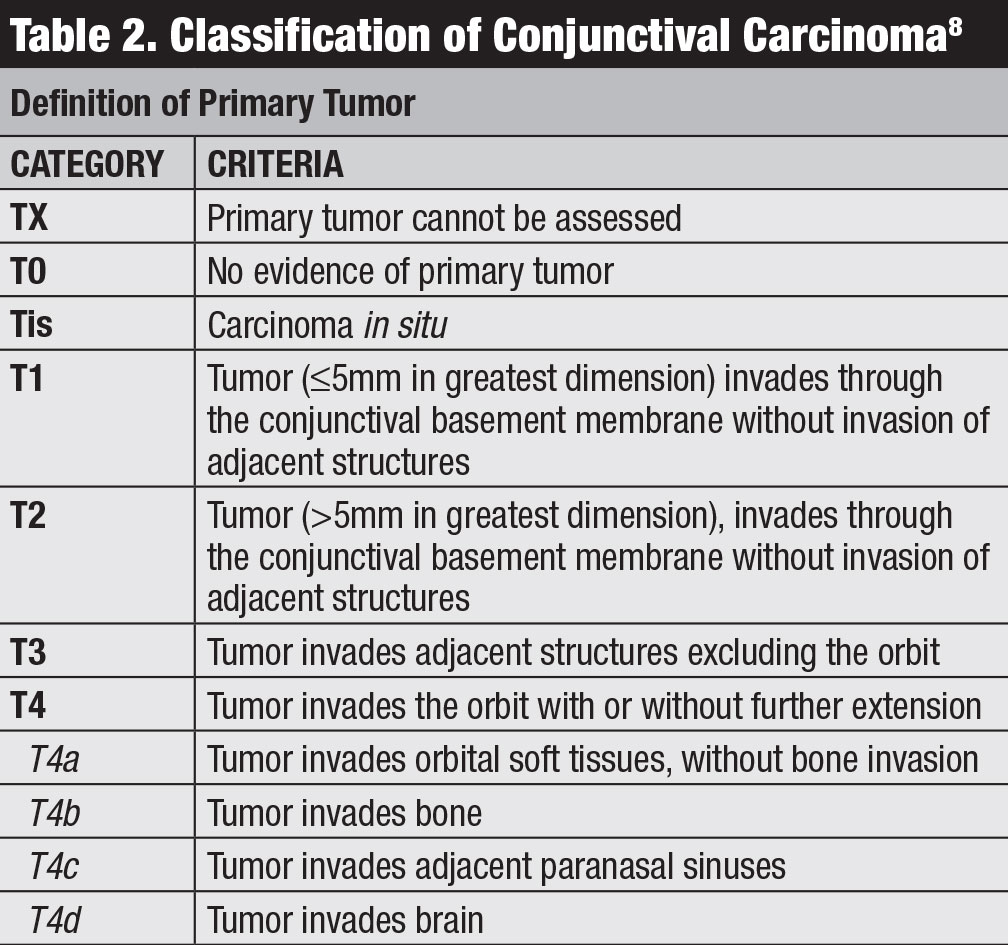
luokitus. American Joint Committee on Cancer (AJCC) ‘ s 8th edition manual tarjoaa viimeisimmän luokituksen sidekalvon karsinooma, mukaan lukien SCC ja CIN (Taulukko 2).8
johtaminen. Tähän kuuluu kirurginen resektio “No-touch” -tekniikalla tai ei-kirurgiset hoidot, kuten paikallinen kemoterapia mitomysiini C: llä (MMC) tai 5-fluorourasiililla (5-FU), paikallinen tai injektoitu immunoterapia interferoni alfa-2b: llä (IFN), ajankohtainen viruslääke (sidofoviiri) tai fotodynaaminen hoito.7,9-11
kirurgiseen no-touch-tekniikkaan kuuluu kasvaimen yksityiskohtainen arviointi rakolampun biomikroskopian avulla, jotta voidaan visualisoida kaikki kasvaimen marginaalit, mukaan lukien bulbar -, forniceal-ja tarsal-komponentit, jotta voidaan ymmärtää kasvaimen koko laajuus ja jotta kliinikko voi käsin piirtää mallin tallennuksen.9 Tämä malli otetaan sitten leikkaus varmistaa koko kasvain on poistettu.
leikkaushetkellä pidetään pihdeillä kiinni vain ympäröivästä normaalista kudoksesta,eikä kasvaimeen koskaan kosketa, jotta kasvain ei kasvaisi. Lisäksi tasapainoista suolaliuosta ei käytetä leikkauksessa syöpäsolujen nestemäisen dispersion välttämiseksi. Kasvaimen poistamisen jälkeen sulkeminen puhtailla välineillä on ratkaisevan tärkeää. Käyttämällä tätä tekniikkaa OSSN, kasvaimen pysyvyys tai toistuminen löytyy alle 5% tapauksista.
klikkaa taulukkoa suuremmaksi.
paikallinen 5-FU-tai MMC-kemoterapia parantaa tehokkaasti OSSN: ää, usein kahden-neljän viikon kuluessa hoidosta, vaikka kantasolujen puutoksen riski on olemassa. Meidän ajankohtainen hoito etusija on immunoterapia IFN, koska se on hyvin siedetty hyvä kasvain ohjaus, usein yli kolme kuukautta ja vähän komplikaatio ja vain vähäinen follikulaarinen sidekalvotulehdus.10, 11 nämä lääkkeet voivat olla paikallisesti myrkyllisiä sarveiskalvon epiteelille, mutta vähemmän interferonilla, ja potilaita tulee seurata tarkasti niiden käytön aikana. Jos kustannukset ovat tekijä potilaalle, ajankohtainen 5-FU on halvin, jonka jälkeen MMC ja sitten IFN.
sidekalvon Imukudoskasvaimet
Imukudoskasvaimet vaihtelevat matalan ja korkean asteen kasvaimista ja johtuvat lymfosyyttien monoklonaalisesta proliferaatiosta. Imukudoskasvaimet, jotka esiintyvät periokulaarisella alueella usein liittyy useita kudoksia, kuten sidekalvon, kiertoradalla ja silmäluomen ja kutsutaan “silmän adnexal” imukudoskasvaimia, mukaan lukien hyvänlaatuinen reaktiivinen lymfoidi hyperplasia (BRLH) ja lymfooma.
brlh ja lymfooma ovat spektrin vastakkaisissa päissä; BRLH esiintyy kliinisesti paikallisena “lohilaastarina” ja histopatologisesti hyvänlaatuisena, kun taas lymfooma esiintyy myös “lohilaastarina”, mutta aggressiivisempana histopatologisena piirteenä, jolla on mitoottinen vaikutus ja joka luokitellaan pahanlaatuiseksi.
Okulaariset adnexaaliset imukasvaimet ovat tyypillisesti B-soluperää. Monikeskustutkimuksessa, johon osallistui 268 sidekalvolymfoomapotilasta, neljä yleisintä tyyppiä olivat ekstranodaalinen marginaalivyöhykkeen lymfooma (enmzl, jota aiemmin kutsuttiin limakalvoihin liittyväksi imukudokseksi) 68%: lla, follikulaarinen lymfooma (FL) 16%: lla, manttelisolulymfooma (MCL) 7%: lla ja diffuusi suuri B-solulymfooma (DLBCL) 5%: lla.12 muuta sidekalvolymfoomatyyppiä ovat lymfoplasma-lymfooma ja plasmasytooma.
kliiniset ominaisuudet. Sidekalvon lymfooma esiintyy yleensä vanhemmilla potilailla vuotiaita 60 ja 70. Tämä kasvain voi ilmetä ensisijainen lymfooma, rajoittuu periocular alueella, tai toissijainen lymfooma taudin muualla. Suurin osa primaarisesta lymfoomasta esiintyy enmzl: llä ja FL: llä sekä sekundaarisesta lymfoomasta DLBCL: llä ja MCL: llä. Yhdessä analyysissä 117: stä sidekalvolymfoomapotilaasta todettiin systeeminen osallisuus 31%: lla, useimmiten niillä, joilla oli molemminpuolinen multifokaalinen silmän adnexal lymfooma.13
sidekalvon lymfooma ilmenee klassisesti vaaleanpunaisena lohenvärisenä, sileäpintaisena subjunktiaalisena massana, joskus syöttöaluksineen (kuva 2). Tämä sileä, multilobulated massa voi muistuttaa follikulaarinen tai papillaarinen sidekalvotulehdus. Tämä kasvain sijaitsee useimmiten sidekalvon fornix (44%) tai midbulbar (42%) alueella ja, harvoin, caruncle (7%) tai limbus (7%).13 sidekalvon lisäksi lymfoomaa voi esiintyä soluttautuneena kiertorataan, silmäluomeen tai uveaan.13 useimmat potilaat, joilla sidekalvon lymfooma ei ole silmänsisäinen komponentti, mutta jos läsnä, se asuu yleensä uvea eikä verkkokalvon tai lasiaisen.
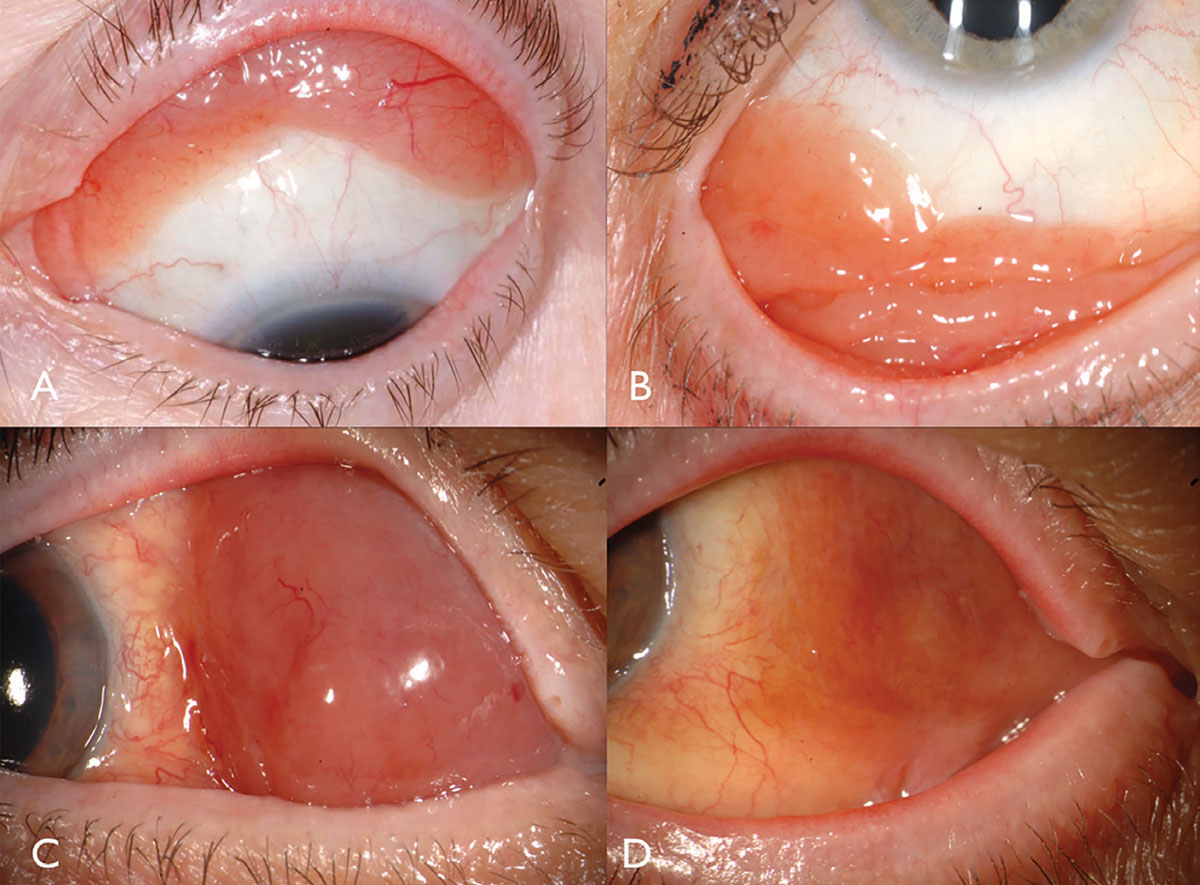
Fig. 2. Conjunctival lymphoma can be salmon-pink (A) or multilobulated forniceal (B). Medial forniceal conjunctival lymphoma before (C) and after (D) ritiximab. Click image to enlarge.
Predisposing factors. Immune dysfunction and autoimmune conditions, as well as infective etiologies such as Helicobacter pylori and Chlamydia psittaci are all predisposing factors for conjunctival lymphoma. BRLH voi olla mahdollinen lymfooman esiaste, ja vaikka sitä esiintyy pääasiassa aikuisilla, sitä voi esiintyä satunnaisesti lapsilla.5 itse asiassa, nuorempi potilas aikaan diagnoosi sidekalvon imukudoksen kasvain, sitä todennäköisemmin se on BRLH eikä lymfooma.
luokitus. Useita luokituksia sidekalvon lymfooma olemassa, mukaan lukien Ann Arbor, Maailman terveysjärjestö ja AJCC 8th edition lavastus (Taulukko 3).8 AJCC kliininen lavastus perustuu kasvaimen sijainti, alueellinen imusolmuke ja kaukainen osallistuminen.8
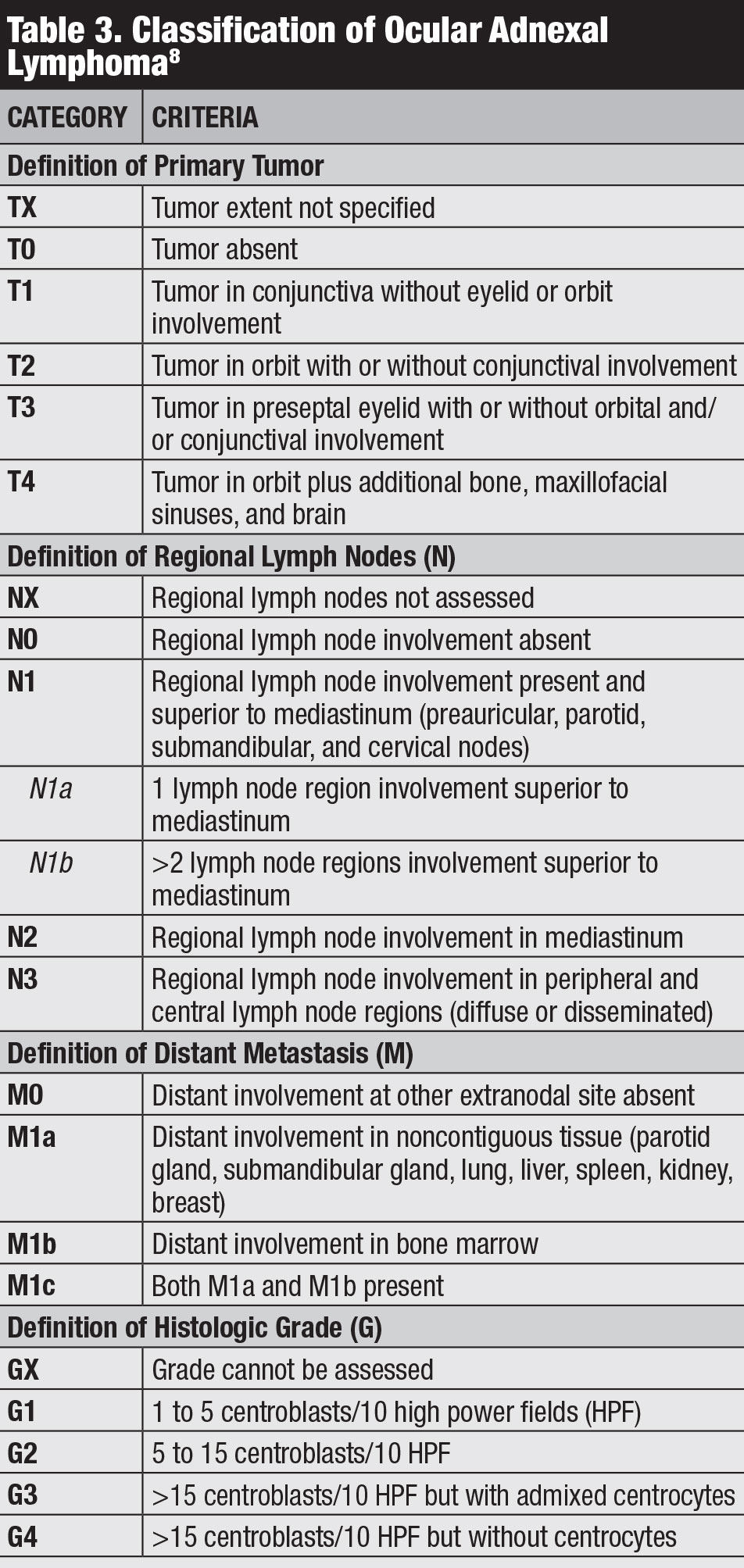
klikkaa taulukkoa suuremmaksi.
johtaminen. Hoito potilailla sidekalvon lymfooma riippuu ensisijaisesti laajuus periocular osallistuminen, systeeminen osallistuminen ja niiden yleinen terveys. Potilailla, joilla on vain sidekalvon lymfooma eikä systeemistä vaikutusta, hoito keskittyy täydelliseen kirurgiseen resektioon. Hoito ulkoinen sädehoito tai rituksimabi ovat vaihtoehtoja, jos kasvain ei ole havaittavissa. Periokulaarista ja systeemistä lymfoomaa sairastaville systeemisen rituksimabin hoito tai kemoterapian lisääminen ovat näkökohtia.
sidekalvolymfooman systeeminen ennuste liittyy suoraan kuhunkin alatyyppiin, sillä erään tutkimuksen mukaan viiden vuoden elossaoloaika oli ENMZL: llä 97%, FL: llä 82%, DLBCL: llä 55% ja MCL: llä vain 9%.12
Sidekalvomelanooma
Sidekalvomelanosyyttiset kasvaimet ovat kiistatta yleisiä, ja ne edustavat yli 50%: a tapauksista, joissa silmän syöpätautien yksikössä on suuri sarja sidekalvokasvaimia.1,2 tämä melanosyyttisten kasvainten luokka sisältää monia tyyppejä, kuten luomi, ihonväriin liittyvä melanoosi, Pam, toissijainen hankittu melanoosi, melanooma ja etäpesäkkeet.1-5 joillakin mantereilla, joissa potilailla on tummia komplekseja, jopa OSSN voi esiintyä melanosyyttisesti. Näistä leesioista sidekalvon luomi edustaa 45% ja primaarinen sidekalvomelanooma edustaa 23% kaikista melanosyyttisistä kasvaimista silmän syöpätautien hoidossa.2
Yhdysvalloissa sidekalvomelanooman ikäkorjattu ilmaantuvuus kaksinkertaistui vuosien 1973 ja 1999 välillä 0,27 miljoonasta 0,54 miljoonaan.14,15 ilmaantuvuus lisääntyi 295% valkoisilla miehillä Yhdysvalloissa saman 27 vuoden jakson aikana, erityisesti 60-vuotiailla tai sitä vanhemmilla miehillä.14 tutkijaa arvelee, että lisääntyvä nopeus saattaa liittyä ultraviolettivalolle altistumiseen.
kliiniset ominaisuudet. Sidekalvomelanooma on pigmentoitunut tai pigmentoimaton maligniteetti, joka voi syntyä Pamista, luovasta tai de Novosta.16 melanooma löytyy limbal, bulbar, forniceal tai palpebral sidekalvon ja usein osoittaa laajentuneen, mutkikas syöttölaite ja luontainen alukset tyypillisesti ympäröi tasainen Pam (kuva 3). Yleensä kasvaimet, jotka mittaavat yli 2 mm paksuutta, ovat merkittävässä vaarassa imusolmuke etäpesäkkeitä. Kasvaimen invaasio kiertoradalle on erityisen vakava ja merkittävä metastaattinen riski.
50%: ssa tapauksista esiintyy paikallista kasvaimen uusiutumista tai uutta kasvainta, joka liittyy usein uuteen PAM-transformaatioon. Etäpesäke-usein preaurikulaariseen, submandibulaariseen tai kohdunkaulan imusolmukeketjuun—löytyy 25%: lla potilaista. Sentinel imusolmuke biopsia voi auttaa kliinikot arvioida subkliininen imusolmuke soluttautuminen. Moninkertainen toistuminen, erityisesti ne, joihin kiertorata, edellyttävät kiertoradan poistumista.
altistavat tekijät. Tärkein sidekalvomelanooman altistava tekijä on pitkäaikainen sidekalvon luomi eli PAM.16-18 kun sidekalvomelanooman alkuperää tutkittiin histopatologisesti, tutkijat havaitsivat alkuperän olevan PAM 74%: lla, de novo 19%: lla ja nevus 7%: lla.16 kliinistä tutkimusta arvioi, että joka 300 nevistä kehittyy melanooma.17,18
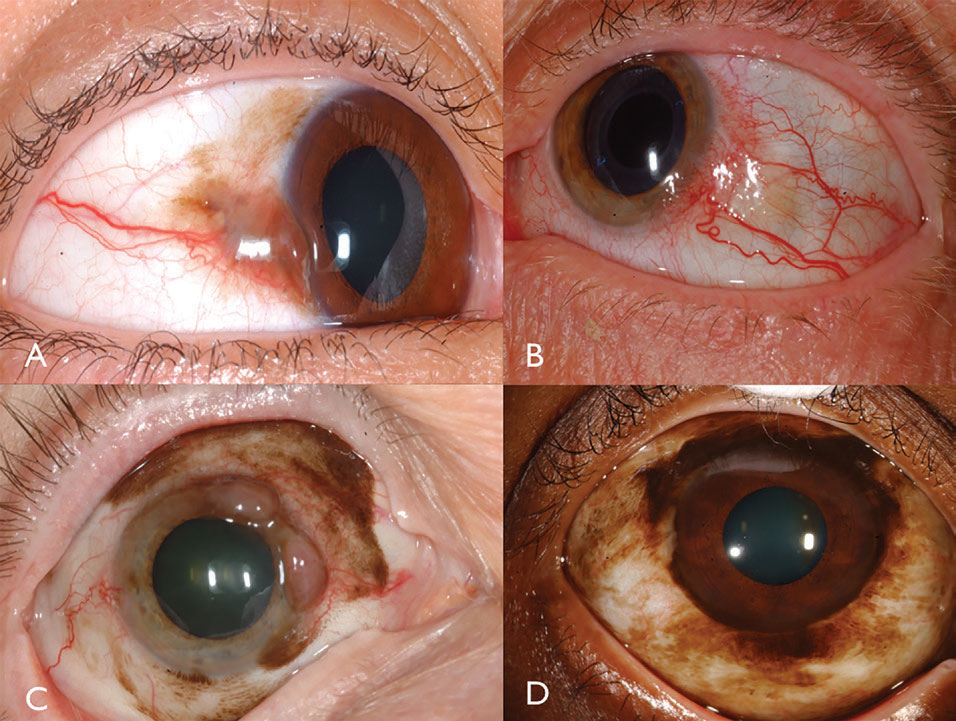
Kuva. 3. Pigmentoitunut sidekalvomelanooma voi syntyä Pam (A). Pigmentittömässä sidekalvomelanoomassa voi olla voimakas verisuonitus (B). PAM voi myös aiheuttaa sekapigmentoidun / pigmentittömän sidekalvomelanooman (C). PAM aiheutti limbaalisen melanooman tällä Afroamerikkalaisella potilaalla (D). Klikkaa kuvaa suuremmaksi.
laajassa kliinisessä tutkimuksessa havaittiin, että PAMin 10 vuoden riski muuttua melanoomaksi oli noin 9 prosenttia, ja Pamin suurempi riski muuttua melanoomaksi.19 siksi on tärkeää tunnistaa PAM ja hoitaa tämä ehto kirurginen, kylmähoito ja jopa pinnallinen keratectomy (jos on sarveiskalvon osallistuminen) tarkoituksena on estää melanooma.
sidekalvon luoman eriytyminen melanoomasta voi olla haastavaa. Tuoreessa analyysissä 510 tapausta sidekalvon luomi vs. melanooma lapsilla, melanooma oli yleisempi vanhemmilla lapsilla, suhteellinen riski (RR) oli 4, 80, suurempi kasvaimen paksuus (RR 1, 14), suurempi emäs (RR 4, 92), kasvaimen verenvuoto (RR 25, 30) ja sisäsyntyisten kystien puuttuminen (RR 5, 06).5 tutkijat määritetty nämä ominaisuudet, ennustava sidekalvon melanooma lapsilla, on muistisääntö: CATCH melanooma, edustavat: Lapset ikä vanhempi, paksuus/pohja suurempi, kysta puuttuu, verenvuoto melanooma.5
myös PAMin eriytyminen melanoomasta voi olla haastavaa; melanooma on kuitenkin paksuudeltaan ja Pam on täysin litteä. Analyysissä tarkasteltiin 1 224: ää PAM vs. melanoomatapausta kaikenikäisillä, melanoomaa, joka oli merkitsevästi suurempi potilaan mediaanin iän perusteella (54 vs. 61 vuotta), miessukupuoli (35% vs. 49%), sijainti fornix-potilailla (2% vs. 6%) ja tarsus-potilailla (1% vs. 4%), suurempi keskipohjaisen läpimitan mediaani (6mm vs. 8mm), paksuus (<1mm vs. 1mm), syöttöalukset (10% vs. 48%) ja sisäsuonet (4% vs. 33%); ja verenvuoto (<1% vs. 3%).2
kudosbiomarkkerit ovat tärkeitä sidekalvomelanooman arvioinnissa ja niihin kuuluvat BRAF-mutaatio, TERT-promoottorimutaatio ja PTEN-mutaatio.1 näiden biomarkkerien tunnistaminen on ratkaisevan tärkeää, kun suunnitellaan systeemistä hoitoa etäpesäkkeiden hoitoon tai ehkäisyyn, sillä tiettyihin biomarkkereihin on saatavilla kohdennettuja hoitoja, kuten VEMURAFENIBIA BRAF-mutatoituneeseen maligniteettiin.
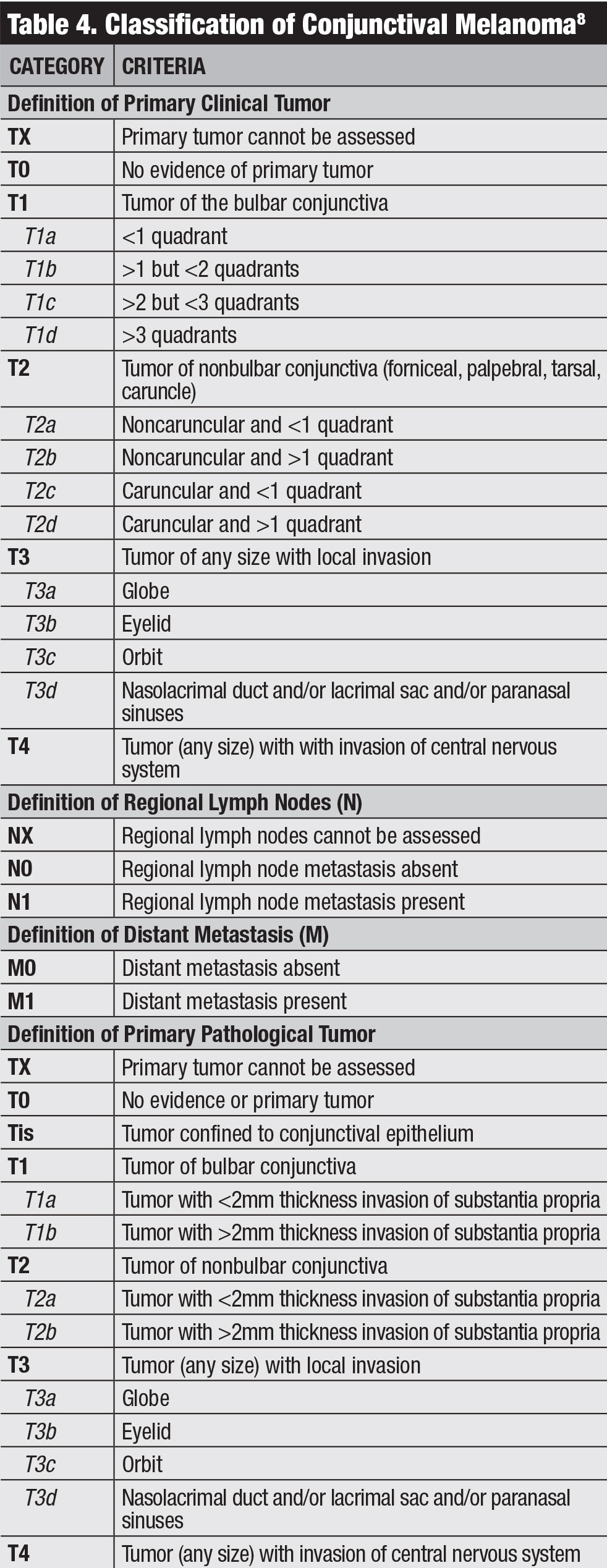
klikkaa taulukkoa suuremmaksi.
luokitus. AJCC: n kliininen luokittelu sidekalvomelanoomaan perustuu kasvaimen laajuuteen kvadranteilla, kasvaimen sijaintiin ja invasiivisiin ominaisuuksiin (Taulukko 4).8 tiimimme tutki tuloksia sidekalvon melanooma perustuu AJCC 7. painos ja totesi Tämä lavastus oli erittäin ennusteita.20 melanoomassa, joka luokiteltiin T2: ksi ja T3: ksi (verrattuna T1: een), esiintyi huomattavasti enemmän paikallista uusiutumista, alueellista imusolmukepesäkettä, kaukaista etäpesäkettä ja kuolemaa.
johtaminen. Hoito sidekalvon melanooma pohjimmiltaan liittyy täydellinen kirurginen resektio käyttäen no-touch tekniikka välttää kasvaimen Kylvö. Ensimmäinen leikkaus on tärkein, sillä koko kasvaimen herkkä poisto ilman kasvaimen kylvöä on avain tulevien uusiutumisten ja etäpesäkkeiden estämiseen.
sarveiskalvon limbusalueen melanooma poistetaan leikkausmikroskoopilla myös kosketuksetonta tekniikkaa käyttäen. Litteä sarveiskalvon komponentti poistetaan absoluuttisella alkoholilla, pinnallinen epiteliektomia ilman häiriöitä Bowmanin kalvo. Sidekalvon osa poistetaan 2mm 3mm marginaalit ja vapautetaan limbus käyttäen tasainen episcleral dissection. Jos kovakalvon invaasio on läsnä, plakin sädehoitoa sovelletaan. Kaikki sidekalvon reunukset hoidetaan kaksinkertaisella kylmähoidolla.
rekonstruktioon kuuluu primäärinen sulkemistekniikka, rotaatioläppä tai lapsiveden kalvosiirto, usein symblepharonirengas, jossa on lapsivesikalvo. Kiertoradalle ulottuva melanooma vaatii kiertoradalta poistumista tai viime aikoina immunoterapiaa, jossa on tarkastuspisteen esto.21
sidekalvomelanoomaa sairastavia potilaita tulee tarkkailla silmälläpidettävästä onkologista paikallisen uusiutumisen varalta ja systeemisestä melanoomasta vastaavasta onkologista metastasoituneen taudin varalta, erityisesti alueellisen imusolmukkeiden tunnustelun ja sentinelisen imusolmukebiopsian avulla. Etäpesäkkeitä esiintyy aluksi preaurikulaarisissa tai submandibulaarisissa imusolmukkeissa, sitten myöhemmin keuhkoissa ja aivoissa. Uudet todisteet viittaavat siihen, että melanooman etäpesäke voisi olla herkkä BRAF-estäjille tai immuunitarkastusaseman estäjille.21, 22
sidekalvon kasvaimet käsittävät laajan kasvainten kirjon. Yleisimpiä maligniteetteja ovat OSSN, lymfooma ja melanooma. Klassisten kliinisten ominaisuuksien tunnistaminen, esiasteiden ymmärtäminen ja näiden maligniteettien nopea ja asianmukainen hoito ovat tärkeitä parhaan hoitotuloksen saavuttamiseksi.
Drs. Shields, Lally ja Shields työskentelevät Ocular Oncology Service-yksikössä Wills Eye Hospitalissa Thomas Jeffersonin yliopistossa Philadelphiassa. Tukea tarjoaa Eye Tumor Research Foundation, Philadelphia.
1. Shields CL, Chien JL, Surakiatchanukul T, et al. Sidekalvon kasvaimet: katsaus kliinisiin ominaisuuksiin, riskeihin, biomarkkereihin ja tuloksiin. J. Donald M. Gassin Luento 2017. Aasia PAC J Oftalmol. 2017;6:109-20.
2. Shields CL, Alset AE, Boal NS, et al. Sidekalvon kasvaimia 5002 tapauksessa. Hyvän-ja pahanlaatuisten verrokkien vertailuanalyysi. James D. Allenin Luento 2016. Am J Oftalmoli. 2017;173:106-33.
3. Kilvet CL, kilvet JA. Sidekalvon ja sarveiskalvon kasvaimet. Surv Ophthalmol. 2004;49:3-24.
4. Grossniklaus HE, Green WR, Luckenbach M, et al. Sidekalvon leesiot aikuisilla. Kliininen ja histopatologinen katsaus. Sarveiskalvo. 1987;6:78-116.
5. Shields CL, Sioufi K, Alset AE, et al. Sidekalvon kasvaimia lapsilla. Ominaisuudet erottaa hyvänlaatuisia pahanlaatuisia kasvaimia. Jama Ophthalmol. 2017;135:215-24.
6. Gichuhi s, Sagoo MS, Weiss HA, et al. Epidemiology of ocular surface squamous neoplasia in Africa. Trop Med Int Health. 2013;18:1424-43.
7. Shields CL, Ramasubramanian A, Mellen P, Shields JA. Immunosuppressiopotilailla (elinsiirto, ihmisen immuunikatovirusinfektio) esiintyvä sidekalvon okasolusyöpä. Silmätaudit. 2011;118:2133-7.
8. Amin MB, Edge S, Greene F, et al., toim. AJCC Cancer Staging Manual. 8.toim. Chicago; Springer International Publishing: 2017.
9. Shields JA, Shields CL, de Potter PV. Kirurginen lähestymistapa sidekalvon kasvaimiin. Lynn B. Mcmahanin Luento Vuodelta 1994. Arch Oftalmol. 1997;115:808-15.
10. Shields CL, Kaliki S, Kim Hj, et al. Interferonia käytetään silmän pinnan levyepiteeleihin 81 tapauksessa: tulokset perustuvat American Joint Committee on Cancer classification-komiteaan. Sarveiskalvo. 2013;32(3):248-56.
11. Karp CL, Galor A, Chhabra s, et al. Subjunktiivinen / perilesionaalinen rekombinantti interferoni A2B silmän pinnan levyepiteeleihin: 10-vuotiskatsaus. Silmätaudit. 2010;117(12):2241-6.
12. Kirkegaard MM, Rasmussen PK, Coupland SE, et al. Sidekalvon lymfooma-kansainvälinen monikeskustutkimus. Jama Ophthalmol. 2016;134:406-14.
13. Shields CL, Shields JA, Carvalho C, et al. Sidekalvon lymfoidikasvaimet: kliininen analyysi 117 tapauksesta ja suhde systeemiseen lymfoomaan. Silmätaudit. 2001;108:979-84.
14. Yu GP, Hu DN, McCormick S, Finger PT. Sidekalvomelanooma: Lisääntyykö se Yhdysvalloissa? Am J Oftalmoli. 2003;135:800-6.
15. Tuomaala S, Kivela T. kirjeenvaihto sidekalvomelanoomasta: lisääntyykö se Yhdysvalloissa? Am J Oftalmoli. 2003;136:1189-90.
16. Shields CL, Markowitz JS, Belinsky I, et al. Sidekalvomelanooma. Tulokset perustuvat kasvaimen alkuperää 382 peräkkäisissä tapauksissa. Silmätaudit. 2011;118:389-95.
17. Shields CL, Fasiuddin AF, Mashayekhi A, et al. Sidekalvon nevi: kliiniset piirteet ja luonnollinen kurssi 410 peräkkäisellä potilaalla. Arch Oftalmol. 2004;122:167-75.
18. Gerner N, Norregaard JC, Jensen OA, Prause JU. Sidekalvon naevi Tanskassa 1960-1980. 21 vuoden seurantatutkimus. Acta Oftalmol Scand. 1996;74:334-7.
19. Shields JA, Shields CL, Mashayekhi A, et al. Primaarinen hankittu sidekalvon melanoosi: melanooman etenemisriski 311 silmässä. Lorenz E. Zimmermanin luento vuodelta 2006. Silmätaudit. 2008;115:511-9.
20. Shields CL, Kaliki S, Al-Dahmash s, et al. American Joint Committee on Cancer (AJCC) Clinical Classification ennustaa sidekalvon melanooman tuloksia. Ophthalm Plast Reconstr Surg. 2012; 5:313-23.
21. Sagiv O, Thakar SD, Kandl TJ, et al. Immunoterapia ohjelmoidun solukuoleman kanssa 1 estäjä 5 potilaalle, joilla on sidekalvomelanooma. Jama Ophthalmol. 2018 marras 1; 136 (11): 1236-41.
22. Dalvin LA, Shields CL, Orloff M, et al. Checkpoint inhibitor immune therapy. Systeemiset käyttöaiheet ja oftalmiset haittavaikutukset. Verkkokalvo. 2018;6:1063-78.