rajat endokrinologiassa
- Johdanto
- Materials and Methods
- Trial Design and Participants’ Characteristics
- interventio
- tulosten arviointi
- lymfosyyttisolujen eristäminen
- RNA-uutto ja reaaliaikainen PCR (RT-PCR)
- otoskoko ja tilastolliset menetelmät
- tulokset
- Keskustelu
- kromin vaikutukset insuliinin ja lipidimetabolian Geeniekspressioon
- kromin vaikutukset Tulehdusmerkkiaineiden Geeniekspressioon
- tekijän osuus
- Rahoitus
- Eturistiriitalausunto
Johdanto
munasarjan monirakkulatauti (PCOS), lisääntymisikäisten naisten anovulaation ja hedelmättömyyden suurin syy, on yleisin endokriininen häiriö, jota esiintyy 5-10%: lla naisista maailmassa (1). Nopeutettuun lipolyysiin ja sitä seuraavaan DYSLIPIDEMIAAN PCOS-potilailla liittyy metabolisia poikkeavuuksia, kuten liikalihavuutta, insuliiniresistenssiä ja tyypin 2 diabetesta (T2DM) (2). Heijastuneet muutokset dominoivan follikkelin nesteessä (FF) (3, 4) voivat vaikuttaa suoraan munasolun laatuun ja metaboliaan. Matala-asteista kroonista tulehdusta pidetään yleisesti lapsettomuuden etiopathogeneettisenä mekanismina. Tulehdussytokiinit ovat huomattavasti yleisempiä selittämätöntä hedelmättömyyttä sairastavilla naisilla (5). Proinflammatoristen tekijöiden on osoitettu olevan merkittävästi yhteydessä suurempiin in vitro-hedelmöityksen (IVF) epäonnistumisasteisiin erityisesti implantaatiovaiheessa naisilla, joilla on selittämätöntä hedelmättömyyttä (6). Tutkimuksissa on havaittu kohonneita gamma-interferonin (IFN-γ) ja interleukiini-2: n (IL-2) tasoja ja alentuneita muuntavan kasvutekijän beetatasoja (TGF-β), joka on tärkeä endogeeninen anti-inflammatorinen välittäjä, (7) niiden naisten plasmassa, joilla on selittämätöntä hedelmättömyyttä verrattuna hedelmällisiin kontrolleihin implantaatioikkunan aikana (luteaalivaihe) (8). Lisäksi selittämättömillä hedelmättömillä potilailla on todettu kohonneita seerumin IL-2, IL-4, IL-6, IL-21, tuumorinekroositekijän alfan (TNF-α) ja IFN-γ: n pitoisuuksia verrattuna hedelmällisiin naisiin (5).
kromilisien suotuisia vaikutuksia on jo raportoitu PCOS-oireyhtymästä kärsivien naisten metabolisissa poikkeavuuksissa. Fazelin ym. tekemässä meta-analyysissä. (9) kromilisä vähensi seerumin insuliinia ja vapaata testosteronia ja paransi kehon painoa potilailla, joilla oli PCOS. Olemme jo julkaisseet edut Kromi täydentää 8 viikkoa glykeeminen ohjaus, cardiometabolic riskiparametrit, ja oksidatiivinen stressi hedelmättömillä naisilla PCOS jotka olivat ehdokas IVF (10). Lisäksi kromilisä diabetesrotilla osoitti diabeteslääkitystä, mikä voidaan selittää kromin vaikutuksella peroksisomiproliferaattorilla aktivoidun gamma-reseptorin (PPAR-γ), insuliinireseptorin substraatin 1 (IRS-1) ja ydintekijän KB (NF-kB) proteiinien modulaatioon (11). Samoin Wang et al. (12) todettiin, että verrattuna ylipainoisiin kontrollirottiin, niillä, joita täydennettiin kromia, oli merkittävä parannus glukoosin hävittämisnopeudessa ja nousu insuliinin stimuloimassa P-IRS-1: ssä ja fosfatidyylinositoli-3-kinaasiaktiivisuudessa luurankolihaksissa. Toisessa eläinkokeessa, jossa diabeettiset rotat söivät kromia 7 viikon ajan, tulehdusmerkkiaineet, kuten C-reaktiivinen proteiini (CRP), TNF-α ja IL-6 (13), vähenivät merkittävästi.
ottaen huomioon kromin (11, 14) diabeteslääkkeet ja lipidiarvoja alentavat vaikutukset, oletimme, että kromi-lisäravinteesta voi olla hyötyä naisille, joilla on PCOS ja IVF-ehdokas ja jotka kärsivät erilaisista metabolisista poikkeavuuksista. Parhaan tietämyksemme mukaan mitään ei ole julkaistu Kromi-lisäravinteen vaikutuksista insuliinin, lipidien ja tulehdusmerkkiaineiden geeniekspressioon hedelmättömillä naisilla, joilla oli PCOS ja jotka olivat ehdolla IVF: ään. Tämän tutkimuksen tarkoituksena oli selvittää kromilisän vaikutuksia insuliinin, lipidien ja tulehdusmerkkiaineiden geeniekspressioon hedelmättömillä naisilla, jotka kärsivät PCOS: stä ja olivat ehdolla IVF: ään.
Materials and Methods
Trial Design and Participants’ Characteristics
tämä satunnaistettu, kaksoissokkoutettu, lumekontrolloitu tutkimus rekisteröitiin Iranian website for clinical trials registration (http://www.irct.ir:IRCT20170513033941N32)-sivustolla. Mukana oli 40 lapsetonta naista, joilla oli PCOS, iältään 18-40 vuotta ja jotka olivat ehdolla IVF: ään ilman aikaisempaa IVF: ää. Tutkimus tehtiin taleghanin sairaalassa Teheranissa Iranissa helmi-toukokuussa 2018. Rotterdamin kriteerejä käytettiin PCOS-diagnoosin vahvistamiseen (15). Tutkimuksesta suljettiin pois osallistujat, joilla oli metabolisia häiriöitä, kuten kilpirauhasen toimintahäiriö, diabetes tai heikentynyt glukoosinsietokyky. Tutkimus tehtiin Helsingin julistuksen ja hyvän kliinisen käytännön ohjeiden mukaisesti, ja sen hyväksyi Teheranissa, Iranissa sijaitsevan Shahid Beheshti University of Medical Sciencesin (SUMMS) tutkimuseettinen komitea. Kirjallisen tietoon perustuvan suostumuksen allekirjoittivat kaikki henkilöt.
interventio
osallistujat jaettiin satunnaisesti interventioryhmiin ottamaan joko 200 µg/vrk kromipikolinaattia (Nature Made, Kalifornia, USA) (n = 20) tai lumelääkettä (Barij Essence, Kashan, Iran) (N = 20) 8 viikon ajan. Kromilisät ja placebot sopivat yhteen muodon, ulkonäön, hajun ja pakkauksen suhteen. Satunnaistaminen tehtiin tietokoneella luotujen satunnaislukujen avulla. Satunnaistaminen ja allokaatioprosessi salattiin sekä tutkijoilta että osallistujilta lopullisten analyysien loppuun asti. Toinen henkilö, joka ei ollut mukana tutkimuksessa ja tietämätön satunnaisista sekvensseistä, määräsi koehenkilöt numeroituihin tablettipurkkiin. Lisäravinteiden ja placebojen noudattamista seurattiin koko tutkimuksen ajan pyytäen ihmisiä tuomaan lääkepakkaukset takaisin. Noudattamisasteen nostamiseksi kaikki osallistujat saivat kännyköihinsä lyhyitä päivittäisiä muistutusviestejä lisäravinteiden ottamisesta. Tutkimukseen osallistuneet saivat valmiiksi ruokavaliotiedot Intervention viikoilla 0, 4 ja 8.
tulosten arviointi
seerumin korkean herkkyyden C-reaktiivisen proteiinin (hs-CRP) tasoja pidettiin ensisijaisena lopputuloksena ja metaboliaprofiileja mitattiin toissijaisina tuloksina. Paastoverinäytteet (15 mL) kerättiin 8 viikon toimenpiteen alussa ja lopussa Taleghanin sairaalassa (Teheran, Iran). Hs-CRP-tasot mitattiin käyttäen kaupallista ELISA-pakkausta (LDN, Nordhorn, Saksa), jonka määrityskertoimien väliset ja sisäiset varianssit (CVs) olivat alle 7 prosenttia. Typpioksidin (NO) pitoisuudet plasmassa mitattiin Griess-menetelmällä (16), ja määrityksen sisäinen CVs oli < 5%.
lymfosyyttisolujen eristäminen
verinäytteitä käytettiin lymfosyyttisolujen uuttamiseen käyttäen 50% percollia (Sigma-Aldrich, Dorset, UK). Solumäärä ja elinkelpoisuus testattiin käyttämällä trypan blue, RNA ja, DNA-uutto (17).
RNA-uutto ja reaaliaikainen PCR (RT-PCR)
RNA uutettiin verinäytteistä käyttäen rnx-plus kit-valmistetta (Cinnacolon, Teheran, Iran). RNA-suspensio jäädytettiin -20°C: ssa, kunnes saatiin cDNA. Kun jokaisesta näytteestä oli uutettu RNA: n kokonaismäärä, RNA määritettiin UV-spektrofotometrillä. Kukin näyte OD 260/280 suhde 1,7 – 2,1 ei aiheuttanut kontaminaatiota proteiinin eikä DNA: n kanssa (17). Moloneyn hiirileukemiaviruksen käänteiskopioijaentsyymin (RT) avulla eristetty RNA kirjattiin käänteiskopioijaentsyyminä cDNA-kirjastoon. PPAR-γ: n, glukoosin kuljettajaproteiini 1: n (GLUT-1), low-density lipoproteiinireseptorin (LDLR), IL-1: n, IL-8: n, TNF-α: n, TGF-β: n ja verisuonten endoteelikasvutekijän (VEGF) geeniekspressiot tehtiin perifeerisen veren mononukleaarisoluilla (PBMC) käyttäen SYBR green detection and Amplikon Kit-ohjelmaa ja soveltamalla kvantitatiivista RT-PCR-ja Light Cycler-teknologiaa (Roche Diagnostics, Rotkreuz, Sveitsi) (Taulukko 1). Glyseraldehydi-3-fosfaattidehydrogenaasi (GAPDH) alukkeita käytettiin kodinhoitogeeninä. Alukkeet suunniteltiin käyttäen Primer Express-ohjelmistoa (Applied Biosystems, Foster City, USA) ja Beacon designer-ohjelmistoa (Takaposizt, Teheran, Iran). Suhteelliset transkriptiotasot laskettiin käyttäen Pffafi – tai 2-ΔΔCT-menetelmiä.

Taulukko 1. Erityiset alukkeet, joita käytetään reaaliaikaisessa kvantitatiivisessa PCR: ssä.
otoskoko ja tilastolliset menetelmät
otoskoko laskettiin käyttäen RCTs: lle vahvistettua kaavaa, jossa tyypin yksi (α) ja tyypin kaksi virhettä (β) pidettiin arvoina 0, 05 ja 0.20 antaa 80 prosentin tehon. Aiemmin julkaistun tutkimuksen (18) perusteella hs-CRP: n keskimääräinen ero (D) oli 1500, 0 ng/mL ja keskihajonta (SD) 1496, 1 ng/mL. Kun otetaan huomioon 4 tutkimushenkilön todennäköinen keskeyttäminen kussakin interventioryhmässä, lopulliseksi otoskooksi määritettiin 20 (16 + 4) tutkimushenkilöä ryhmää kohti.
tietojen normaalius arvioitiin Kolmogorov-Smirnov-testillä. Analyysit tehtiin intention-to-treat (ITT) – menetelmällä. Riippumattomien näytteiden t-testiä käytettiin määrittämään antropometristen mittausten ja insuliinin, lipidin ja tulehduksen geeniekspression erot interventioryhmien välillä. Kromilisän vaikutuksia tulehdusmerkkiaineisiin arvioitiin toistuvilla ANOVA-testeillä. Mittasuhteiden eroja arvioitiin Fisherin tarkalla testillä. P < 0, 05: tä pidettiin tilastollisesti merkitsevänä. Tilastoanalyysit tehtiin Yhteiskuntatieteiden tilastopaketin versiolla 18(SPSS Inc., Chicago, Illinois, Yhdysvallat).
tulokset
kussakin interventioryhmässä raportoitiin kolme keskeyttämistä henkilökohtaisista syistä. Tutkimukseen osallistui siis yhteensä 34 henkilöä (Kuva 1). ITT-lähestymistapaa käyttäen kaikki 40 osallistujaa (20 kussakin ryhmässä) otettiin mukaan lopulliseen data-analyysiin. Tässä tutkimuksessa noudattamisaste oli korkea, ja yli 90 prosenttia tableteista kului intervention aikana molemmissa ryhmissä. Tässä tutkimuksessa PCOS: ää sairastavilla naisilla ei raportoitu kromin nauttimisen jälkeen haittavaikutuksia.

Kuva 1. Yhteenveto potilaan vuokaaviosta.
Antropometrisissä mitoissa ei ollut tilastollisesti eroa interventioryhmien välillä (Taulukko 2). Lisäksi Kromi-lisäyksen jälkeen IVF-tulokset, mukaan lukien kohdun limakalvon paksuus, haettujen varhaismunasolujen määrä, hedelmöittyneiden varhaismunasolujen määrä, hedelmöitysnopeus, raskausaste ja alkion määrä, eivät poikenneet merkitsevästi täydennetyn ja lumelääkeryhmän välillä.

Taulukko 2. Tutkimukseen osallistuneiden yleiset ominaisuudet.
makro – ja mikroravinteiden saantien keskiarvo ei myöskään eronnut merkittävästi kahden interventioryhmän välillä koko käsittelyn ajan (Tietoja ei näy).

Taulukko 3. Tulehdusmerkkiaineet lähtötilanteessa ja 8 viikon intervention jälkeen hedelmättömässä munasarjojen monirakkulatautioireyhtymässä naiset, jotka saivat joko kromilisää tai lumelääkettä koeputkihedelmöitykseen.
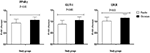
kuva 2. PPAR-γ: n, GLUT-1: n ja ldlr: n geeniekspressiotasojen kertamuutos (±SDS) naisilla, joilla on diagnosoitu munasarjojen monirakkulatauti ja jotka olivat ehdolla koeputkihedelmöitykseen ja saivat kromilisää ja lumelääkettä. P-arvo saatiin riippumattomasta t-testistä. N = 20 kussakin ryhmässä. IL-1, interleukiini-1; IL-8, interleukiini-8; ldlr, hapettunut pienitiheyksinen lipoproteiinireseptori; PPAR-γ, peroksisomiproliferaattorin aktivoima gammareseptori; TNF-α, tuumorinekroositekijä alfa; TGF-β, muuntava kasvutekijä beeta; VEGF, verisuonten endoteelikasvutekijä.
Kromilisäys vähensi myös IL-1: n (p = 0, 004) geeniekspressiota PBMCs: ssä verrattuna lumelääkkeeseen (kuva 3). Kromilisäyksellä ei ollut merkittävää vaikutusta IL-8: n, TNF-α: n, TGF-β: n ja VEGF: n geeniekspressioon PCOS-potilaiden Pbmc: issä.
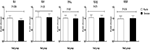
kuva 3. Muutos IL-1: n, IL-8: n, TNF-α: n, TGF-β: n ja VEGF: n geeniekspressiotasoissa naisilla, joilla on diagnosoitu munasarjojen monirakkulatauti ja jotka olivat ehdolla koeputkihedelmöitykseen ja saivat kromilisää ja lumelääkettä. P-arvo saatiin riippumattomasta t-testistä. N = 20 kussakin ryhmässä. IL-1, interleukiini-1; IL-8, interleukiini-8; ldlr, hapettunut pienitiheyksinen lipoproteiinireseptori; PPAR-γ, peroksisomiproliferaattorin aktivoima gammareseptori; TNF-α, tuumorinekroositekijä alfa; TGF-β, muuntava kasvutekijä beeta; VEGF, verisuonten endoteelikasvutekijä.
Keskustelu
löysimme suotuisia vaikutuksia kromin antamisesta 8 viikon ajan hedelmättömillä naisilla, joilla oli PCOS ja jotka olivat ehdolla IVF: ään. Kromilisä vähensi tulehdusta ja paransi PPAR-γ: n, GLUT-1: n, LDLR: n ja IL-1: n geeniekspressiota, vaikka se ei vaikuttanut IL-8: n, TNF-α: n, TGF-β: n ja VEGF: n geeniekspressioon. Parhaan tietämyksemme mukaan tämä on ensimmäinen tutkimus, jossa raportoidaan Kromi-lisäravinteen vaikutuksista insuliinin, lipidien ja tulehdusmarkkereiden geeniekspressioon hedelmättömillä naisilla, joilla on diagnosoitu PCOS ja IVF-ehdokas.
kromin vaikutukset insuliinin ja lipidimetabolian Geeniekspressioon
PCOS-potilaat ovat alttiita erilaisille metabolisille poikkeavuuksille, kuten lisääntyneelle insuliiniresistenssille, dyslipidemialle ja krooniselle tulehdukselle (19, 20). Nykyinen tutkimus osoitti, että kromilisä 8 viikon ajan hedelmättömille naisille, joilla oli PCOS ja jotka olivat ehdolla IVF: ään, lisäsi merkittävästi PPAR-γ: n, GLUT-1: n ja LDLR: n geeniekspressiota. Sopusoinnussa havaintojemme kanssa, kromin antaminen diabeettisille rotille osoitti anti-diabeettista toimintaa, joka todennäköisesti liittyy kromin vaikutukseen PPAR-γ-ja IRS-1-proteiinien modulaatioon (11). Wang ym. (12) havaitsi myös, että ylipainoiset rotat, joihin oli lisätty kromia, lisäsivät merkittävästi glukoosin hävittämisnopeuttaan. Lisäksi näillä rotilla havaittiin suurentuneita insuliinin stimuloimia p-IRS-1-ja fosfatidyyli-inositoli-3-kinaasiaktiivisuuksia luurankolihaksissa verrattuna ylipainoisiin verrokkeihin. Toisessa tutkimuksessa Kromi, biotiini tai niiden yhdistelmä sääteli merkittävästi PPAR-γ-ilmentymistä rasvakudoksessa, millä saattaa olla tehokas insuliiniherkistävä vaikutus ja vähentää insuliiniresistenssiä diabeettisessa rottamallissa (11). Kromi voi myös edistää GLUT-4: n kauppaa ja insuliinin stimuloimaa glukoosin kuljetusta (21). Samoin niillä rotilla, joilla oli diabeettinen retinopatia ja joita täydennettiin kromilla 12 viikon ajan, glut-1: n, GLUT-3: n ja insuliinin (22) geeniekspressio parani. PPAR-γ on insuliini -, glukoosi-ja rasva-aineenvaihdunnan keskeinen säätelijä, jota esiintyy laajalti rasvakudoksessa. PPAR-γ saattaa parantaa insuliiniherkkyyttä ja lipidiprofiileja tyypin 2 diabetesta sairastavilla potilailla sekä diabeettisissa jyrsijämalleissa (23). Tämänhetkinen näyttö viittaa siihen, että PPAR-γ-agonisteista voi olla hyötyä munuaiskuoren lipidien ja proteinurian vähentämisessä niiden hypoglykeemisesta vaikutuksesta riippumattoman mekanismin avulla (24, 25).
kromin vaikutukset Tulehdusmerkkiaineiden Geeniekspressioon
Tutkimuksemme tuki sitä, että kromin anto 8 viikon ajan vähensi merkittävästi IL-1: n ja seerumin hs-CRP-pitoisuuksien geeniekspressiota lapsettomilla naisilla, joilla oli PCOS ja jotka olivat ehdolla IVF-hoitoon, vaikka se ei vaikuttanut IL-8: n, TNF-α: n, TGF-β: n ja VEGF: n geeniekspressioon. Nykyiset todisteet, jotka osoittavat kromilisän vaikutukset tulehdusmerkkiaineiden geeniekspressioon ja niiden verenkierrossa oleviin pitoisuuksiin, ovat vähäiset ja rajoittuvat enimmäkseen eläinkokeisiin. Kromi täydentää 8 viikon ajan Zucker diabeettinen rasva (ZDF) rotat merkittävästi laski seerumin CRP tasot (26). Toisessa tutkimuksessa Kromi-niasinaatin nauttiminen 7 viikon ajan vähensi proinflammatorisia sytokiinipitoisuuksia (TNF-α, IL-6 ja CRP), oksidatiivista stressiä ja lipidipitoisuuksia diabeetikkorotilla (13). Lisäksi kromipikolinaattia, fosfatidyyliseriiniä, dokosaheksaeenihappoa ja booria sisältävän ravintolisän antaminen 12 viikon ajan vähensi CRP: n ja TNF-α: n pitoisuuksia merkittävästi rotilla, joita ruokittiin runsasrasvaisella ruokavaliolla (27). Emme löytäneet merkittävää vaikutusta Kromi täydentää IL-8, TNF-α, TGF-β, ja VEGF, joka voitaisiin selittää soveltamalla erilaisia tutkimus malleja, tyyppi ja annokset Kromi käytetty, kesto intervention ja osallistujien ominaisuudet. Suuremmat Kromi-annokset voivat merkittävästi parantaa metaboliaprofiileja, mukaan lukien IL-8, TNF-α, TGF-β ja VEGF. Tulehduksen ja oksidatiivisen stressin merkkiaineet ovat koholla monilla diabeetikoilla, mikä kuvaa positiivisesti verisuonitulehdusta (28). Insuliiniresistenssi ja sitä seuraava verisuonitulehdus ovat tärkeimmät riskitekijät CVD: n kehittymiselle (29). Kromin tulehdusta edistäviä markkereita vaimentavaa vaikutusta voidaan helpottaa inaktivoimalla oksidatiivisia stressireittejä ja vähentämällä Akt-fosforylaatiota, joka liittyy insuliiniresistenssikaskadiin maksassa (30). Tämänhetkinen näyttö on osoittanut, että lisääntyneet tulehdukselliset sytokiinit ovat mukana IVF: n tuloksissa. Haimovici et al: n tekemässä tutkimuksessa. (31) sikiönsä elävinä synnyttäneillä naisilla IL-6-tasot olivat matalammat. Progesteronia tuottavien luteaalisolujen inhibitio il-1β: n läsnä ollessa voi olla yksi implantaation epäonnistumiseen johtavista tekijöistä (32). Follikkelien TNF-α ja IL-6 lisääntyminen saattavat heikentää follikkelin mikroympäristöä ja siten vaikuttaa negatiivisesti munasolun ja alkion laatuun (33). Toisessa tutkimuksessa johti Levin et al. (34), korkeammat CRP-tasot IVF-stimulaation aikana liittyivät merkittävästi hedelmöityksen epäonnistumiseen. Edellä mainitun julkaistun todistusaineiston mukaan oletimme, että IVF: n tuloksiin voi vaikuttaa alentunut tulehdus. Tuore tutkimus osoitti, että TNF-α-inhibiittorin ja laskimonsisäisen immunoglobuliinin käyttö paransi merkittävästi IVF: n tuloksia mm.; implantaatio, kliininen raskaus ja elävänä syntyvyys nuorilla hedelmättömillä naisilla, joilla oli korkea T-auttaja 1/T-auttaja 2-sytokiinipitoisuus (35).
tässä tutkimuksessa oli muutamia rajoituksia. Puutteellisen rahoituksen vuoksi emme pystyneet mittaamaan kromipitoisuuksia emmekä arvioimaan kromin vaikutuksia oksidatiivisen stressin geeniekspressioon.
kaiken kaikkiaan tutkimuksemme viittaa siihen, että kromi-lisäravinteen edut alentavat tulehdusmerkkiaineita parantamalla PPAR-γ: n, GLUT-1: n, LDLR: n ja IL-1in: n geeniekspressiota hedelmättömillä naisilla, joilla oli PCOS ja jotka olivat ehdolla IVF: ään.
tekijän osuus
ZA auttoi käsikirjoituksen suunnittelussa, suunnittelussa ja tilastollisessa analyysissä. MA, SZ, NM, EA ja SS osallistuivat tiedonkeruuseen ja käsikirjoitusten laatimiseen. ZA valvoi tutkimusta.
Rahoitus
tätä tutkimusta tukivat tutkimuksen varakansleri, Shahid Beheshti University of Medical Sciences, ja Teheran, Iran.
Eturistiriitalausunto
kirjoittajat toteavat, että tutkimus tehtiin ilman kaupallisia tai taloudellisia suhteita, joita voitaisiin pitää mahdollisena eturistiriitana.
1. Yildiz BO, Bozdag G, Yapici Z, Esinler I, Yarali H. prevalenssi, fenotyyppi ja kardiometabolinen munasarjojen monirakkulatautioireyhtymän riski eri diagnostisilla kriteereillä. Hum Reprod. (2012) 27:3067–73. doi: 10.1093 / humrep / des232
PubMed Abstract / CrossRef Full Text | Google Scholar
2. Amato G, Conte M, Mazziotti G, Lalli E, Vitolo G, Tucker AT, et al. Seerumin ja follikulaarisen nesteen sytokiinit munasarjojen monirakkulatautioireyhtymässä stimuloitujen syklien aikana. Obstet Gynecol. (2003) 101:1177–82.
PubMed Abstract / Google Scholar
3. Valckx SD, Arias-Alvarez M, De Pauw I, Fievez V, Vlaeminck B, Fransen e, et al. Fatty acid composition of the follikulary fluid of normal weight, ylipainoinen and obese women get assisted Reproduction treatment: a descriptive cross-sectional study. Reprod Biol Endocrinol. (2014) 12:13. doi: 10.1186/1477-7827-12-13
PubMed Abstrakti / CrossRef Kokoteksti / Google Scholar
4. Valckx SD, de Pauw I, de Neubourg D, Inion I, laituri M, Fransen e, et al. BMI: hen liittyvä avusteisia lisääntymishoitoja saavien naisten follikulaarisen nesteen metabolinen koostumus ja munasolujen ja alkion laatuun kohdistuvat seuraukset. Hum Reprod. (2012) 27:3531–9. doi: 10.1093 / humrep / des350
PubMed Abstract / CrossRef Full Text | Google Scholar
7. Letterio JJ, Roberts AB. TGF-beetan immuunivasteen säätely. Annu Rev. Immunol. (1998) 16:137–61
PubMed Abstract | Google Scholar
8. Fornari MC, Sarto A, Berardi VE, Martinez MA, Rocha MG, Pasqualini S, et al. Effect of ovaric hyper-stimulation on blood lymphocyte subpopulations, cytokines, leptin and nitrite among patients with unexplained infertility. Am J Reprod Immunol. (2002) 48:394–403.
PubMed Abstract | Google Scholar
10. Jamilian M, Zadeh Modarres S, Amiri Siavashani M, Karimi M, Mafi A, Ostadmohammadi V, et al. Vaikutukset Kromi lisäravinteen glykeeminen ohjaus, markkereita sydän-metabolisen riskin, ja oksidatiivista stressiä hedelmätön munasarjojen monirakkulatauti naiset candidate for in vitro lannoitus: satunnaistettu, kaksoissokkoutettu, lumekontrolloitu tutkimus. Biol Trace Elem Res. (2018): 48-55. doi: 10.1007 / s12011-017-1236-3
PubMed Abstrakti / CrossRef kokoteksti / Google Scholar
11. Sahin K, Tuzcu M, Orhan C, Sahin N, Kucuk O, Ozercan IH, et al. Anti-diabeettinen aktiivisuus kromipikolinaattia ja biotiinia rotilla tyypin 2 diabetes aiheuttama rasvainen ruokavalio ja streptotsotosiini. BRJ Nutr. (2013) 110:197–205. doi: 10.1017 / S0007114512004850
PubMed Abstract / CrossRef Full Text | Google Scholar
13. Jain SK, Rains JL, Croad JL. Kromi-niasinaatin ja kromipikolinaattilisän vaikutus lipidiperoksidaatioon, TNF-Alfaan, IL-6: een, CRP: hen, glykoloituneeseen hemoglobiiniin, triglyserideihin ja kolesterolitasoihin streptotsotosiinilla hoidettujen diabeettisten rottien veressä. Ilmainen Radic Biol Med. (2007) 43:1124–31. doi: 10.1016 / J. freeradbiomed.2007.05.019
PubMed Abstract | CrossRef Full Text | Google Scholar
14. Martino F, Puddu PE, Pannarale G, Colantoni C, Martino E, Niglio T, et al. Pieniannoksinen Kromi-polynikotinaatti tai policosanol tehoaa hyperkolesteroleemisiin lapsiin vain yhdessä glukomannaanin kanssa. Ateroskleroosi. (2013) 228:198–202. doi: 10.1016/j.ateroskleroosi.2013.02.005
PubMed Abstract | CrossRef Full Text | Google Scholar
15. Rotterdam ESHRE / ASRM sponsoroima PCOS Consensus Workshop Group. Tarkistettu vuoden 2003 konsensus munasarjojen monirakkulatautiin liittyvistä diagnostisista kriteereistä ja pitkän aikavälin terveysriskeistä. Fertil Steril. (2004) 81:19–25.
Google Scholar
17. Dunkley PR, Jarvie PE, Robinson PJ. Nopea percoll gradienttimenettely synaptosomien valmistamiseksi. Nat-Protokolla. (2008) 3:1718–28. doi: 10.1038 / nprot.2008.171
PubMed Abstract | CrossRef Full Text | Google Scholar
18. Jamilian M, Bahmani F, Siavashani MA, Mazloomi M, Asemi Z, Esmaillzadeh A. The Effects of Kromi supplementation on endocrine profiles, Biomarkers of inflammation, and oxidative stress in women with polycystic ovary syndrome: a randomized, double-Block, placebo-controlled trial. Biol Trace Elem Res. (2016) 172:72-8. doi: 10.1007 / s12011-015-0570-6
PubMed Abstrakti / CrossRef kokoteksti / Google Scholar
19. Asemi Z, Foroozanfard F, Hashemi T, Bahmani F, Jamilian M, Esmaillzadeh A. Kalsium – ja D-vitamiinilisä vaikuttaa glukoosiaineenvaihduntaan ja lipidipitoisuuksiin ylipainoisilla ja lihavilla naisilla, joilla on munasarjojen monirakkulatauti. Clin Nutr. (2015) 34:586–92. doi: 10.1016 / J.clnu.2014.09.015
PubMed Abstract | CrossRef Full Text | Google Scholar
20. Foroozanfard F, Jamilian M, Bahmani F, Talaee R, Talaee N, Hashemi T, et al. Kalsium plus D-vitamiinilisä vaikuttaa tulehduksen ja oksidatiivisen stressin biomarkkereihin ylipainoisilla ja D-vitamiinipuutteisilla naisilla, joilla on munasarjojen monirakkulatauti: satunnaistettu kaksoissokkoutettu lumekontrolloitu kliininen tutkimus. Clin Endocrinol. (2015) 83:888–94. doi: 10.1111 / cen.12840
PubMed Abstract | CrossRef Full Text | Google Scholar
21. Chen G, Liu P, Pattar GR, Tackett L, Bhonagiri P, Strawbridge AB, et al. Kromi aktivoi glukoosin kuljettajaproteiini 4: n salakuljetuksen ja lisää insuliinin stimuloimaa glukoosin kuljetusta 3T3-L1-adiposyyteissä kolesterolista riippuvaisen mekanismin kautta. Mol Endokrinoli. (2006) 20:857–70. doi: 10,1210 / me.2005-0255
PubMed Abstract | CrossRef Full Text | Google Scholar
24. Benigni a, Zoja C, Campana M, Corna D, Sangalli F, Rottoli D, et al. TGFbeta-antagonismin suotuisa vaikutus diabeettisen nefropatian hoidossa riippuu hoidon aloittamisajankohdasta. Nefron Exp Nefroli. (2006) 104:e158–68. doi: 10.1159/000094967
PubMed Abstrakti / CrossRef kokoteksti / Google Scholar
25. Bobulescu IA. Munuaisten rasva-aineenvaihdunta ja lipotoksisuus. Curr Opin Nefrol Hypertens. (2010) 19:393–402. doi: 10.1097 / MNH.0b013e32833aa4ac
PubMed Abstract | CrossRef Full Text | Google Scholar
26. Jain SK, Croad JL, Velusamy T, Rains JL, Bull R. Kromi-dinikokysteinaattilisä voi alentaa verensokeria, CRP, MCP-1, ICAM-1, kreatiniini, ilmeisesti välittämä kohonnut veren C-vitamiini ja adiponektiini ja esto nfkappab, Akt, ja Glut-2 maksoissa Zucker diabeettinen rasva rotilla. Mol Nutr Food Res. (2010) 54:1371-80. doi: 10.1002 / mnfr.200900177
PubMed Abstract | CrossRef Full Text | Google Scholar
27. Sahin N, Akdemir F, Orhan C, Aslan A, Agca CA, Gencoglu H, et al. A novel nutritional supplement containing chromium picolinate, phosphatidylserine, docosahexaenoic acid, and boron activates the antioxidant pathway Nrf2/HO-1 and protects the brain against oxidative stress in high-fat-fed rats. Nutr Neurosci. (2012) 15:42–7. doi: 10.1179/1476830512Y.0000000018
PubMed Abstract | CrossRef Full Text | Google Scholar
31. Haimovici F, Anderson JL, Bates GW, Racowsky C, Ginsburg ES, Simovici D, et al. Hedelmättömillä pareilla molempien osapuolten stressi, ahdistus ja masennus ovat yhteydessä sytokiinitasoihin ja haitalliseen IVF-tulokseen. Am J Reprod Immunol. (2018) 79:e12832. doi: 10.1111 / aji.12832
PubMed Abstract | CrossRef Full Text | Google Scholar
32. Wang XF, Xing FQ, Chen SL. Interleukiini-1beta ilmentyy munasarjojen granulosasoluissa ja sen kliinisistä vaikutuksista naisilla, joille tehdään koeputkihedelmöitys. Di Yi Jun Yi Da Xue Xue Bao. (2002) 22:934–6.
PubMed Abstract / Google Scholar
33. Wunder DM, Mueller MD, Birkhauser MH, Bersinger NA. Lisääntynyt ena-78-pitoisuus endometrioosipotilaiden follikulaarisessa nesteessä. Acta Obstet Gynecol Scand. (2006) 85:336–42. doi: 10.1080/00016340500501715
PubMed Abstract | CrossRef Full Text / Google Scholar