12.4: párolgás és páralecsapódás
párolgás
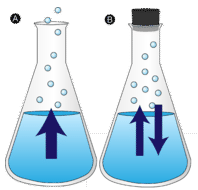
a tócsa a víz maradt zavartalan végül eltűnik. A folyékony molekulák a gázfázisba kerülnek, vízgőzré válnak. A párolgás az a folyamat, amelyben a folyadék gázzá alakul. A párolgás a folyadék gőzré történő átalakulása a folyadék forráspontja alatt. Ha a vizet ehelyett zárt tartályban tartják, akkor a vízgőzmolekuláknak nincs esélyük a környezetbe menekülni, így a vízszint nem változik. Amint egyes vízmolekulák gőzzé válnak, azonos számú vízgőzmolekula kondenzálódik vissza folyékony állapotba. A kondenzáció az állapot változása gázról folyadékra.
ahhoz, hogy egy folyékony molekula gázállapotba kerüljön, a molekulának elegendő kinetikus energiával kell rendelkeznie ahhoz, hogy legyőzze a folyadékban lévő intermolekuláris vonzó erőket. Emlékezzünk arra, hogy egy adott folyékony mintának kinetikus energiák széles skálájával rendelkező molekulái lesznek. Azok a folyékony molekulák, amelyek rendelkeznek ezzel a bizonyos küszöbértékű kinetikus energiával, elhagyják a felületet, és gőzré válnak. Ennek eredményeként a megmaradt folyékony molekulák mozgási energiája alacsonyabb. A párolgás során a maradék folyadék hőmérséklete csökken. Megfigyelte a párolgási hűtés hatásait. Egy forró napon az izzadságban lévő vízmolekulák elnyelik a testhőt, és elpárolognak a bőr felszínéről. A párolgási folyamat elhagyja a fennmaradó izzadási hűtőt, amely viszont több hőt szív fel a testéből.
egy adott folyadék gyorsabban elpárolog, ha felmelegszik. Ennek oka az, hogy a fűtési folyamat azt eredményezi, hogy a folyadék molekuláinak nagyobb része rendelkezik a szükséges kinetikus energiával a folyadék felszínének elkerüléséhez. Az alábbi ábra a folyékony molekulák kinetikus energiaeloszlását mutatja két hőmérsékleten. Az elpárologtatáshoz szükséges kinetikus energiával rendelkező molekulák számát A jobb oldali görbe alatti árnyékolt területen mutatjuk be. A magasabb hőmérsékletű folyadék \(\bal (T_2 \ jobb)\) több molekulával rendelkezik, amelyek képesek a gőzfázisba menekülni, mint az alacsonyabb hőmérsékletű folyadék \(\bal( T_1 \jobb)\).
a 29.029 láb \(\balra( 8848 \: \text{m} \right)\), a Mount Everest a Himalája tartományban a határ Kína és Nepál a legmagasabb pont a földön. Magassága számos gyakorlati problémát jelent a hegymászók számára. A levegő oxigéntartalma jóval alacsonyabb, mint a tengerszinten, ezért oxigéntartályokat kell magával vinni (bár néhány hegymászó oxigén nélkül érte el a csúcsot). Egy másik probléma az, hogy forrásban lévő víz szakács étel. Bár a víz \(100^\text{o} \text{C}\) tengerszint feletti magasságban forr, a forráspont a Mount Everest tetején csak körülbelül \(70^\text{o} \text{C}\). Ez a különbség nagyon megnehezíti egy tisztességes csésze tea beszerzését (ami határozottan frusztrálta a brit hegymászókat).