7.5: komplex IV
komplex IV az elektrontranszport lánc végső rendeltetési helye. Itt az elektronok, amelyek a légzőszervi szuperkomplex többi tagján keresztül haladtak, végül az O2-be kerülnek, vízzel redukálva. Ez lenyűgöző teljesítmény, mivel számos reaktív oxigénfajnak kell kialakulnia az elektron kezdeti hozzáadása és a víz végső felszabadulása között, de a reakciót úgy szabályozzák, hogy a sejtkárosodás lehetősége minimálisra csökkenjen. Ugyanakkor több protont pumpálnak át a belső mitokondriális membránon.
- a komplex IV-ben az elektronokat végső rendeltetési helyükre, egy O2 molekulába szállítják.
- az O2 vízre redukálódik.
gyakorlat \(\PageIndex{1}\)
írjon egy kiegyensúlyozott redox félreakciót, hogy megmutassa, hány elektronra van szükség az oxigénmolekula vízre redukálásához.
válasz
O2 + 4e -+ 9054>
O2 2 H2O (o kiegyensúlyozott)
O2 + 4o + 2 H2O (kiegyensúlyozott töltés)
O2+ 4e – + 4o + 2 H2O (kiegyensúlyozott töltés))
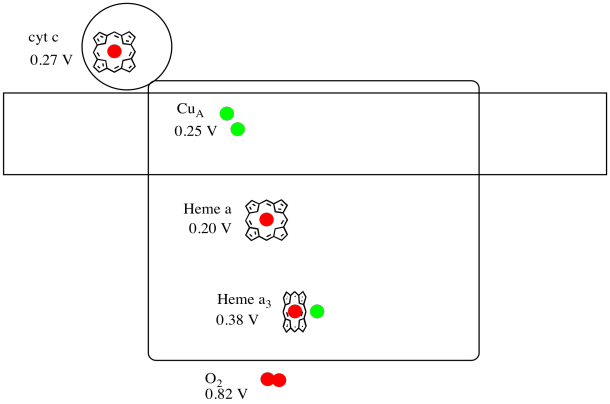
a komplex IV Röntgenszerkezetét az alábbiakban mutatjuk be. Ismét a mátrix a kép alsó végén, az intermembrán tér pedig a tetején van. Ez az, ahol a citokróm c dokkok, a tetején.
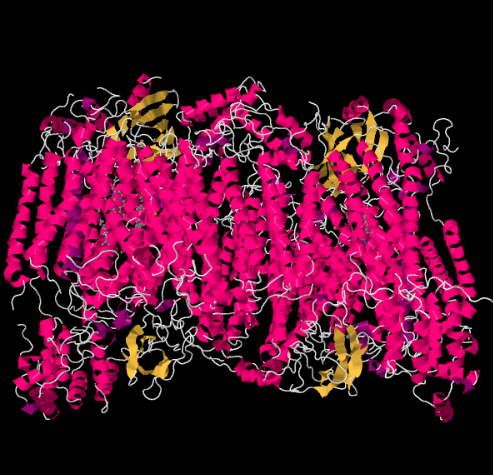
a mobil elektron hordozó, a citokróm c, a komplex IV-ben kötődik, és egy elektront szállít a CuA nevű kétmagos réz helyre. Láthatjuk, hogy a binukleáris réz hely, amikor belenézünk a fehérje, lent. Csak a fehérjéhez kötődik, semmi máshoz, így csak a kép tetején látjuk a két réziont. Ez a rézatompár továbbítja az elektront egy hemnek, a citokróm A-nak, amelyet alább és balra láthat. Innen az elektron egy másik binukleáris klaszterbe jut, amely ezúttal egy hemhez kötött vasból (citokróm a3) és egy közeli rézből (CuB) áll. Ez a binukleáris hely a dioxigén vízre redukálását végzi. A szerkezetben a citokróm A3 és a CuB közötti aktív helyen szén-monoxid molekula van kötve. A szénatomok a vashoz, az oxigén pedig a rézhez kapcsolódnak. Ez az a hely, ahol az oxigén molekula kötődik, várva, hogy csökken a víz.
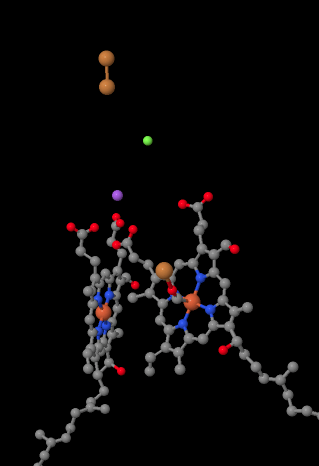
ha erre gondolsz, ez azt jelenti, hogy az elektronok az ellenkező irányba haladnak, mint amit az első három komplexben láttunk. Az I. és II. komplexekben az elektronok a mitokondriális mátrixból érkeztek, és az intermembrán tér felé haladtak, megállva a mitokondriális membrán ubiquinonjánál. Komplexben az elektronok abban a “felfelé” irányban folytatódtak, a mitokondriális membrántól a citokróm c-ig az intermembrán térben. Komplexben IV, az elektronok megfordulnak, visszafelé haladva a mitokondriális mátrix felé. Ne feledje, hogy a mitokondriális mátrix n-adalékolt a protonpumpálás miatt, tehát ezek az elektronok a membrán pozitív oldaláról a negatív oldalra haladnak. Nehéz lehet.
- a IV komplexben az elektrontranszport ellentétes irányban van a többi komplextől.
- az elektronok az intermembrán tér oldaláról a mitokondriális mátrix oldalára haladnak a töltési gradiens ellen.
vessünk egy pillantást a komplex fontos ligandumaira. Az alábbiakban egy rajzfilm látható. A rajzfilmben az O2 molekula ebben a helyzetben kötődik az A3 hem és a CuB között. Ez a dinukleáris fémhely az, ahol az oxigénmolekula vízzé redukálódik.
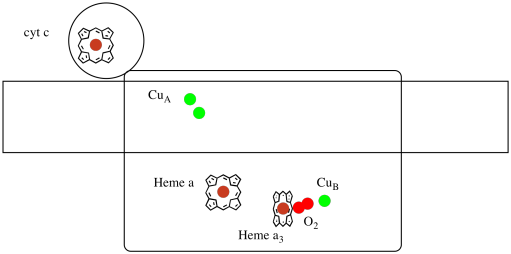
mivel négy elektronra van szükség az O csökkentéséhez2 H2O-ra, négy citokróm C molekulának meg kell kötődnie a komplex IV-nél, mielőtt ez a redukció folytatódhat. Valószínű, hogy az oxigénmolekula koordinációs környezete-két fém között, nem csak egyhez kötve-lehetővé teszi, hogy gyorsabban redukálódjon egészen a vízig, ahelyett, hogy reaktív oxigénfajokat képezne, amelyek megmaradnak a sejtben, mint például a peroxidok.
gyakorlat \(\PageIndex{2}\)
tegyük fel, hogy az A3 hemben lévő vas csökkentett Fe(II) állapotban, a CuB pedig csökkentett Cu(I) állapotban kezdődik. Biztosítson egy mechanizmust az oxigén vízzel való redukciójára, négy elektron és négy proton hozzáadásával. Használja az FE (II) – t elektron donorként, a lizint pedig proton donorként.
válasz
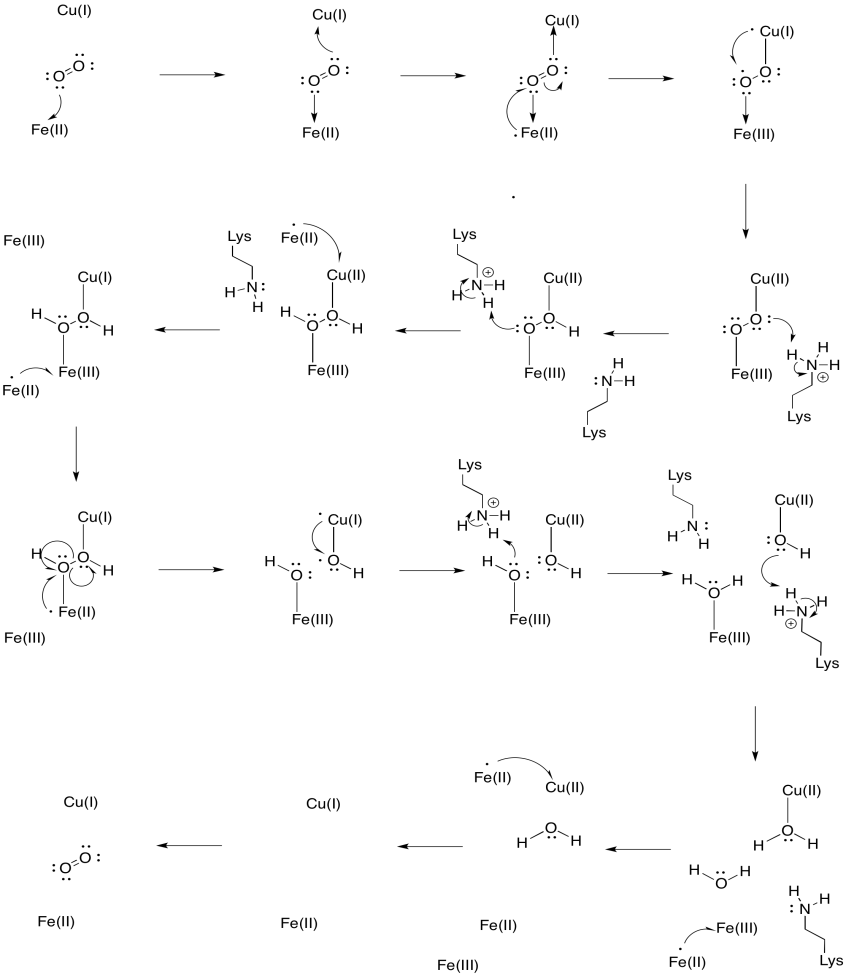
e két fém mellett van egy módosított hisztidin-tirozin konjugátum is, amely a CuB-hoz kötődik. Felvetődött, hogy ez a tirozin Az azonnali elektronok másik forrását biztosítja, amelyet redukcióban lehet felhasználni.
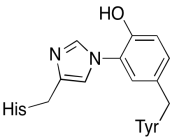
gyakorlat \(\PageIndex{3}\)
mutassa be, hogy a tirozin miért lehet mind a proton, mind az elektron forrása a biokémiai folyamatokban.
válasz
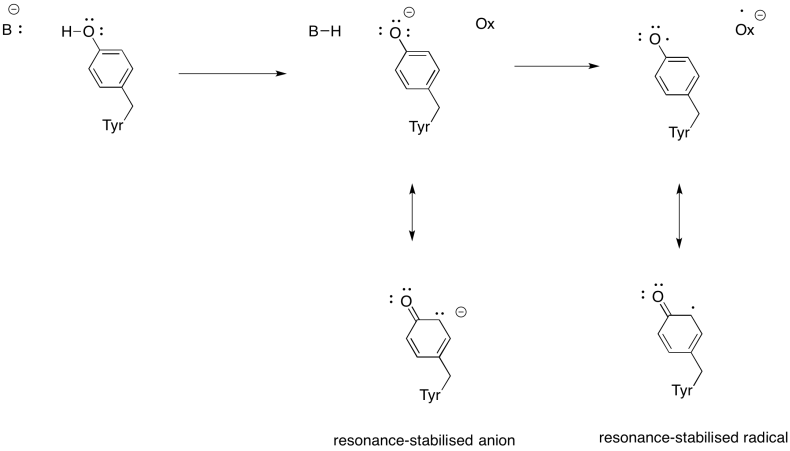
amellett, hogy csökkenteni kell az oxigént a vízbe, a komplex IV hozzájárul a protongradienshez is, további protonokat pumpálva a mitokondriális membránon. Ez a feladat további kihívásokat jelent. Egy egyszerű kapcsolási mechanizmus nem lehetséges, mert az elektronok az ellenkező irányba mozognak. Azonban a mechanizmus magában foglalja a fehérje konformációs változásait, amelyek akkor fordulnak elő, amikor a fémek megváltoztatják az oxidációs állapotokat. A koordinációs környezet finom változásai a közelben lévő aminosavmaradékok elmozdulását eredményezhetik. Könnyű elképzelni, hogy ha egy adott aminosav felfelé tolódik az intermembrán tér felé, akkor protont húzhat vele.
- a PROTONPUMPÁLÁS és az elektrontranszport ellentétes irányban fut a IV.komplexben, és le kell kapcsolni.
- a PROTONPUMPÁLÁSNAK a IV komplexben konformációs változásokra kell támaszkodnia.
gyakorlat \(\PageIndex{4}\)
a CuA helyén két réz található,két áthidaló ciszteinnel. Mindkettőt terminális histidinek kötik. Ezenkívül az egyik rézet egy további metionin köti, míg a másikat a fehérje gerincéből származó karbonil köti.
- húzza meg a rézeket a kötőhelyükön.
- írja le az egyes réz geometriáját.
- ha minden réz Cu (I), mekkora a koordinált elektronszám a komplex minden rézén?
- ha minden réz Cu (I), mekkora a komplex teljes töltése?
válasz a)
a)
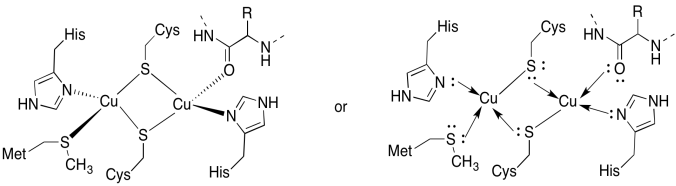
válasz b)
b) tetraéderes
válasz c)
c) Cu (I) = d10
4 donorok = 8 e –
összesen = 18E –
válasz d)
d) 2 x Cu (I) = 2+
2 x Cys-S- = 2-
összes többi semleges
összesen = 0
gyakorlat \(\PageIndex{5}\)
a CuB helyén lévő réz két hisztidinnel és a hisztidin-tirozin konjugátummal van összekötve.
- húzzuk fel a rezet a kötőhelyre.
- írja le a réz geometriáját.
- ha a réz Cu(I), mekkora a koordinált elektronszám a komplexben?
- ha a réz Cu(I), mekkora a komplex teljes töltése?
válasz a)
a)
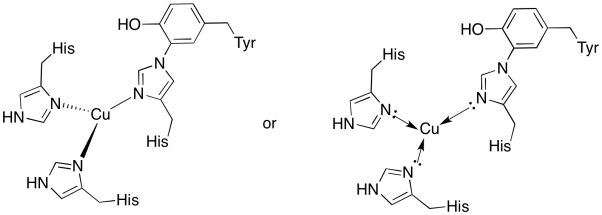
válasz b)
b) trigonális sík
válasz c)
c) Cu (I) = d10
3 donorok = 6 e –
összesen = 16 e –
válasz d)
d) Cu (I) = 1+
histidines semleges
összesen = 1+
gyakorlat \(\PageIndex{6}\)
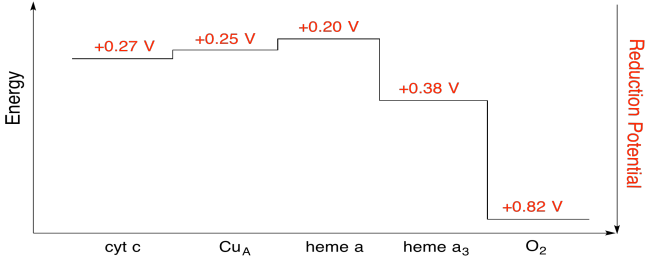
nehéz mérni az egyes helyek redukciós potenciálját egy fehérjén belül. A kutatók azonban képesek voltak megbecsülni ezeket az értékeket az EPR spektrumok különböző körülmények közötti mérésével. Az alábbi redukciós potenciálokat feltételezve rajzoljon egy reakció előrehaladási diagramot egy elektron szállításához egészen a citokróm c-től a molekuláris oxigénig.
 válasz
válasz
gyakorlat \(\PageIndex{7}\)
a fenti ábra értékeinek felhasználásával számítsa ki az energiaváltozást, amikor egy elektron átkerül az a hemről az a3 hemre.
válasz
feltételezve, hogy a redukciós potenciálok a következők:
a hem(ökör) + e – a – hem(piros) eored = 0,20 V
A3 hem(ökör) + e-A3 hem(piros) eored = 0.38 V
ezután a reakció potenciális különbsége, 6eo = 0,38 – (0,20) V = 0,18 V.
a Faraday – reláció = – N F A 6 fő =
6G = -1 x 96,485 J V-1 mol-1 x 0,13 V = 17,367 J mol-1 = 17,4 kJ mol-1
forrás
Chris P Schaller, Ph. D., (Szent Benedek Főiskola / Szent János Egyetem)