A conjunctiva tumorok útmutatója
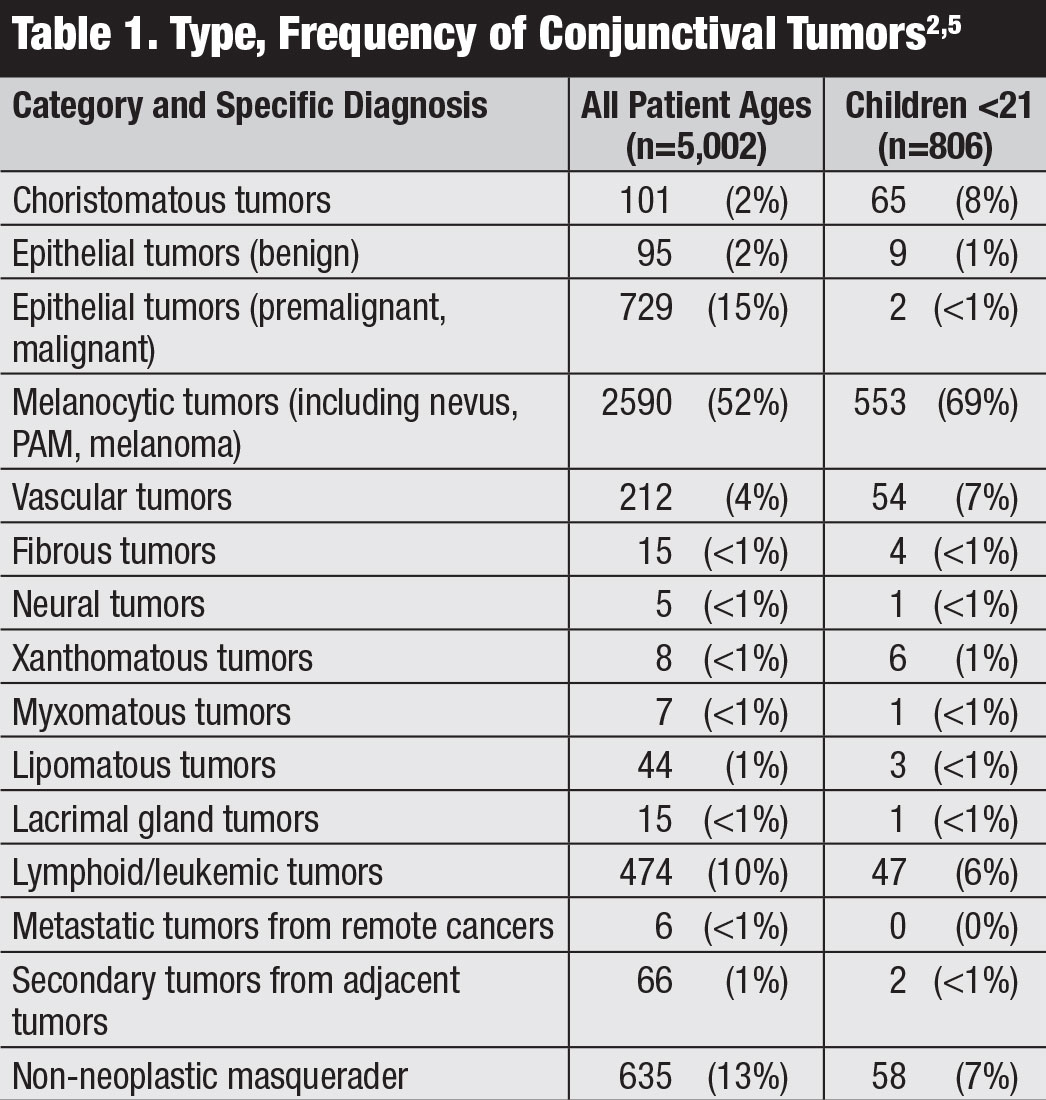
a conjunctiva tumorok közé tartozik a jóindulatú és rosszindulatú daganatok spektruma.1-5 a típusok életkor és rassz, szisztémás immunállapot és hosszú távú expozíció alapján különböznek. Egy szemészeti Onkológiai Központ 5002 esetének nagy vizsgálata kimutatta, hogy 52% jóindulatú, 18% premalignus és 30% rosszindulatú volt (1.táblázat).1,2 annak ellenére, hogy ez a jelentés egy szemészeti onkológiai központból származik, és a rosszindulatú daganatok felülreprezentáltak lehetnek, fontos, hogy a klinikusok megértsék a kötőhártya daganatok sokféleségét.
az öt leggyakoribb daganat a nevus (23%), az ocularis surface squamous neoplasia (OSSN, 14%), az elsődleges szerzett melanosis (PAM, 12%), a melanoma (12%) és a lymphoid tumor (9%) volt.5 malignus tumorokat észleltek leggyakrabban felnőtteknél, köztük melanomát (12%), laphámsejtes karcinómát (SCC, 9%), lymphomát (7%), Kaposi-szarkómát (<1%), metasztázist (<1%) és másokat.1 Conjunctival tumorok gyermekeknél malignitást mutatnak csak az idő 3% – ában.5
a leggyakoribb kötőhártya-daganatok áttekintése felkészíti Önt arra, hogy megfelelően kezelje őket, akár irodájában, akár áttétel útján.
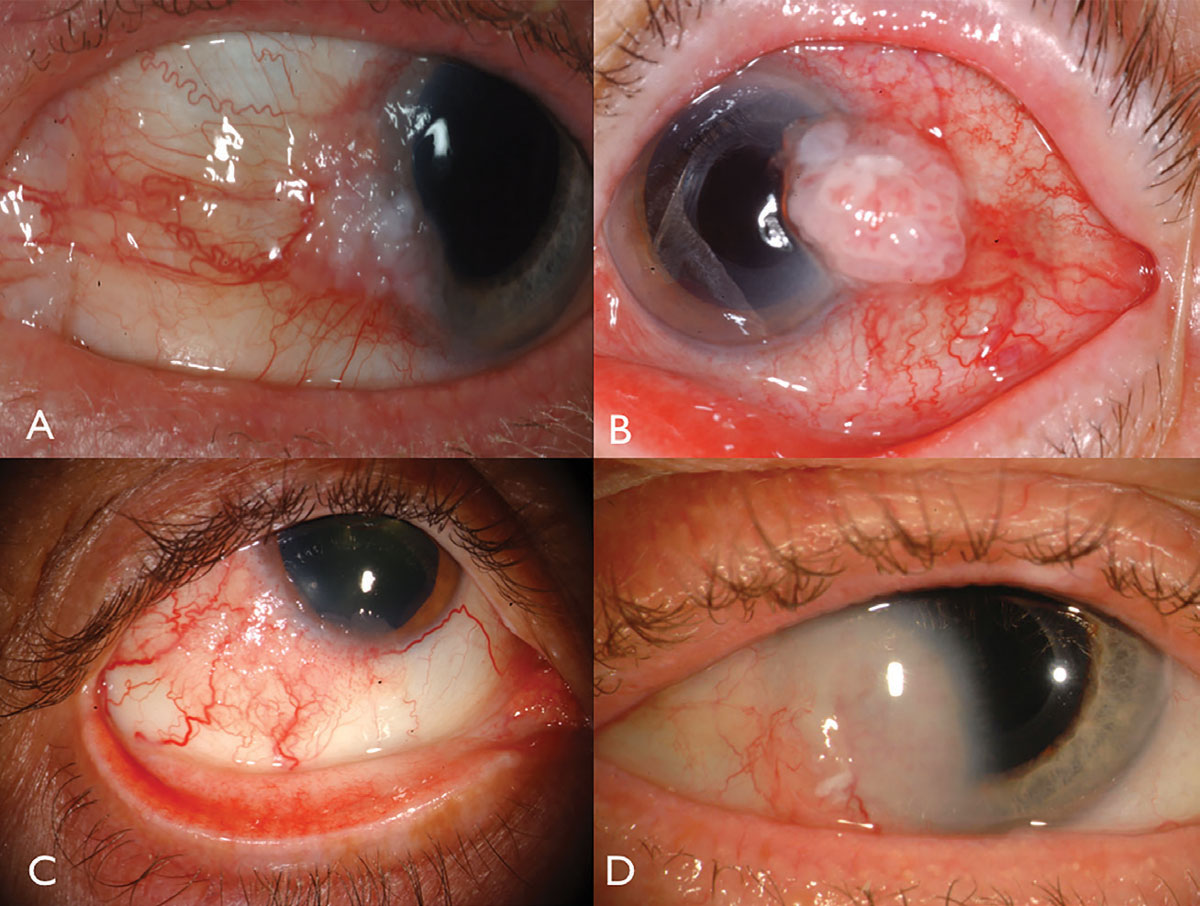
Fig. 1. Limbal OSSN: leukoplakiával és szaruhártya érintettséggel (a), kiemelkedő belső érrendszerrel és feeder erekkel (B), HIV-betegben (C), valamint mély szaruhártya-invázióval, amely reszekciót és plakk sugárterápiát igényel (D). Kattintson a képre a nagyításhoz.
szemfelszíni laphám neoplazia
az OSSN általános klinikai kifejezése magában foglalja a rosszindulatú daganatok spektrumát, amely az enyhe epitheliális diszplasztikus változásoktól, például a kötőhártya intraepithelialis neopláziájától (CIN) a súlyosabb invazív karcinómáig terjed, amely az alapmembránon keresztül behatol a substantia propria-ba, például a laphámsejtes karcinómáig terjed.
klinikai jellemzők. A Conjunctival OSSN klasszikusan idősebb kaukázusi férfiaknál fordul elő, különösen azoknál, akiknek krónikus napsugárzása van. Az Egyesült Államokban a conjunctiva SCC ötször gyakoribb a férfiaknál és a kaukázusiaknál. Afrikában azonban a kötőhártya SCC szinte egyformán gyakori a férfiak és a nők körében, és fiatalabb korban fordul elő, mint az Egyesült Államokban.6
a szemfelszíni laphám neoplazia általában egyoldalú, vaszkularizált kocsonyás tömegként jelenik meg, amely a napnak kitett kötőhártyában helyezkedik el az orr-vagy temporális limbusnál (1.ábra). Átfedő leukoplakia, kitágult feeder hajók és habos infiltráció a szomszédos szaruhártya hám előfordulhat, és ritkán támadják meg a földgömb vagy pályára.
kattintson a táblázat gombra a nagyításhoz.
hajlamosító tényezők. Az OSSN legfontosabb környezeti tényezői közé tartozik a krónikus napsugárzás és a cigarettafüst expozíció. Két kulcsfontosságú gazda hajlamosító tényező közé tartozik a tisztességes arcszín és a mögöttes humán immundeficiencia vírus (HIV) és a humán papillomavírus.6 az immunhiányos betegek, különösen a HIV-fertőzöttek, veszélyeztetik az OSSN-t, és előrehaladott, kétoldalú és invazív daganataik lehetnek.1 Ez különösen Afrikában figyelhető meg, ahol a HIV elterjedt, és az OSSN mind férfiaknál, mind nőknél, fiatalabb korban fordul elő.6 Egyéb immunrendszeri rendellenességek HAJLAMOSÍTHATJÁK a beteget az OSSN-re, beleértve a szervátültetett immunszuppressziót, az ekzema/atopiát, az ocularis cicatricialis pemphigoidot, a xeroderma pigmentosumot és az autoimmun betegségeket.7
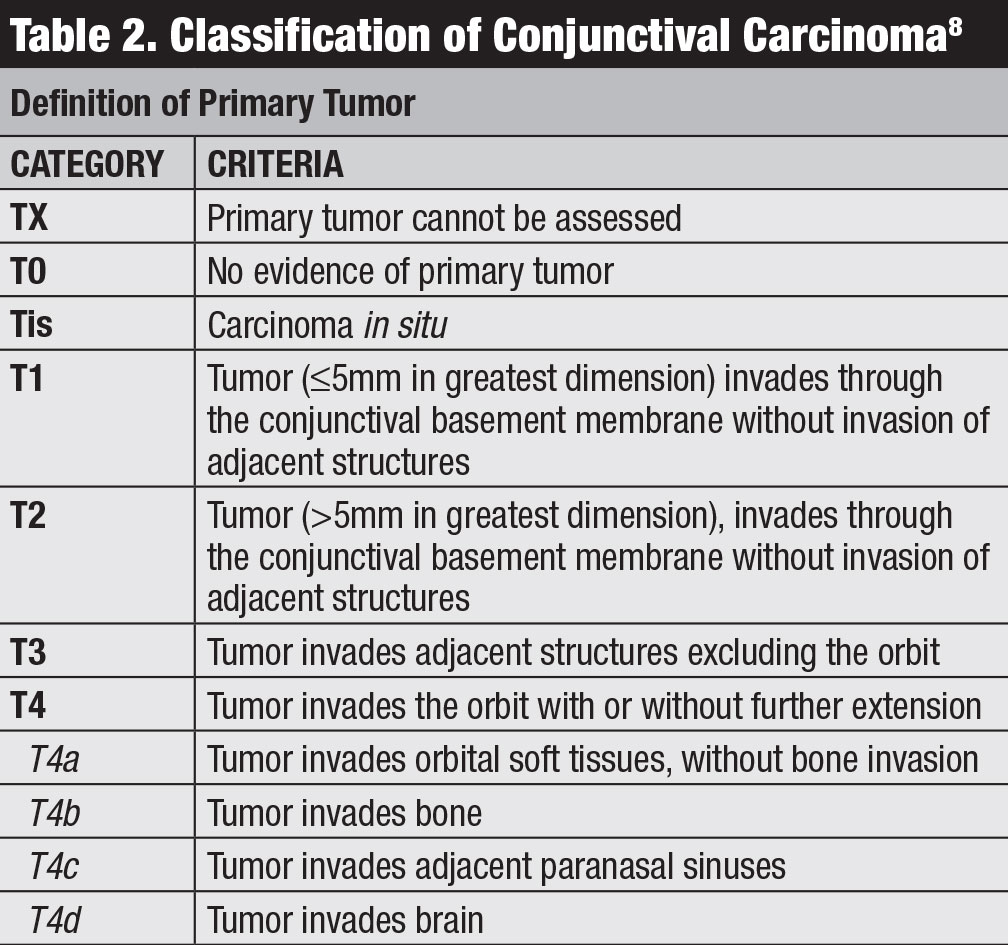
besorolás. Az American Joint Committee on Cancer (AJCC) 8. kiadású kézikönyve tartalmazza a conjunctiva carcinoma legfrissebb osztályozását, beleértve az SCC – t és a CIN-T (2.táblázat).8
menedzsment. Ez magában foglalja a műtéti reszekciót “érintés nélküli” technikával vagy nem sebészeti terápiákkal, például helyi kemoterápiával mitomicin C-vel (MMC) vagy 5-fluorouracil (5-FU), helyi vagy injektált immunterápia interferon alfa-2b-vel (IFN), helyi vírusellenes gyógyszerek (cidofovir) vagy fotodinamikai terápia.7,9-11
a műtéti érintés nélküli technika magában foglalja a tumor részletes értékelését réslámpás biomikroszkópiával, hogy megjelenítse az összes tumor margót, beleértve a bulbar, fornicealis és tarsalis komponenseket, hogy megértse a daganat teljes kiterjedését, és lehetővé tegye a klinikus számára, hogy kézzel rajzoljon sablonfelvételt.9 ezt a sablont ezután beviszik a műtétbe, hogy biztosítsák a teljes daganat eltávolítását.
a műtét idején csak a környező normál szövetet tartják csipesszel, és a daganatot soha nem érintik meg, hogy elkerüljék a tumor vetését. Ezenkívül a műtét során nem alkalmaznak kiegyensúlyozott sóoldatot a rákos sejtek folyadék-diszperziójának elkerülése érdekében. A daganat eltávolítását követően döntő fontosságú a tiszta eszközökkel történő Bezárás. Ezt a technikát alkalmazva az OSSN esetében a tumor perzisztenciája vagy kiújulása az esetek kevesebb mint 5% – ában fordul elő.
kattintson a táblázat gombra a nagyításhoz.
az 5-FU-val vagy MMC-vel végzett helyi kemoterápia hatékonyan oldja meg az OSSN-t, gyakran a terápiát követő két-négy héten belül, bár fennáll az őssejthiány kockázata. Helyi terápiás preferenciánk az IFN-vel végzett immunterápia, mivel jól tolerálható jó daganatkontroll mellett, gyakran három hónap alatt, kevés komplikációval és csak kisebb follikuláris kötőhártya-gyulladással.10,11 ezek a gyógyszerek lokálisan mérgezőek lehetnek a cornea epitheliumra, de interferon esetén kevésbé, ezért a betegeket szoros megfigyelés alatt kell tartani. Ha a költség tényező a beteg számára, akkor a lokális 5-FU a legolcsóbb, amelyet az MMC, majd az IFN követ.
Conjunctival Lymphoid tumorok
a Lymphoid neoplazmák az alacsony és magas fokú tumoroktól a limfociták monoklonális proliferációjáig terjednek. A periokuláris régióban előforduló limfoid tumorok gyakran több szövetet is magukban foglalnak, mint például a kötőhártya, az orbit és a szemhéj, és “okuláris adnexális” limfoid tumoroknak nevezik, beleértve a jóindulatú reaktív lymphoid hyperplasiát (BRLH) és a lymphomát.
a brlh és a lymphoma a spektrum ellentétes végein helyezkednek el, a BRLH klinikailag lokalizált “lazacfoltként” és kórszövettanilag jóindulatúként jelenik meg, míg a limfóma “lazacfoltként” is megjelenik, de agresszívebb kórszövettani jellemzőkkel, mitotikus aktivitással és rosszindulatúnak minősítve.
a szem adnexális limfoid daganatai jellemzően B-sejt eredetűek. Egy 268 conjunctivalis lymphomában szenvedő betegen végzett multicentrikus vizsgálatban a négy leggyakoribb típus az extranodális marginális zónás lymphoma (ENMZL, korábban mucosalis asszociált limfoid szövetnek nevezték) 68%-ban, follicularis lymphoma (FL) 16%-ban, köpenysejtes lymphoma (MCL) 7% – ban és diffúz nagy B-sejtes lymphoma (DLBCL) 5% – ban.12 a kötőhártya-limfóma egyéb típusai közé tartozik a lymphoplasmacytic lymphoma és a plasmacytoma.
klinikai jellemzők. A kötőhártya-limfóma általában 60-70 év közötti idősebb betegeknél jelentkezik. Ez a daganat elsődleges limfómaként nyilvánulhat meg, a periokuláris régióra korlátozva, vagy másodlagos limfómaként, másutt betegséggel. A legtöbb primer lymphoma ENMZL és FL, valamint másodlagos lymphoma DLBCL és MCL esetén fordul elő. Egy 117 conjunctival lymphomában szenvedő beteg elemzése 31% – ban talált szisztémás érintettséget, leggyakrabban kétoldali multifokális okuláris adnexalis lymphomában szenvedőknél.13
a kötőhártya limfóma klasszikusan rózsaszín lazac színű, sima felületű szubkonjunktivális tömegként nyilvánul meg, néha feeder edényekkel (2.ábra). Ez a sima, multilobulált tömeg hasonlít a follikuláris vagy papilláris kötőhártya-gyulladásra. Ez a daganat leggyakrabban a kötőhártya fornix (44%) vagy a középső (42%) régióban, ritkán pedig a karuncle (7%) vagy a limbus (7%) területén található.13 a kötőhártya mellett lymphoma is megtalálható, amely beszivárog a pályára, a szemhéjra vagy az uvea-ra.13 a kötőhártya-limfómában szenvedő betegek többsége nem mutat intraokuláris komponenst, de ha jelen van, általában az uvea-ban található, nem pedig a retinában vagy az üvegtestben.
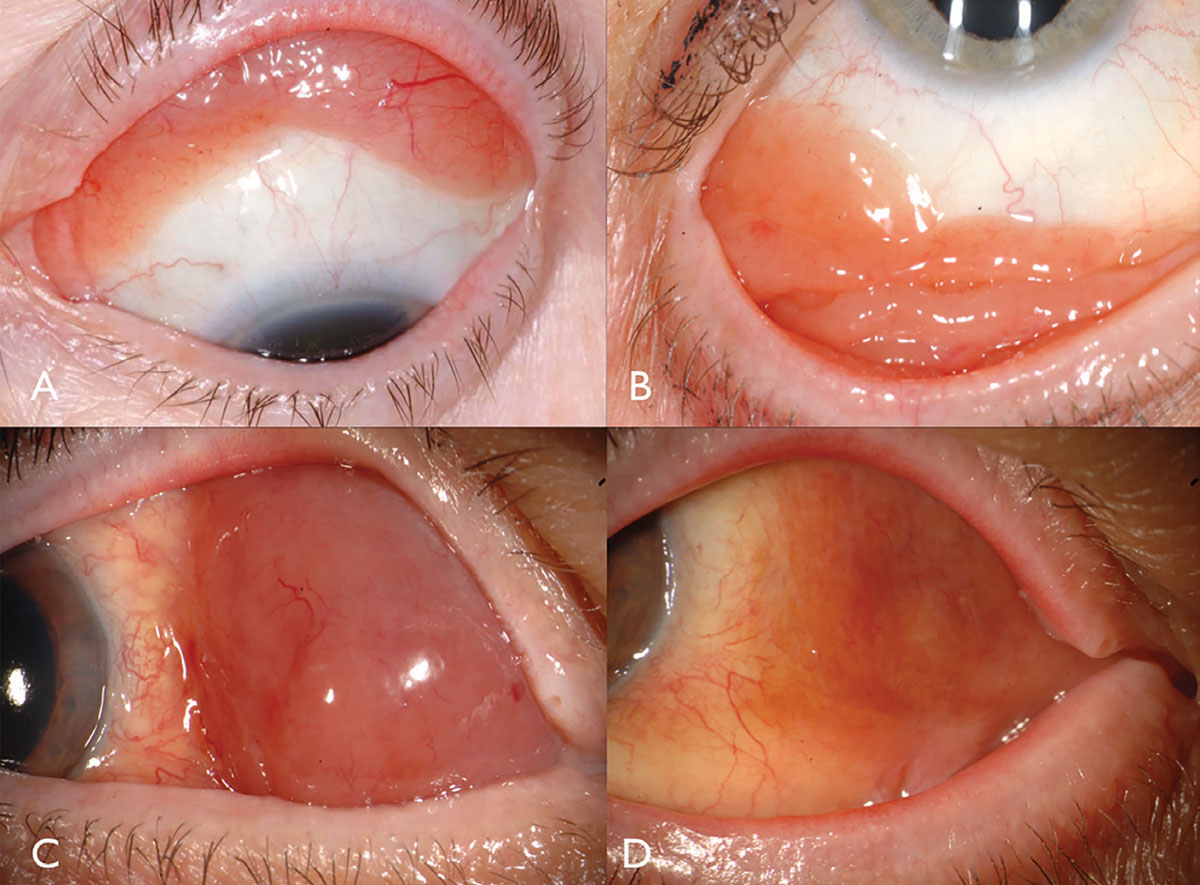
Fig. 2. Conjunctival lymphoma can be salmon-pink (A) or multilobulated forniceal (B). Medial forniceal conjunctival lymphoma before (C) and after (D) ritiximab. Click image to enlarge.
Predisposing factors. Immune dysfunction and autoimmune conditions, as well as infective etiologies such as Helicobacter pylori and Chlamydia psittaci are all predisposing factors for conjunctival lymphoma. A BRLH a lymphoma potenciális prekurzora lehet, és bár túlnyomórészt felnőtteknél fordul elő, alkalmanként gyermekeknél is előfordulhat.5 valójában minél fiatalabb a beteg a kötőhártya limfoid tumor diagnosztizálásakor, annál valószínűbb, hogy BRLH, nem pedig limfóma.
besorolás. A conjunctival lymphoma számos osztályozása létezik, köztük az Ann Arbor, az Egészségügyi Világszervezet és az AJCC 8th edition staging (3. táblázat).8 az AJCC klinikai stádiuma a tumor elhelyezkedésén, a regionális nyirokcsomón és a távoli érintettségen alapul.8
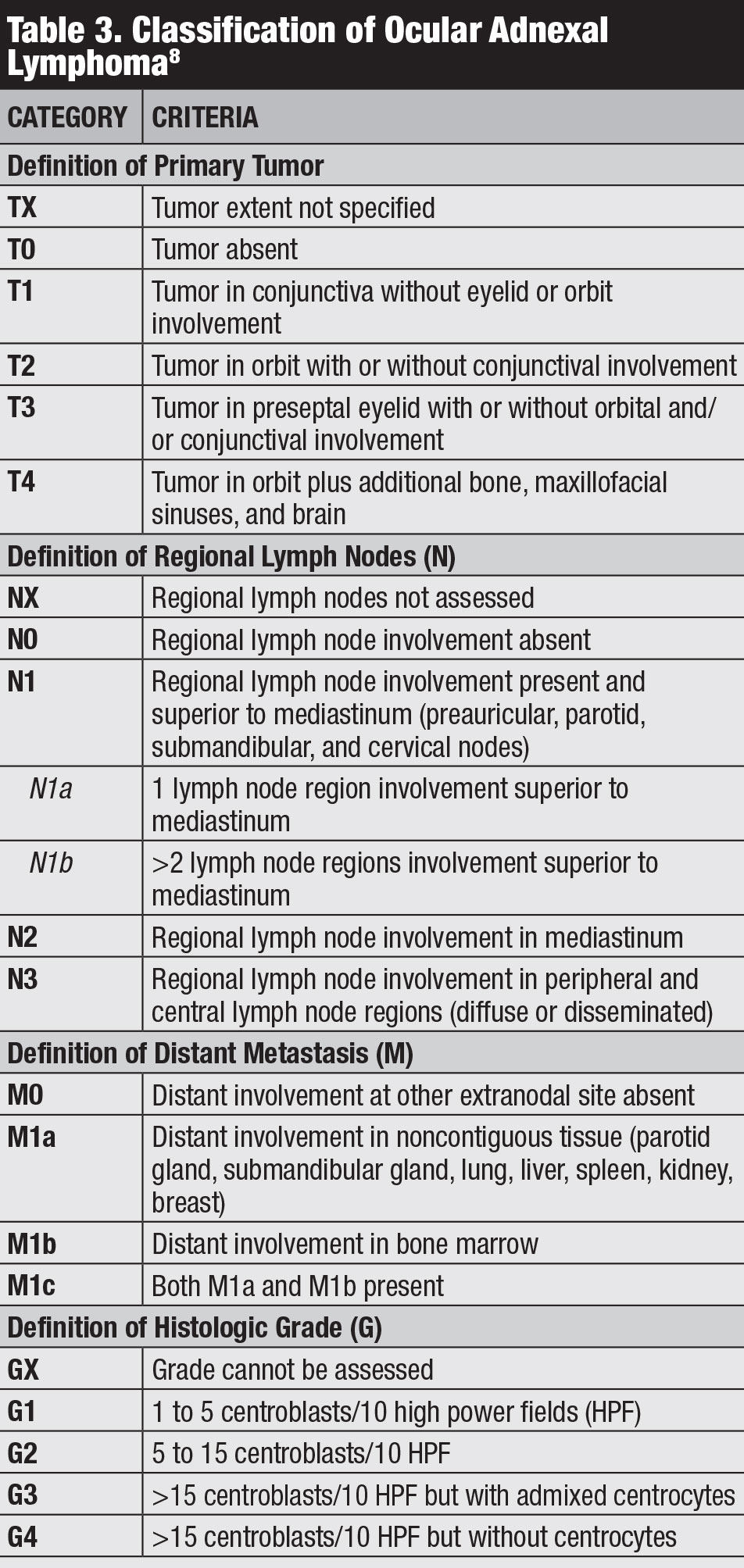
kattintson a táblázat gombra a nagyításhoz.
menedzsment. A conjunctiva lymphomában szenvedő betegek gondozása elsősorban a periokuláris érintettség mértékétől, a szisztémás érintettségtől és általános egészségi állapotuktól függ. Csak conjunctival lymphomában szenvedő betegeknél, akiknek nincs szisztémás érintettsége, a kezelés a teljes műtéti reszekcióra összpontosít. Külső sugárterápiával vagy rituximabbal történő kezelés lehetséges, ha a daganat nem gyógyítható. A periokuláris és szisztémás lymphomában szenvedők esetében a szisztémás rituximab-kezelés vagy a kemoterápia hozzáadása megfontolandó.
a kötőhártya-limfóma szisztémás prognózisa közvetlenül kapcsolódik az egyes altípusokhoz, mivel egy tanulmány szerint az ötéves túlélés 97% volt az ENMZL-nél, 82% az FL-nél, 55% A DLBCL-nél és csak 9% az MCL-nél.12
Conjunctival Melanoma
a Conjunctival melanocytás daganatok vitathatatlanul gyakoriak, az esetek több mint 50% – át képviselik egy szemészeti onkológiai egységből származó kötőhártya daganatok nagy sorozatában.1,2 a melanocita tumorok ebbe az osztályába számos típus tartozik, mint például a nevus, az arcszínnel kapcsolatos melanózis, A Pam, a másodlagos szerzett melanózis, a melanoma és a metasztázisok.1-5 egyes kontinenseken, ahol a betegek sötét arcbőrűek, még az OSSN is melanocitikusnak tűnhet. Ezen elváltozások közül a kötőhártya nevus 45% – ot, az elsődleges kötőhártya melanoma pedig az összes melanocita daganat 23% – át képviseli egy szem onkológiai gyakorlatban.2
az Egyesült Államokban a kötőhártya melanoma életkorhoz igazított előfordulása 1973 és 1999 között megduplázódott, 0,27 / millióról 0,54 / millióra.14,15 az incidencia 295% – kal nőtt a fehér férfiaknál az Egyesült Államokban ugyanabban a 27 éves időszakban, különösen a 60 éves vagy annál idősebb férfiak körében.14 A kutatók feltételezik, hogy a növekvő Arány összefüggésben lehet az ultraibolya fény expozíciójával.
klinikai jellemzők. A kötőhártya-melanoma pigmentált vagy nem pigmentált rosszindulatú daganat, amely Pam, nevus vagy de novo eredetű lehet.16 a Melanoma megtalálható a limbális, bulbar, fornicealis vagy palpebralis kötőhártyán, és gyakran kitágult, kanyargós adagolót és belső ereket mutat, amelyeket általában lapos PAM vesz körül (3.ábra). Általában a 2 mm-nél nagyobb vastagságú daganatok jelentős kockázatot jelentenek a nyirokcsomó metasztázisában. A tumor inváziója a pályára különösen súlyos, jelentős metasztatikus kockázattal.
az esetek 50% – ában lokális tumor kiújulás vagy új daganat található, gyakran az új PAM transzformációval összefüggésben. A távoli metasztázis—gyakran a preauricularis, submandibularis vagy nyaki nyirokcsomó láncra-a betegek 25% – ában fordul elő. A Sentinel nyirokcsomó biopszia segíthet a klinikusoknak a szubklinikai nyirokcsomó-infiltráció értékelésében. Többszörös kiújulás, különösen azok, amelyek a pályát érintik, szükségessé teszik az orbitális exenterációt.
hajlamosító tényezők. A kötőhártya melanoma legfontosabb hajlamosító tényezője a régóta fennálló kötőhártya nevus vagy PAM jelenléte.16-18 a kötőhártya melanoma eredetének szövettani vizsgálata során a kutatók azt találták, hogy az eredet 74% – ban PAM, 19% – ban de novo, 7% – ban nevus volt.16 klinikai vizsgálat becslése szerint 300 nevi közül egy melanoma alakul ki.17,18
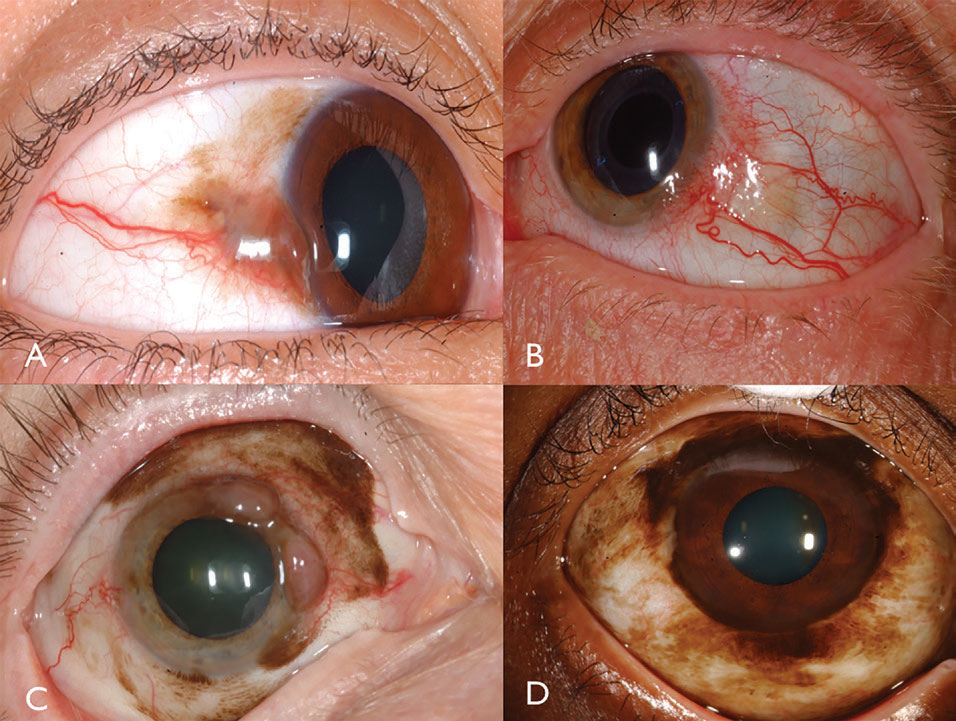
Fig. 3. Pigmentált kötőhártya melanoma a PAM (A) – ból származhat. A nem pigmentált kötőhártya melanoma intenzív vaszkularitással járhat (B). A PAM vegyes pigmentált/nem pigmentált kötőhártya melanomát is okozhat (C). PAM limbális melanómát okozott ebben az afro-amerikai betegben (D). Kattintson a képre a nagyításhoz.
egy nagy klinikai vizsgálat megállapította, hogy a Pam melanomává történő átalakulásának 10 éves kockázata körülbelül 9% volt, és a Pam nagyobb mértéke elősegítette a melanomává történő átalakulás nagyobb kockázatát.19 ezért fontos azonosítani a PAM-ot, és kezelni ezt az állapotot műtéti kivágással, krioterápiával, sőt felületes keratectomiával (ha szaruhártya érintettsége van) a melanoma megelőzése céljából.
a kötőhártya nevus megkülönböztetése a melanomától kihívást jelenthet. A közelmúltban végzett elemzés 510 esetben kötőhártya nevus vs. melanoma gyermekeknél a melanoma gyakoribb volt az idősebb gyermekeknél, 4,80 relatív kockázattal (RR), nagyobb tumorvastagsággal (RR 1,14), nagyobb bázissal (RR 4,92), tumorvérzéssel (RR 25,30) és belső ciszták hiányával (RR 5,06).5 a kutatók ezeket a jellemzőket, amelyek prediktív kötőhártya melanoma gyermekeknél, egy emlékeztető: fogás Melanoma, ami: gyermekek idősebb, Vastagság / bázis nagyobb, ciszta hiányzik, vérzés Melanoma.5
a Pam megkülönböztetése a melanomától szintén kihívást jelenthet; azonban a melanoma vastagsága és a PAM teljesen lapos. 1224 Pam vs.melanoma eset elemzése során minden életkorban szignifikánsan nagyobb volt a melanoma a beteg medián életkora (54 vs. 61 év), a férfi nem (35% vs. 49%), a fornix (2% vs. 6%) és a tarsus (1% vs. 4%), a nagyobb medián bazális átmérő (6 mm vs. 8 mm), a vastagság (<1 mm vs. 1 mm), a feeder hajók (10% vs. 48%) és az intrinsic hajók (4% vs. 33%); és vérzés (<1% vs. 3%).2
a szöveti biomarkerek fontosak a kötőhártya melanoma értékeléséhez, és magukban foglalják a BRAF mutációt, a TERT promoter mutációt és a PTEN mutációt.1 ezeknek a biomarkereknek az azonosítása kritikus fontosságú a metasztázis kezelésére vagy megelőzésére szolgáló szisztémás terápia tervezésekor, mivel bizonyos biomarkerek elleni célzott terápiák állnak rendelkezésre, például a vemurafenib a BRAF-mutált malignitás esetén.
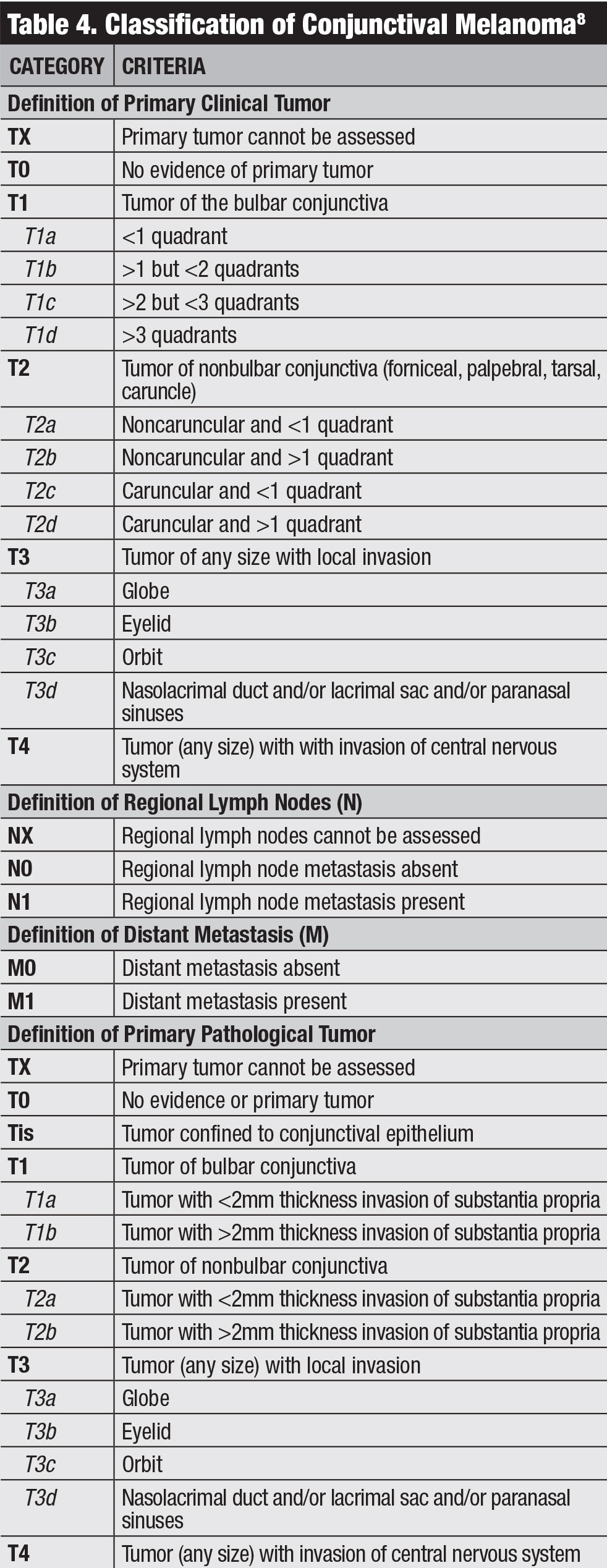
kattintson a táblázat gombra a nagyításhoz.
besorolás. Az AJCC conjunctiva melanoma klinikai besorolása a tumor kiterjedésén, a kvadránsokon, a tumor helyén és az invazív jellemzőkön alapul (4.táblázat).8 csapatunk az AJCC 7. kiadása alapján tanulmányozta a kötőhártya melanoma kimenetelét, és megállapította, hogy ez a stádium nagymértékben előrejelzi a prognózist.20 a T2 és T3 kategóriába sorolt Melanoma (a T1-hez képest) szignifikánsan magasabb lokális kiújulás, regionális nyirokcsomó metasztázis, távoli metasztázis és halálozási arányokat mutatott.
menedzsment. A kötőhártya melanoma gondozása alapvetően magában foglalja a teljes műtéti reszekciót érintés nélküli technikával a tumor vetésének elkerülése érdekében. Az első műtét a legfontosabb, mivel a teljes daganat finom eltávolítása tumor vetés nélkül kulcsfontosságú a jövőbeni visszatérések és áttétek megelőzésében.16
a corneoscleralis limbus Melanómáját az operáló mikroszkóp alatt is eltávolítják az érintés nélküli technikával. A lapos szaruhártya komponenst abszolút alkohollal, felületes epitheliectomiával távolítják el Bowman membránjának megzavarása nélkül. A kötőhártya részt 2-3 mm-es margókkal távolítják el, majd a limbusnál lapos episcleralis disszekcióval szabadítják fel. Ha szklerális invázió van jelen, plakk sugárterápiát alkalmaznak. Az összes kötőhártya margót kettős fagyasztás-olvadás krioterápiával kezeljük.
a rekonstrukció magában foglalja az elsődleges zárási technikákat, rotációs csappantyút vagy amniotikus membránátültetést, gyakran symblepharon gyűrűvel, amniotikus membrán izolálásával. A pályára kiterjedő Melanoma orbitális exenterációt vagy újabban immunterápiát igényel ellenőrzőpont gátlással.21
a conjunctivalis melanomában szenvedő betegeket szemészeti onkológusnak kell monitoroznia a lokális kiújulás, illetve a metasztatikus betegség szempontjából szisztémás melanoma onkológusnak, különösen regionális nyirokcsomó-tapintás és sentinel nyirokcsomó biopszia esetén. A metasztázisok kezdetben a preauricularis vagy submandibularis nyirokcsomókban, majd később a tüdőben és az agyban jelentkeznek. Új bizonyítékok arra utalnak, hogy a melanoma metasztázis érzékeny lehet a BRAF-gátlókra vagy az immun-ellenőrzőpont-gátlókra.21,22
a kötőhártya daganatok a daganatok széles spektrumát ölelik fel. A leggyakoribb rosszindulatú daganatok közé tartozik az OSSN, a lymphoma és a melanoma. A klasszikus klinikai jellemzők felismerése, a prekurzorok megértése, valamint ezeknek a rosszindulatú daganatoknak a gyors és megfelelő kezelése fontos a betegek legjobb kimeneteléhez.
Dr. Shields, Lally és Shields a Philadelphiai Thomas Jefferson Egyetem Wills Eye Hospital szemészeti onkológiai szolgálatánál dolgoznak. A támogatást az Eye Tumor Research Foundation, Philadelphia nyújtja.
1. Shields CL, Chien JL, Surakiatchanukul T, et al. Kötőhártya daganatok: a klinikai jellemzők, kockázatok, biomarkerek és eredmények áttekintése. A 2017-Es J. Donald M. Gass Előadás. Ázsia Pac J Ophthalmol. 2017;6:109-20.
2. Shields CL, Alset AE, Boal NS, et al. Kötőhártya daganatok 5002 esetben. Összehasonlító elemzése jóindulatú versus rosszindulatú társaik. A 2016-Os James D. Allen Előadás. Am J Ophthalmol. 2017;173:106-33.
3. Pajzsok CL, pajzsok JA. A kötőhártya és a szaruhártya tumorai. Surv Ophthalmol. 2004;49:3-24.
4. Grossniklaus ő, Zöld WR, Luckenbach M, et al. Conjunctival elváltozások felnőtteknél. Klinikai és kórszövettani áttekintés. Szaruhártya. 1987;6:78-116.
5. Shields CL, Sioufi K, Alset ae, et al. Kötőhártya daganatok gyermekeknél. Jellemzők, amelyek megkülönböztetik a jóindulatúakat a rosszindulatú daganatoktól. JAMA Ophthalmol. 2017;135:215-24.
6. Gichuhi S, Sagoo MS, Weiss HA, et al. A szem felszíni laphám neoplázia epidemiológiája Afrikában. Trop Med Int Egészség. 2013;18:1424-43.
7. Pajzsok CL, Ramasubramanian A, Mellen P, pajzsok JA. Kötőhártya laphámsejtes karcinóma, amely immunszuppresszált betegeknél jelentkezik (szervátültetés, humán immundeficiencia vírusfertőzés). Szemészet. 2011;118:2133-7.
8. Amin MB, Edge S, Greene F, et al., Szerk. AJCC Rákmegtartó kézikönyv. 8. kiadás. Chicago; Springer Nemzetközi Kiadó: 2017.
9. Pajzsok JA, pajzsok CL, de Potter PV. A kötőhártya daganatok sebészeti megközelítése. Az 1994-Es Lynn B. McMahan Előadás. Arch Ophthalmol. 1997;115:808-15.
10. Pajzsok CL, Kaliki S, Kim HJ, et al. Interferon szemfelszíni laphám neoplázia esetén 81 esetben: Eredmények Az Amerikai Rákosztályozási Vegyes Bizottság alapján. Szaruhártya. 2013;32(3):248-56.
11. Karp CL, Galor A, Chhabra S, et al. Subconjunctival/perilesional rekombináns interferon A2B ocularis surface squamous neoplasia esetén: 10 éves áttekintés. Szemészet. 2010;117(12):2241-6.
12. Kirkegaard MM, Rasmussen PK, Coupland SE, et al. Conjunctival lymphoma-nemzetközi multicentrikus retrospektív vizsgálat. JAMA Ophthalmol. 2016;134:406-14.
13. Pajzsok CL, pajzsok JA, Carvalho C, et al. Conjunctival lymphoid tumorok: 117 eset klinikai elemzése és a szisztémás lymphomával való kapcsolat. Szemészet. 2001;108:979-84.
14. Yu GP, Hu DN, McCormick S, ujj PT. Conjunctiva melanoma: Növekszik az Egyesült Államokban? Am J Ophthalmol. 2003;135:800-6.
15. Tuomaala S, Kivela T. a kötőhártya-melanómával kapcsolatos levelezés: növekszik-e az Egyesült Államokban? Am J Ophthalmol. 2003;136:1189-90.
16. Shields CL, Markowitz JS, Belinsky I, et al. Kötőhártya melanoma. A tumor eredetén alapuló eredmények 382 egymást követő esetben. Szemészet. 2011;118:389-95.
17. Shields CL, Fasiuddin AF, Mashayekhi a, et al. Conjunctival nevi: klinikai jellemzők és természetes lefolyás 410 egymást követő betegnél. Arch Ophthalmol. 2004;122:167-75.
18. Gerner N, Norregaard JC, Jensen OA, Prause JU. Conjunctival naevi Dániában 1960-1980. 21 éves nyomon követési tanulmány. Acta Ophthalmol Scand. 1996;74:334-7.
19. Pajzsok JA, pajzsok CL, Mashayekhi a, et al. A kötőhártya elsődleges szerzett melanózisa: a melanoma progressziójának kockázata 311 szemben. A 2006-os Lorenz E. Zimmerman előadás. Szemészet. 2008;115:511-9.
20. Shields CL, Kaliki S, Al-Dahmash S, et al. Az Amerikai Rákellenes Vegyes Bizottság (AJCC) klinikai osztályozása előrejelzi a kötőhártya melanoma kimenetelét. Ophthalm Plast Reconstr Surg. 2012; 5:313-23.
21. Sagiv O, Thakar SD, Kandl TJ, et al. Immunterápia programozott sejthalállal 1 inhibitor 5 kötőhártya melanomában szenvedő beteg számára. JAMA Ophthalmol. 2018 november 1;136(11): 1236-41.
22. Dalvin LA, Shields CL, Orloff M, et al. Ellenőrzőpont inhibitor immunterápia. Szisztémás javallatok és szemészeti mellékhatások. Retina. 2018;6:1063-78.