Chemical Species
Kulcsinformációk & összefoglaló
- a chemical species olyan molekuláris entitások halmaza, amelyek kémiailag azonosak, és ugyanazokat a molekuláris energiaszinteket képesek feltárni egy meghatározott időskálán
- ha két konformációs izomer elég lassan interkonvertál ahhoz, hogy mindegyiket különböző NMR spektrumok detektálják, akkor két különböző NMR-spektrummal detektálhatóak kémiai Fajok
- a szupramolekuláris kémiában olyan szupramolekuláris struktúrák, amelyek kölcsönhatásai a létrehozás vagy bizonyos intermolekuláris kötések megszakítása ugyanaz a kémiai faj
mit jelent a ‘kémiai Fajok’?
egyszerűen fogalmazva, ha egy atom azonos egy másik atommal,akkor ugyanaz a kémiai faj. Ez igaz a molekulákra is, mivel ha az egyik molekula azonos a másikkal, akkor ugyanazok a kémiai Fajok.
egy kémiai faj meghatározható olyan molekuláris entitások halmazaként is, amelyek kémiailag azonosak, és egy meghatározott időskálán ugyanazokat a molekuláris energiaszinteket fedezhetik fel.
például egy vízzel teli palack pontosan ugyanolyan kémiai molekulákat tartalmaz. Sőt, egy tömör aranyrúd pontosan ugyanazon kémiai faj atomjait tartalmazza.
a ‘kémiai Fajok’ kifejezés arra a formára is utalhat, amelyben egy vegyi anyag létezik, amikor az oldatban megtalálható. Például, ha a NaCl oldatban oldódik, akkor valójában nem találja meg a NaCl-t. Inkább Na+ ionok és Cl – ionok vannak – ez azért van, mert a NaCl disszociált. Mint ilyen, a kémiai fajok ebben az oldatban a Na + ionok és a Cl-ionok lesznek. Ez a szabály minden erős elektrolitra igaz. Azt mondják, hogy Ionos fajok vannak oldatban.
azon elektrolitok esetében, amelyek oldatban nem disszociálnak, a kémiai faj meghatározása szerint ugyanaz, mint az oldathoz való hozzáadás előtt. Azt mondják, hogy molekuláris fajok vannak oldatban.
a gyenge elektrolitokról ismert, hogy mind az ionos, mind a molekuláris Fajok oldatban vannak – ez azért van, mert egyes molekulák disszociálnak, mások pedig nem.
ezen túlmenően a különböző izotópokkal rendelkező molekulák egy csoportját is ugyanazon kémiai fajba sorolják.
kémiai fajok és NMR
az NMR (magmágneses rezonancia) spektroszkópia a szerves kémiai vegyületek szerkezetének meghatározására használt kémiai technika – ez az egyetlen spektroszkópiai módszer, amely a teljes spektrum teljes elemzését biztosítja. Ez egy roncsolásmentes technika, és mindössze egy milligramm analitot igényel a jó adatok előállításához.
az NMR azon az elméleten alapul, hogy minden atommag elektromos töltésű és rendelkezik spinnel. Ez azt jelenti, hogy ha külső mágneses mezőt alkalmazunk az atommagokra, lehetséges az energiaátvitel az alap energiaszint és a magasabb energiaszint között. Amikor ez a spin visszatér az alapszintjére, energiát bocsát ki. A frekvencia, amelyen ez megtörténik, mérhető, majd feldolgozható, hogy NMR spektrumot kapjon.
NMR használható a konformációs izomerek azonosítására. Ezek olyan izomerek, amelyek a forgás során keletkeznek 6-6 kötések – szobahőmérsékleten is nagyon gyorsan átalakulnak (váltanak a kettő között). Az egyik példa egy molekulára, amely ezt teszi, a bután, amely az alábbi képen látható.

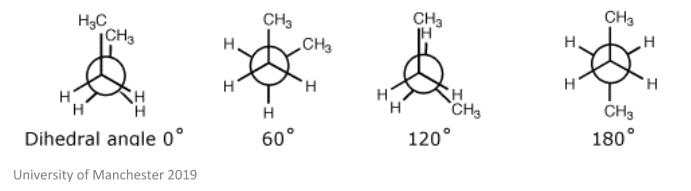
ez az elmélet akkor válik fontossá, amikor kémiai fajokról beszélünk. Mivel ezek az izomerek egyik formából a másikba képesek átalakulni, két izomer keveréke viszonylag lassan átalakulhat. Amint azt korábban tárgyaltuk, a kémiai fajokat egy bizonyos időpontban ilyennek definiálják. Ez azt jelenti, hogy ha ez a két izomer elég lassan átalakul ahhoz, hogy mindegyiket különböző NMR spektrumok detektálják, akkor két különböző kémiai fajként definiálnák őket. Ez azt is jelenti, hogy ugyanazon izomer keveréke ugyanazon kémiai fajnak tekinthető, mivel a kettő egyensúlyban van.
kémiai fajok a szupramolekuláris kémiában
ahhoz, hogy először megértsük, hogyan határozzák meg a kémiai fajokat a szupramolekuláris kémiában, ismernie kell a tudományág alapjait. A szupramolekuláris a kémia azon területére utal, amely azzal foglalkozik, hogy a molekulák hogyan kapcsolódnak össze, hogy diszkrét számú alegységből nagyobb ‘rendszereket’ alkossanak. A szupramolekuláris kémiában szerepet játszó erők a gyenge erőktől (például hidrogénkötés és elektrosztatikus kölcsönhatások) az erősebb erőkig (például kovalens kötések) terjedhetnek. Tanulmányok ezen a területen a kémia elsősorban a gyengébb és reverzibilis nem kovalens kötések között bizonyos molekulák, mint például:
- hidrogénkötések
- hidrofób erők
- van Der Walls erők
- Fémkoordináció
- Pi-pi kölcsönhatások
ezeknek a kötéseknek a tanulmányozása különösen fontos a biológiai tudományokban, mivel fontosnak bizonyultak a molekuláris önszerelésben és hajtogatásban.
a szupramolekuláris kémia kémiai fajait tekintve szupramolekuláris struktúrákként definiálják őket, amelyek kölcsönhatásai bizonyos intermolekuláris kötések létrehozásával vagy megszakításával jöttek létre.