3.3 Conformazione del cicloesano
Conformazioni del cicloesano
Una struttura planare per il cicloesano è chiaramente improbabile. Gli angoli di legame sarebbero necessariamente 120º, 10,5 º più grandi dell’angolo tetraedrico ideale. Inoltre, ogni legame carbonio-carbonio in una tale struttura sarebbe eclissato. L’angolo risultante e le tensioni eclissanti destabilizzerebbero gravemente questa struttura. Se due atomi di carbonio sui lati opposti dell’anello a sei membri vengono sollevati dal piano dell’anello, gran parte della deformazione angolare può essere eliminata.
Questa struttura barca ha ancora due legami eclissati e grave affollamento sterico di due atomi di idrogeno sulla “prua” e “poppa” della barca. Questo affollamento sterico è spesso chiamato ostacolo sterico. Torcendo la conformazione della barca, l’ostacolo sterico può essere parzialmente alleviato, ma il conformatore twist-boat conserva ancora alcune delle tensioni che caratterizzano il conformatore della barca. Infine, sollevando un carbonio sopra il piano dell’anello e l’altro sotto il piano, si forma un conformatore “a sedia” relativamente privo di sforzi. Questa è la struttura predominante adottata dalle molecole di cicloesano.
Le indagini riguardanti le conformazioni del cicloesano furono avviate da H. Sachse (1890) e E. Mohr (1918), ma non fu fino al 1950 che un trattamento completo delle molteplici conseguenze dei conformatori della sedia interconvertente e dei diversi orientamenti dei legami pendenti fu chiarito da D. H. R. Barton (Premio Nobel 1969 insieme a O. Hassel). La seguente discussione presenta alcune delle caratteristiche essenziali di questa analisi conformazionale.
Esaminando attentamente la conformazione di una sedia del cicloesano, troviamo che i dodici idrogeni non sono strutturalmente equivalenti. Sei di loro si trovano alla periferia dell’anello di carbonio e sono chiamati equatoriali. Gli altri sei sono orientati sopra e sotto il piano approssimativo dell’anello (tre in ogni posizione) e sono definiti assiali perché sono allineati parallelamente all’asse di simmetria dell’anello.
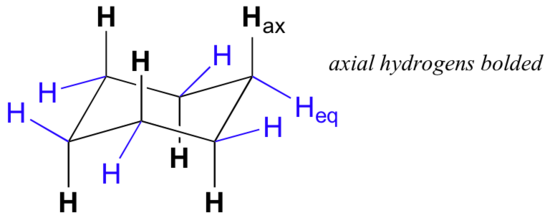
Nella figura sopra, gli idrogeni equatoriali sono colorati di blu e gli idrogeni assiali sono in grassetto. Poiché ci sono due conformazioni sedia equivalenti di cicloesano in rapido equilibrio, tutti i dodici idrogeni hanno 50% equatoriale e 50% carattere assiale. La figura seguente illustra come convertire un modello molecolare di cicloesano tra due diverse conformazioni della sedia-questo è qualcosa che dovresti praticare con i modelli. Si noti che un “flip ad anello” fa sì che gli idrogeni equatoriali diventino assiali e viceversa.
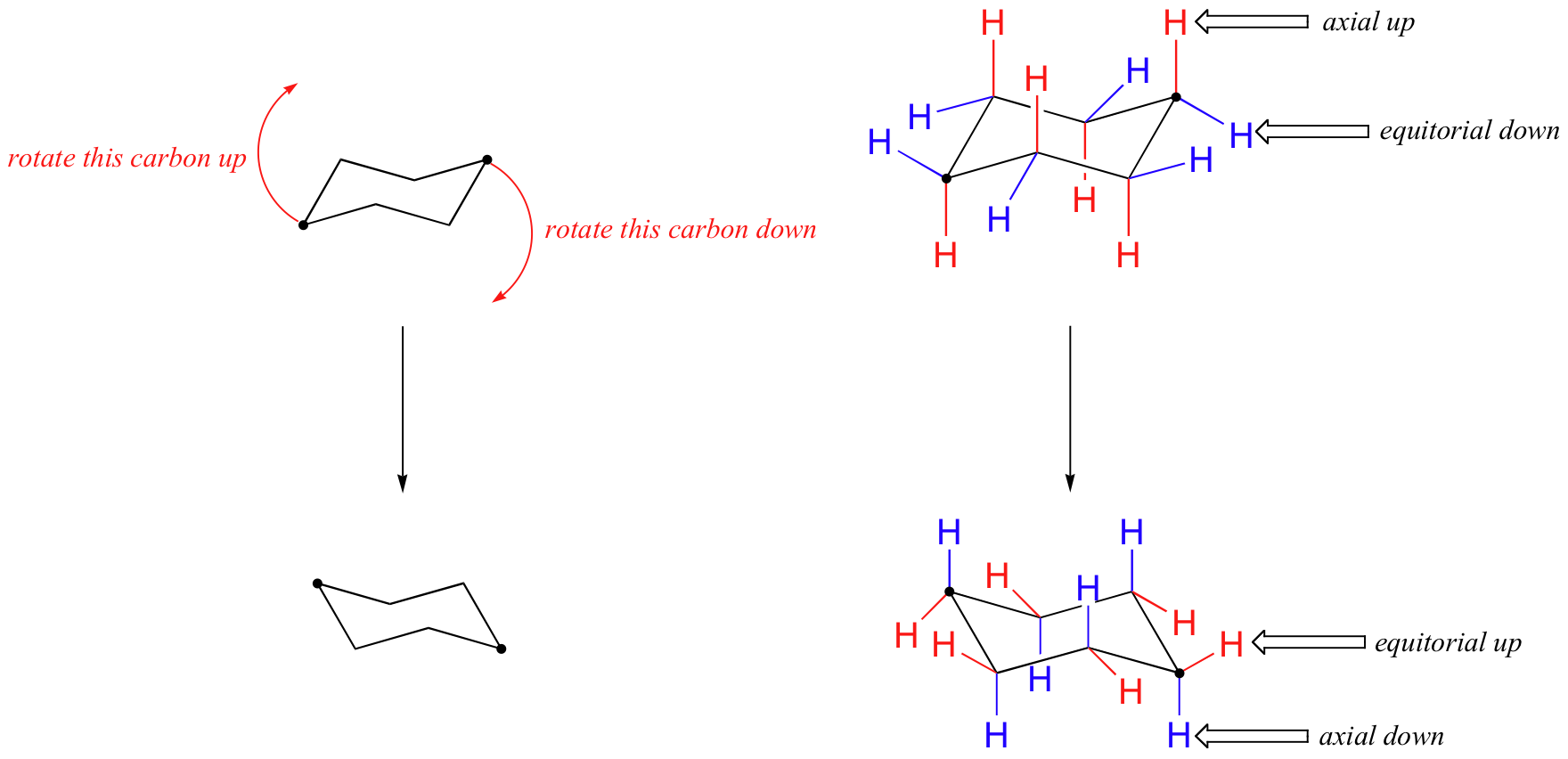
Poiché i legami assiali sono paralleli tra loro, i sostituenti più grandi dell’idrogeno generalmente soffrono di un maggiore affollamento sterico quando sono orientati assiale piuttosto che equatoriale. Di conseguenza, i cicloesani sostituiti adotteranno preferenzialmente conformazioni in cui i sostituenti più grandi assumono l’orientamento equatoriale.
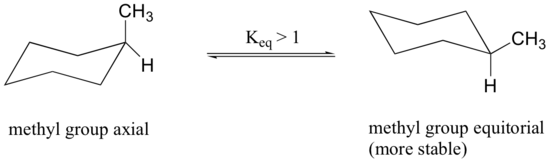
Quando il gruppo metilico nella struttura sopra occupa una posizione assiale subisce l’affollamento sterico dai due idrogeni assiali situati sullo stesso lato dell’anello.

La conformazione in cui il gruppo metilico è equatoriale è più stabile, e quindi l’equilibrio si trova in questa direzione.
L’ostacolo sterico relativo sperimentato da diversi gruppi sostituenti orientati in una posizione assiale contro equatoriale sul cicloesano può essere determinato dall’equilibrio conformazionale del composto. La corrispondente costante di equilibrio è correlata alla differenza di energia tra i conformatori e la raccolta di tali dati ci consente di valutare la tendenza relativa dei sostituenti ad esistere in una posizione equatoriale o assiale.Una tabella di questi valori di energia libera (a volte indicato come Un valori) può essere esaminata cliccando qui.
Guardando i valori energetici in questa tabella, è chiaro che la “dimensione” apparente di un sostituente (in termini di preferenza per l’orientamento equatoriale rispetto all’orientamento assiale) è influenzata dalla sua larghezza e dalla lunghezza del legame con il cicloesano, come evidenziato dal fatto che un gruppo vinilico assiale è meno ostacolato dell’etile e lo iodio leggermente inferiore al cloro.
Abbiamo notato in precedenza che i cicloalcani aventi due o più sostituenti su diversi atomi di carbonio ad anello esistono come una coppia (a volte più) di stereoisomeri configurazionali. Ora dobbiamo esaminare il modo in cui le conformazioni degli anelli favorevoli influenzano le proprietà degli isomeri configurazionali. Ricorda, gli stereoisomeri configurazionali sono stabili e non si interconvertono facilmente, mentre gli isomeri conformazionali normalmente si interconvertono rapidamente. Nell’esaminare le possibili strutture per i cicloesani sostituiti, è utile seguire due principi:
(i) Le conformazioni delle sedie sono generalmente più stabili di altre possibilità.
(ii) I sostituenti sui conformatori della sedia preferiscono occupare posizioni equatoriali a causa dell’aumento dell’ostacolo sterico delle posizioni assiali.
Le seguenti equazioni e formule illustrano come la presenza di due o più sostituenti su un anello cicloesano sconvolga l’interconversione dei due conformatori della sedia in modi che possono essere previsti.
Nel caso di cicloesani 1,1-disostituiti, uno dei sostituenti deve necessariamente essere assiale e l’altro equatoriale, indipendentemente dal conformatore della sedia considerato. Poiché i sostituenti sono gli stessi in 1,1-dimetilcicloesano, i due conformatori sono identici e presenti in uguale concentrazione. In 1-t-butil-1-metilcicloesano il gruppo t-butile è molto più grande del metile, e quel conformatore di sedia in cui il gruppo più grande è equatoriale sarà favorito nell’equilibrio( > 99%). Di conseguenza, il gruppo metilico in questo composto è quasi esclusivamente assiale nel suo orientamento.
Nei casi di composti 1,2 -, 1,3-e 1,4-disostituiti l’analisi è un po ‘ più complessa. È sempre possibile avere entrambi i gruppi equatoriali, ma se ciò richiede una relazione cis o una relazione trans dipende dalla posizione relativa dei sostituenti. Mentre contiamo intorno all’anello dal carbonio #1 al #6, il legame più alto su ogni carbonio cambia il suo orientamento da equatoriale (o assiale) ad assiale (o equatoriale) e viceversa. È importante ricordare che i legami su un dato lato di una sedia anello-conformazione si alternano sempre in questo modo. Pertanto, dovrebbe essere chiaro che per cis-1,2-disostituzione, uno dei sostituenti deve essere equatoriale e l’altro assiale; nel trans-isomero entrambi possono essere equatoriali. A causa della natura alternata dei legami equatoriali e assiali, la relazione opposta è vera per 1,3-disubstitution (cis è tutto equatoriale, trans è equatoriale/assiale).
Infine, 1,4-disubstitution ritorna al modello 1,2:
L’analisi di cui sopra non è qualcosa che dovresti provare a memorizzare: piuttosto, diventa comodo con il disegno del cicloesano nella conformazione della sedia, con i legami che puntano nelle direzioni corrette per i sostituenti assiali ed equatoriali. Se riesci a disegnare correttamente una struttura nella conformazione della sedia, dovresti sempre essere in grado di determinare quali posizioni sono assiali e quali sono equatoriali.