Claisen Rearrangement
Il Claisen rearrangement (da non confondere con la condensazione di Claisen) è una potente reazione chimica di formazione del legame carbonio–carbonio scoperta da Rainer Ludwig Claisen nel 1912. Il riscaldamento di un etere vinilico allilico avvierà un riarrangiamento a-sigmatropico per dare un γ, δ-carbonile insaturo.
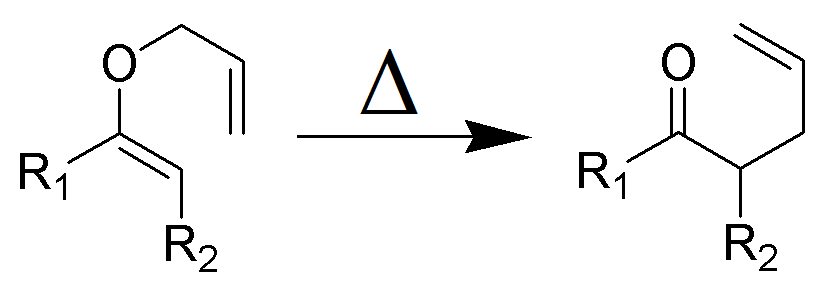
Figura 1: Wikimedia (Opera propria) – riarrangiamento sigmatropico.
Il riarrangiamento di Claisen è una reazione periciclica esotermica, concertata (scissione del legame e ricombinazione). Le regole di Woodward–Hoffmann mostrano una via di reazione stereospecifica soprafacciale. La cinetica è del primo ordine e l’intera trasformazione procede attraverso uno stato di transizione ciclico altamente ordinato ed è intramolecolare. Gli esperimenti crossover eliminano la possibilità che il riarrangiamento avvenga attraverso un meccanismo di reazione intermolecolare e sono coerenti con un processo intramolecolare.
Nel riarrangiamento di Claisen si osservano notevoli effetti solvente, dove i solventi polari tendono ad accelerare la reazione in misura maggiore. I solventi che legano l’idrogeno hanno dato le costanti di tasso più alte. Ad esempio, le miscele di etanolo/acqua solvente danno costanti di velocità 10 volte superiori al sulfolano. È stato dimostrato che i reagenti trivalenti di organoalluminio, come il trimetilalluminio, accelerano questa reazione.
Il primo riarrangiamento di Claisen riportato è il riarrangiamento-sigmatropico di un etere allilfenilico all’intermedio 1, che si tautomerizza rapidamente in un fenolo orto-sostituito.
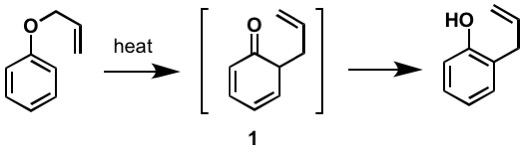
Figura 2: Di Kchemyoung (Proprio lavoro) , via Wikimedia Commons
Riarrangiamento Irlanda-Claisen
Il riarrangiamento Irlanda–Claisen è la reazione di un carbossilato allilico con una base forte (come il litio diisopropilammide) per dare un acido carbossilico γ,δ-insaturo. Il riarrangiamento procede tramite sililchetene acetale, che si forma intrappolando l’enolato di litio con clorotrimetilsilano. Come il Bellus-Claisen (sopra), il riarrangiamento Irlanda-Claisen può avvenire a temperatura ambiente e oltre. L’E-e Z-configurato silylketene acetali portano a anti e syn riarrangiati prodotti, rispettivamente. Ci sono numerosi esempi di riarrangiamenti enantioselettivi Irlanda-Claisen trovati in letteratura per includere reagenti al boro chirale e l’uso di ausiliari chirali.
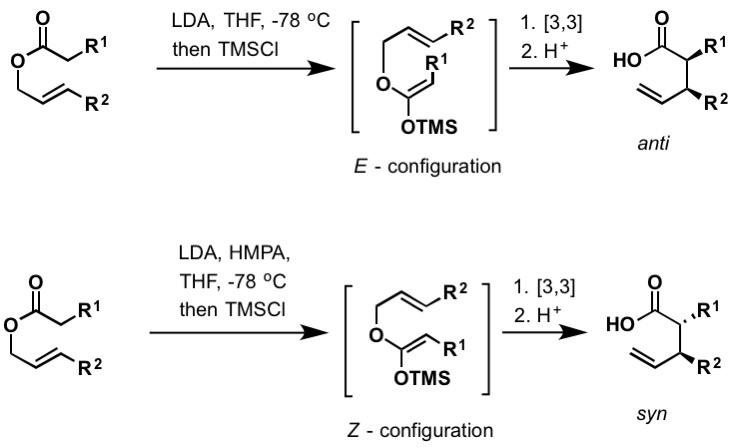
Figura 5: Immagine utilizzata con autorizzazione (CC BY-SA 4.0; Kchemyoung)
Riarrangiamento di Johnson–Claisen
Il riarrangiamento di Johnson–Claisen è la reazione di un alcool allilico con un orto per produrre un estere γ,δ-insaturo. Gli acidi deboli, quale acido propionico, sono stati usati per catalizzare questa reazione. Questo riarrangiamento richiede spesso temperature elevate (da 100 a 200 °C) e può richiedere da 10 a 120 ore per essere completato. Tuttavia, il riscaldamento a microonde assistito in presenza di KSF-argilla o acido propionico ha dimostrato drammatici aumenti della velocità di reazione e delle rese.
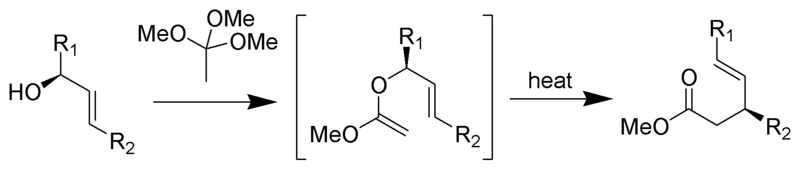
Meccanismo:
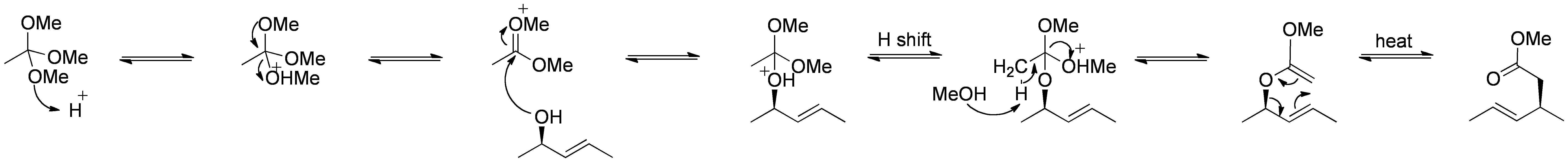
Da Self Made di RAN 10 ( – ), via Wikimedia Commons
Riarrangiamento di Foto-Claisen
Il riarrangiamento di foto-Claisen è strettamente correlato al riarrangiamento di foto-Fries, che procede attraverso un meccanismo radicale simile. Gli eteri arilici subiscono il riarrangiamento foto-Claisen, mentre il riarrangiamento foto-Fries utilizza esteri arilici.
Etero-Claisens
Aza-Claisen
Un iminio può servire come una delle parti legate al pi nel riarrangiamento.
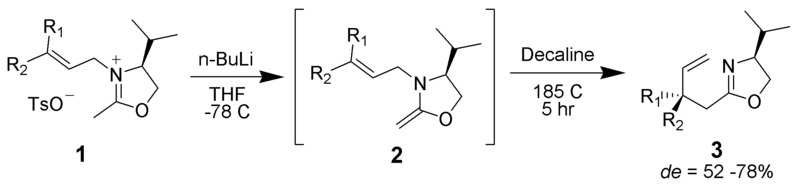
Da nessun autore leggibile dalla macchina fornito. ~ K assunto (sulla base di rivendicazioni di copyright). , via Wikimedia Commons
Ossidazione del cromo
Il cromo può ossidare alcoli allilici a chetoni alfa-beta insaturi sul lato opposto del legame insaturo dall’alcol. Questo avviene attraverso una reazione etero-Claisen concertata, anche se ci sono differenze meccanicistiche poiché l’atomo di cromo ha accesso agli orbitali d – shell che consentono la reazione sotto un insieme meno vincolato di geometrie.
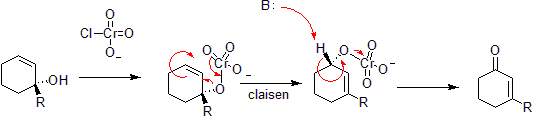
Con l ” uploader originale era Takometer a Wikipedia inglese-Phosphorimidate Riarrangiamento o reazione Staudinger-Claisen installa un fosfito al posto di un alcool e sfrutta la riduzione Staudinger per convertire questo in un immine. Il Claisen successivo è guidato dal fatto che un doppio legame P=O è più energeticamente favorevole di un doppio legame P=N.
.png?revision=1&size=bestfit&width=660&height=112)
Da Howcheng a it.wikipedia, via Wikimedia Commons
Overman riarrangiamento
Overman riarrangiamento (dal nome Larry Overman) è un riarrangiamento Claisen di tricloroacetimidati allilici a tricloroacetamidi allilici.
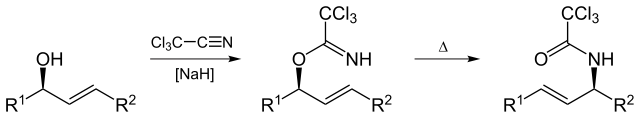
Da Yikrazuul (Proprio lavoro) , via Wikimedia Commons
Overman riarrangiamento è applicabile alla sintesi di vicinol diamino comp da 1,2 diolo allilico vicinale.
Riarrangiamento zwitterionico di Claisen
A differenza dei riarrangiamenti tipici di Claisen che richiedono il riscaldamento, i riarrangiamenti zwitterionici di Claisen avvengono a temperatura ambiente o inferiore. Gli ioni acilammonio sono altamente selettivi per gli Z-enolati in condizioni miti
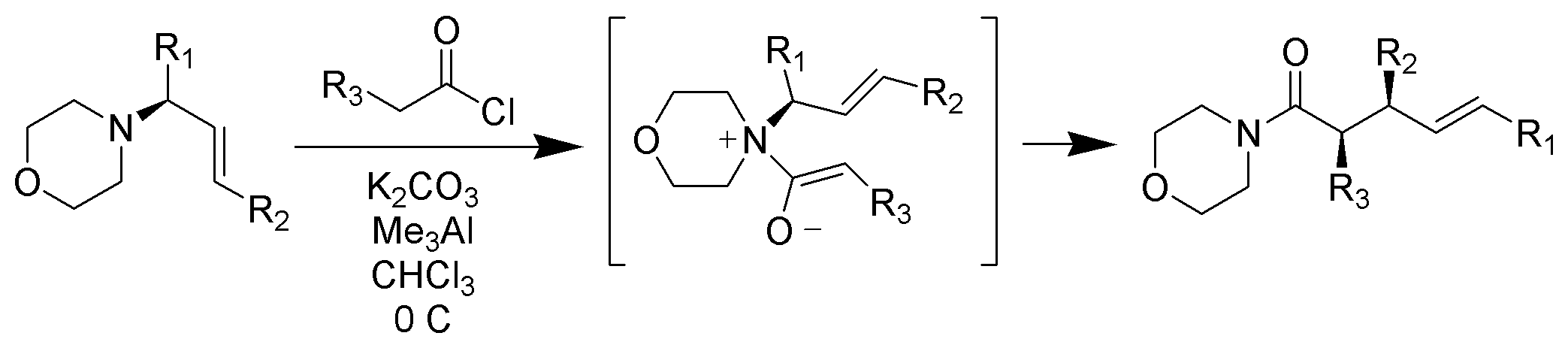
https://upload.wikimedia.org/wikiped…ent_Scheme.png
Claisen riarrangiamento in natura
L’enzima Corismato mutasi (EC 5.4.99.5) catalizza il riarrangiamento di Claisen dello chor corismato in pre prefenato, un intermedio chiave nella via dell’acido shikimico (la via biosintetica verso la sintesi di fenilalanina e tirosina).
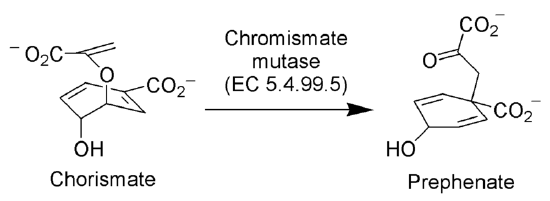
Da nessun autore leggibile dalla macchina fornito. ~ K assunto (sulla base di rivendicazioni di copyright). , via Wikimedia Commons