Classificazione del sangue umano / Immunologia
PUBBLICITÀ:
Il sangue umano può essere classificato in diversi sistemi di gruppo sanguigno, ad esempio gruppo sanguigno ABO, gruppo sanguigno MN e gruppo sanguigno Rh.
Tutti questi gruppi sanguigni nell’uomo sono sotto controllo genetico, ogni serie di gruppi sanguigni è sotto il controllo di geni in un singolo locus o di geni che sono strettamente collegati e si comportano in eredità come se fossero in un singolo locus.
- Gruppo sanguigno ABO:
- Genetica del gruppo sanguigno ABO:
- Sottodivisioni dei gruppi sanguigni A, AB e B:
- Modalità di Ereditarietà:
- Particolari Casi Genetici di Gruppo Sanguigno ABO:
- Gruppi sanguigni MN:
- Fattore Rh:
- Importanza clinica:
- Dettagli sul fattore Rh:
- Controllo genetico della struttura antigenica:
- Un confronto schematico dei concetti di Wiener e Fisher-Race:
- Il concetto di Weiner di Rh:
- Il concetto Fischer-Race di Rh:
- Eredità di Sangue Rh Fattori:
- Significato dello sviluppo del corretto concetto delle relazioni genetiche degli antigeni Rh:
Gruppo sanguigno ABO:
Se consideriamo le reazioni immunitarie in relazione al gruppo sanguigno ABO, scopriamo che alcuni di essi contengono anticorpi “naturali” contro altri.
PUBBLICITÀ:
Segue l’anticorpo contenuto di gruppo sanguigno ABO:

allo stesso modo, se consideriamo la presenza di antigene nei globuli rossi del sangue di diverso gruppo sanguigno ABO persone, poi troviamo:
a Causa della presenza di diversi antigeni e anticorpi nel sangue, gruppi A, B,
PUBBLICITÀ:
AB e O, tutti i tipi di sangue non possono essere mescolati tra loro a causa della loro reazione di agglutinazione come segue:

Quando una trasfusione di sangue è fatto, non fa male se il donatore di sangue contiene anticorpi contro il destinatario per il donatore di sangue è di piccole quantità rispetto al volume totale del destinatario e, pertanto, gli anticorpi sono diluiti.
Ma farebbe del male se il sangue del ricevente avesse gli anticorpi, poiché ora la quantità di anticorpi è relativamente grande. Una persona del gruppo sanguigno O, ad esempio, non potrebbe essere ricevente di sangue da nessun altro gruppo tranne il suo, poiché il suo siero agglutina tutti i corpuscoli tranne il suo, anche se potrebbe essere un donatore per qualsiasi gruppo poiché il sangue di nessuno contiene anticorpi contro i suoi corpuscoli.
Genetica del gruppo sanguigno ABO:
Non sappiamo quale dei quattro gruppi sanguigni sia quello normale. Nella genetica è generalmente accettato che gli individui con tratti normali siano i più numerosi che in tutti gli altri. Per una più facile comprensione, se consideriamo il gruppo O come normale, allora il gruppo A e B è sorto dal gruppo O come risultato di due mutazioni dominanti (una per ogni gruppo), al gene mutante possono essere dati i simboli A e B, rispettivamente. Entrambi questi geni sono sorti nello stesso locus da uno dei geni normali nel gruppo O.
Se designiamo il gene normale usando il simbolo +, allora tre geni +. A e B occupano lo stesso locus e sono alleli multipli. Poiché il gene + è recessivo, quindi il gruppo O deve essere omozigote per +/+, e poiché i geni mutanti A e B sono dominanti, quindi le combinazioni per un gruppo A/A o +/A e allo stesso modo per il gruppo B, B/B o +/B. Il gruppo sanguigno AB, d’altra parte, è sempre l’ibrido
, A/B (Questo è un esempio dell’espressione fenotipica della co-dominanza).
Alcuni genetisti hanno anche proposto che l’ereditarietà del gruppo sanguigno A, B, AB e O nell’uomo sia determinata da una serie di tre geni allelomorfi di cui i per nessuno degli antigeni, IA per l’antigene A, IB per l’antigene B. IA & IB mostra una dominanza completa su i.
Sottodivisioni dei gruppi sanguigni A, AB e B:
PUBBLICITÀ:
I corpuscoli di sangue di un gruppo sanguigno sono stati suddivisi in due sottogruppi noti come A1 e A2 ma di questi due sottogruppi A2 è meno comune. È stato trovato che i corpuscoli A1 non sono agglutinati dal siero A2, né viceversa; ma sia i corpuscoli A1 che A2 sono agglutinati dal siero B e dal siero O.
È stato inoltre osservato che sono stati identificati altri due sottogruppi di A (ad eccezione di A1 e A2) che sono A3 e A4ma entrambi questi gruppi sono più rari di A2. Ciascuno dei sottogruppi A è determinato da un gene separato e i geni per tutti e quattro i sottogruppi sono alleli.
Allo stesso modo, il siero del gruppo B contiene almeno due tipi di anticorpi, uno agglutina i corpuscoli di entrambi i gruppi A1 e A2 e altri agglutina solo A1. Gruppo sanguigno AB è stato anche diviso in A1B, A2B, A3B e A4B.
Così, il gene ‘I’ e un multiplo allele (che determina la produzione dell’antigene) e in grado di produrre 15 genotipi e 10 fenotipi dei gruppi sanguigni, che sono:
Modalità di Ereditarietà:
Se entrambi i genitori in una determinata famiglia di sangue O di gruppo, tutti i bambini devono avere O gruppo di sangue come i loro genitori. Se d’altra parte, entrambi i genitori sono di un gruppo ed entrambi sono stati ibridi (A/+), potrebbero avere alcuni bambini con gruppo sanguigno O.
Quindi, in questo modo, se conosciamo i gruppi sanguigni di un bambino e di sua madre, possiamo legittimamente rivendicare o testare il probabile gruppo sanguigno del padre del bambino.
tabella che Segue è la sintesi medicolegal applicazione dei gruppi sanguigni :
PUBBLICITÀ:
PUBBLICITÀ:
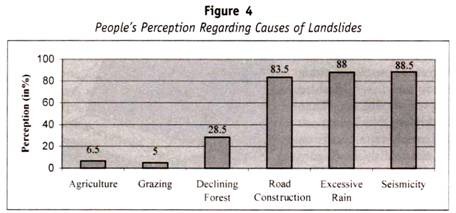
La tabella che segue (tabella 13.1) è la modalità di eredità di sangue di gruppo per i bambini dai genitori:
Particolari Casi Genetici di Gruppo Sanguigno ABO:
E ‘stato’ trovato che alcune persone hanno antigeni A o B nelle loro secrezioni del corpo anche (da occhi, naso, ghiandola salivare e ghiandola mammaria) e sono noti come secretori. Le persone che sono secretori hanno antigene idrosolubile che può passare dai globuli rossi del sangue e quindi è presente nelle secrezioni del corpo.
Ma in caso di non secretori, gli antigeni sono solo solubili in alcool e non possono essere sciolti nelle secrezioni. Quindi, i secretori possono essere identificati mediante test sul sangue e sulle secrezioni del corpo. Questo tratto secretore è ereditato come un gene dominante ‘ S ‘mentre il tratto non secretore è ereditato dall’allele recessivo omozigote’s’. È stato stimato che quasi il 77% delle popolazioni degli Stati Uniti sono secretori.
Allo stesso modo, un altro antigene noto come antigene “H”, identificato anche sugli eritrociti che può essere dimostrato da agglutinazioni da siero anti-H. Si ritiene che questo antigene sia un intermedio tra l’antigene A e B. Il gene dominante H è responsabile della produzione di antigene H e i geotipi sono i seguenti :
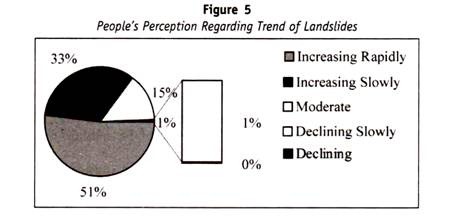
È interessante notare che gli individui il cui sangue non dà alcuna reazione con Anti-A o Anti-B o Anti-H appartengono a un gruppo molto raro e sono noti come” fenotipo di Bombay”, perché è stato descritto per la prima volta in un gruppo molto piccolo di persone nella città di Bombay.
Gruppi sanguigni MN:
I corpuscoli sanguigni di persone diverse possono contenere uno o l’altro, o entrambi M e N e questi antigeni non hanno alcuna relazione con i gruppi sanguigni ABO. Cioè una persona del gruppo sanguigno A potrebbe appartenere a uno qualsiasi dei tre gruppi sanguigni (M, N o MN) MN. Il gene responsabile della produzione di antigeni M e N è dominante e sono alleli.
PUBBLICITÀ:
L’eterozigote per il gene M e N ha mostrato la co-dominanza. Tuttavia, queste tre classi (M, N e MN) non si verificano in semplice rapporto mendeliano nella popolazione generale e la percentuale di ogni classe varia da una razza all’altra. Il gruppo sanguigno di MN non ha importanza nella trasfusione di sangue ma ha importanza medicolegal per esempio prova di paternità. La seguente tabella (Tabella 13.2) mostra il test di paternità per il gruppo sanguigno MN.
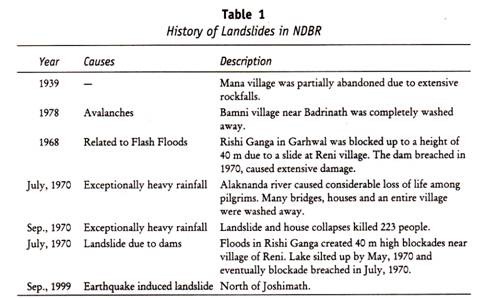
Fattore Rh:
Un agglutinogeno importante è stato dimostrato (1940) nei globuli rossi umani anche da Landsteiner e Wiener. È agglutinogeno della scimmia Rhesus ed è presente nell ‘ 85% dei bianchi. Anche se le informazioni sono limitate, tuttavia si è constatato che tra gli indiani e ceylonese, la percentuale è ancora più grande (circa il 95% o più). Non c’è agglutinina corrispondente nel plasma umano.
Studi recenti indicano che il fattore Rh non è una singola entità. Ci sono sei agglutinogeni Rh-C, c; D, d; E, e; di questi, D e osare il più comune. Questi due forniranno tre sottogruppi: D, Dd e d. D è dominante mendeliana, mentre d è recessiva. Quindi, i gruppi D e Dd (collettivamente chiamati gruppo D) saranno Rh positivi (Rh+) e d saranno rh negativi (Rh~). Praticamente tutte le persone Rh positive appartengono al gruppo D e le persone rh negative al gruppo d.
Importanza clinica:
1. Se il sangue Rh+ viene trasfuso in un paziente Rh”, un fattore anti-Rh si svilupperà nel sangue del paziente in circa 12 giorni. Se una seconda trasfusione dello stesso sangue viene somministrata a tale paziente dopo questo periodo, avrà luogo l’emoagglutinazione dei corpuscoli del donatore. In altre parole, il sangue che prima era compatibile è diventato incompatibile ora. In modo che, prima della trasfusione, il test per il fattore Rh dovrebbe essere fatto con attenzione.
2. Durante la gravidanza il feto può essere Rh + mentre la madre Rh -. L’agglutinogeno Rh (leggermente presente anche nel plasma) dal feto passa nel sangue materno e stimola la formazione del fattore Anti-Rh. Questo anticorpo entra nel sangue fetale e distrugge i globuli rossi del feto. Il feto può morire (causando aborto spontaneo) o, se nato vivo, soffre di grave anemia. Questa malattia è nota come eritro-blastosi fetale.
3. Tale madre diventa sensibilizzata al fattore Rh. In futuro, se riceve una trasfusione di sangue altrimenti compatibile ma contenente fattore Rh, avrà luogo l’agglutinazione.
4. Per lo stesso motivo, una donna Rh”, prima della menopausa, non dovrebbe ricevere trasfusioni di sangue Rh+. Perché nel caso in cui lei rimane incinta con il feto Rh positivo, il problema come descritto sotto no. (2) diventerà ancora più acuto.
Le agglutinine specifiche non sono presenti nel plasma fetale. Ma le agglutinine materne, filtrate attraverso la placenta, si trovano nel plasma fetale. Solo il 50% dei neonati mostra una quantità apprezzabile di questa agglutinina.
Le agglutinine specifiche iniziano a comparire da circa il 10 ° giorno dopo la nascita e salgono al massimo a circa il 10 ° anno. Le agglutinine, come altri anticorpi, si trovano nella frazione globulina del siero. Sono presenti anche in basse diluizioni nei fluidi corporei ricchi di proteine, come latte, essudati linfatici e trasudati. Non si trovano nelle urine e nel liquido cerebrospinale. Le emoagglutinine aumentano temporaneamente durante la malattia da siero e sono ridotte nella leucemia.
Come altri anticorpi, la concentrazione di agglutinina specifica varia a tutte le età da uomo a uomo e anche nello stesso individuo in condizioni diverse. Agiscono meglio a una temperatura più bassa.
Il gruppo sanguigno di un particolare soggetto è di carattere fisso e non varia con l’età o la malattia.
Nel sangue possono talvolta comparire agglutinine aspecifiche che agiscono a freddo (a 0°-5°C o F) e non a temperatura corporea. Queste agglutinine fredde possono a volte essere sufficientemente elevate da causare autoagglutinazione a temperatura corporea. Per questo motivo può esserci emolisi intravascolare che porta ad emoglobinuria (emoglobinuria parossistica).
Dettagli sul fattore Rh:
1. Agglutinogeni Rh:
Ci sono tre coppie di agglutinogeni Rh C, c; D, d; ed E, e; C, D ed E sono dominanti mendeliani e c, d ed e sono recessivi.
2. Globuli rossi umani (RBC):
R. B. C. porterà sempre tre agglutinogeni – uno da ogni coppia, ma non porteranno mai entrambi i membri di qualsiasi coppia. Quindi ODE, CDe e cDE sono possibili ma cDC e CDd non lo sono.
3. Gruppi Rh (genotipi):
Ne consegue, quindi, che ci sono 8 combinazioni possibili, ognuna delle quali può essere portata da entrambi i genitori. Quindi, matematicamente, ci sono 64 combinazioni possibili (genotipi). Di questi 28 essendo identici, 36 sottogruppi sono biologicamente disponibili. Di questi, solo 5 si trovano comunemente, vale a dire, CDe/CDe, CDe/cDe, CDe/cde, cDe/cde e cde/cde. Altri sono rari.
4. Rh + e Rh – gruppi:
Questi gruppi contenenti gli agglutinogeni dominanti—cioè, C, D, E-saranno Rh+. Ma poiché C ed E raramente rimangono senza D, praticamente tutti i casi Rh + contengono D, cioè appartengono a
gruppo D. I casi Rh conterranno gli agglutinogeni recessivi-c, d ed e e per ragioni simili state4 sopra appartengono al gruppo d. Ogni uomo porta un po ‘ di agglutinogeno Rh. La maggioranza ha D e sono di Rh+. Il resto portano d e sono di Rh- . Tutte le reazioni incompatibili con Rh sono dovute alle interazioni tra il gruppo D (donatore) e il gruppo d (ricevente).
5. Anticorpo Rh:
a) Ciascuno dei sei agglutinogeni ha proprietà antigeniche, cioè possono stimolare la formazione di anticorpi. Gli anticorpi corrispondenti sono noti come Anti-C, Anti-D, ecc. D è fortemente antigenico, altri sono molto deboli.
b) Se le cellule D vengono ripetutamente iniettate in un soggetto Rh”, si svilupperà Anti-D. Questo anticorpo può essere di due tipi: “precoce”e ” tardivo”. L’Anti-D precoce si forma per primo e si chiama anticorpo completo. Può agglutinare le cellule D in vitro, quando sono sospese in soluzione salina o albumina. Quindi, è anche noto come agglutinina salina. L’Anti-D tardivo si forma più tardi e si chiama anticorpo incompleto.
Può agglutinare le cellule D in vitro, quando sono sospese solo in soluzioni di albumina e non in soluzioni saline. Quindi è anche chiamato agglutinina di albumina. Ma in quest’ultimo caso, anche se le cellule D non sono agglutinate, tuttavia sono in qualche modo modificate. Perché, queste cellule, una volta trattate in questo modo, non saranno agglutinate dal siero Anti-D precoce, anche quando sono sospese in soluzione di albumina. Quindi, l’Anti-D tardivo è anche conosciuto come l’anticorpo di blocco.
c) Come accennato in precedenza, D è fortemente antigenico. Essa provoca la formazione di Anti-D anche per iniezione intramuscolare; in modo che ripetute iniezioni intramuscolari di sangue intero — come spesso fatto nella pratica medica senza corrispondere i gruppi sanguigni — non è necessariamente una procedura sicura. Pertanto, la corrispondenza incrociata diretta prima di ciascuna di queste imprese è l’unica garanzia più sicura.
6. Distribuzione razziale:
Scrivi persone-85% Rh+, di cui D – 35%, Dd – 48% e il restante 2% contengono anche D insieme ad altri agglutinogeni. Indiani, Ceylonese – 95% Rh+, giapponesi circa 100% Rh+ Quindi, in quest’ultimo, le reazioni di incompatibilità Rh sono estremamente rare.
7. Malattia emolitica del neonato:
Questa malattia è dovuta alla distruzione del Rh+ R. B. C. nel feto da un’agglutinina Anti-Rh, presente, nel siero della madre, che ha filtrato attraverso la placenta durante la gravidanza. L’incompatibilità tra il sangue di madre e figlio è causata dall’eredità del fattore Rh. La seguente tabella (Tabella 13.3) indica le probabilità del gruppo Rh nel bambino.
In questa malattia la distruzione del R. B. C. normale porta alla presenza di R. B. C. nucleato anormale in circolazione. Poche ore dopo la nascita c’è anemia, ittero acuto e sintomi correlati.
Importanza del gruppo sanguigno:
1. Trasfusione.
2. Alcune malattie del sangue.
3. Test di paternità.
4. In medicina legale.
5. Studi etnologici.
6. Studi antropologici.
7. Vari scopi sperimentali.
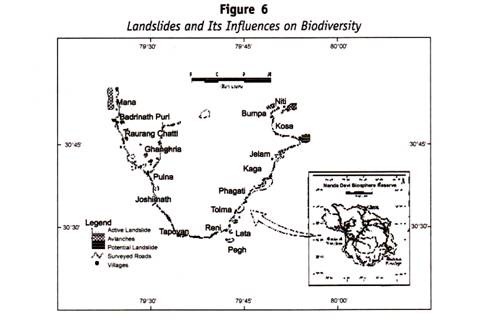
L’incompatibilità del sangue può sorgere solo nei casi contrassegnati da asterisco ( * )-poiché in questi due gruppi la madre è in grado di produrre un’agglutinina Anti-Rh per distruggere il RH+ R. B. C. presente nel feto.
Controllo genetico della struttura antigenica:
Gli antigeni Rh:
I due gruppi indipendenti di geni del gruppo sanguigno allelico discussi finora sono esempi relativamente semplici del controllo genetico delle sostanze del gruppo sanguigno. Un ultimo caso sarà presentato in dettaglio per illustrare la situazione più complessa nell’uomo che è stata resa intelligibile attraverso una comprensione delle relazioni tra geni e antigeni.
Questo caso è quello delle sostanze rhesus, che rappresentano una serie di antigeni ereditati indipendentemente dagli antigeni MN e ABO e che sono determinati da geni che si verificano su un’altra coppia di cromosomi. La serie di antigeni deriva il suo nome, Rh, dalla scimmia rhesus (Macaca mulatta), in cui il primo membro della serie è stato scoperto da Landsteiner e Vincitore nel 1940.
Levine e Stetson (1939) avevano stabilito che la malattia emolitica dei neonati chiamata eritroblastosi fetale era dovuta all’isoimmunizzazione delle madri a un antigene sconosciuto sui globuli rossi dei loro bambini. Poco dopo la descrizione degli antigeni Rh, Levine, Katsin e Burnham (1941) scoprirono che questo era l’antigene responsabile della malattia che stavano studiando.
Queste scoperte iniziano un’indagine intensiva degli antigeni Rh che ha continuato da allora. Questa indagine non solo ha fornito una soluzione a molti problemi associati alla malattia, ma ha notevolmente avanzato i concetti sulla natura dell’eredità delle sostanze che raggruppano il sangue in generale.
Sono state avanzate due ipotesi principali per spiegare il meccanismo genetico che controlla gli antigeni Rh. Uno di questi, proposto da Wiener, postula una serie di alleli in un singolo locus m una coppia di cromosomi diversi da quelli che trasportano altri geni per il gruppo sanguigno antigeni.
L’altro di questi, avanzato da Fisher e Race, concorda con quanto sopra nell’affermare che i geni coinvolti sono sulla propria coppia cromosomica, ma non è d’accordo nel fatto che postula tre coppie di alleli strettamente collegati a tre loci separati.
Si ritiene che il legame coinvolto sia così stretto che si verificano cross-over con frequenze così basse che non sono mai state osservate. Sfortunatamente, le previsioni genetiche di queste due ipotesi sono vive in così tanti dei loro aspetti che non è stato ancora possibile stabilire con finalità quale sia corretta.
Un confronto schematico dei concetti di Wiener e Fisher-Race:
Uno dei punti fondamentali in questione è se esiste o meno una relazione uno-a-uno tra il numero di tipi di anticorpi Rh che una cellula combinerà con e il numero di tipi di geni che determinano le specificità antigeniche responsabili di questa combinazione.
Questo punto è illustrato considerando le cellule (di un individuo geneticamente omozigote) in grado di combinarsi con tre diversi tipi di anticorpi, anti-1, anti-2 e anti-3. L’ipotesi di Weiner avrebbe permesso il concetto che tutti e tre gli anticorpi si stavano combinando con diverse porzioni di una singola molecola di antigeni, le cui specificità complesse erano determinate da un singolo tipo di gene.
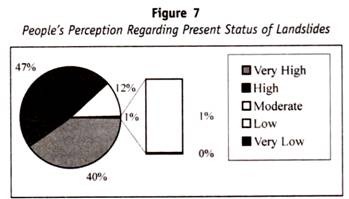
L’ipotesi Fisher – Race non permetterebbe questo concetto, ma visualizza ogni anticorpo che si combina con una molecola di antigene con una sola specificità, determinata da un singolo gene. Il diagramma di accompagnamento delinea la natura del contrasto tra questi due concetti.

Si dovrebbe prestare particolare attenzione al punto che il concetto di Wiener non è in conflitto con la relazione un gene-un antigene di cui all’inizio di questo capitolo. Piuttosto, è facilmente concepibile che l’antigene determinato da un singolo gene possa avere una struttura topografica complessa che indurrà e combinerà con più di un tipo di anticorpo in modo analogo a quello osservato nello studio degli antigeni” artificiali”; In altre parole, il concetto di una relazione uno-a-uno tra un gene e la specificità antigenica che è il suo prodotto non richiede affatto una relazione uno-a-uno tra questa specificità antigenica e gli anticorpi che genera.
Il concetto di Weiner di Rh:
Il concetto di Weiner postula una serie di base di 8 geni allelici (membri aggiuntivi sono stati aggiunti a questa serie, ma questi non devono essere considerati qui), due dei quali possono verificarsi in un singolo individuo eterozigote. Ognuno di questi geni determina un antigene in grado di indurre e combinare con uno a tre (e più) tipi di anticorpi.
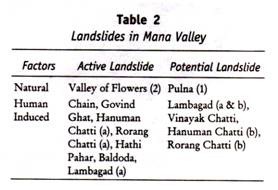
Le specificità antigeniche coinvolte si verificano in varie combinazioni, determinate dal particolare allele responsabile di un dato antigene. (Gli anticorpi utilizzati in questa ricerca sono generalmente ottenuti da esseri umani isoimmunizzati, volontari o madri che hanno un bambino affetto da malattia emolitica; I simboli di Wiener per i vari geni, gli antigeni che determinano e le reazioni di questi antigeni agli antisieri selezionati si trovano nella Tabella 13.4. Tale gene è scritto come singola lettera, seguita da un apice, mentre l’antigene che ciascuno determina è scritto come due lettere seguite da un pedice o apice. I vari antigeni saranno ora considerati.

Il simbolo Rho è in maiuscolo perché rappresenta il primo antigene Rh che è stato scoperto e che rimane ancora il più significativo nella malattia emolitica. I simboli rh ‘e rh” stanno per antigeni aggiuntivi successivamente trovati. I simboli Rh1 e Rh2 rappresentano antigeni complessi costituiti da due specificità. Rhj è composto dalle unità Rho e rh’; Rh2 è composto dalle unità Rho e rh”. I simboli aggiuntivi Rhz e rhy rappresentano antigeni con specificità multiple come indicato. Il simbolo rh richiede un commento speciale.
Originariamente questo simbolo rappresentava l’assenza di specifiche antigeniche note (cioè Rh0, rh’ e rh”). Tuttavia, la scoperta di due nuovi tipi di antisieri ha rivelato l’esistenza di due ulteriori tipi di specificità antigeniche. Questi si verificano in varie combinazioni con le altre specificità appena descritte.

Il primo di questi antisieri, originariamente trovato da Levine e dai suoi collaboratori, identifica una specificità ora chiamata hr ‘che si verifica su tutte le cellule prive della specificità rh’. Il secondo di questi identifica una specificità denominata hr “che si verifica su tutte le cellule prive della specificità rh”. (La controparte antigenica dell’antigene Rh0, Hr0, deve ancora essere identificata con certezza.) Questa situazione storicamente complicata ha portato al riconoscimento del simbolo rh come rappresentante di un antigene complesso con specificità hr’ e hr”.
Inoltre, i due nuovi antisieri hanno esteso la descrizione degli altri simboli Rh. Queste relazioni sono riportate nella Tabella 13.5. Per capire questi (e quelli già presentati nella Tabella 13.4) lo studente deve preparare alcuni diagrammi simili a quelli mostrati in precedenza, sostituendo i simboli di Wiener ai numeri utilizzati.
Per riassumere lo schema di Wiener, i cinque antisieri qui considerati consentono di rilevare cluster variabili di una serie di specificità antigeniche (individualmente definite fattori ematici) che insieme dal gruppo sanguigno Rh di una determinata persona. Questi cluster passano di generazione in generazione, la loro continuità specifica e strutturale è determinata dal particolare allele di cui sono il prodotto. Un’ulteriore considerazione dell’eredità di questi fattori è data in una sezione successiva.
Il concetto Fischer-Race di Rh:
Il concetto Fischer-Race ha la sua origine nell’intuizione analitica del genetista e matematico britannico R. A. Fischer. Egli propose, in un suggerimento presentato da Race nel 1944, che gli antigeni Rh allora noti potessero essere considerati come i prodotti dell’azione di una serie di tre coppie di alleli strettamente collegati, ogni gene in ogni coppia producendo un singolo antigene con la capacità di indurre e reagire con un solo tipo di anticorpo.
Le coppie alleliche di geni proposti sono stati simboleggiati come C, c; D, d; ed E, e. Ciascuno è stato tenuto a produrre un antigene distinto designato dalla stessa lettera. Nessuna dominanza è implicita dall’uso di lettere maiuscole e minuscole, queste selezionate semplicemente per mostrare il loro allelismo.
Le relazioni formalizzate di questi diversi geni sui cromosomi di un individuo eterozigote per tutti loro è:
CDE / cde
Altre combinazioni di tre alleli su cromosomi particolari naturalmente si verificano, ad esempio, C D e, c D E, C d e, ecc. (alcune autorità scrivono la sequenza di lettere coinvolte come D. C. E in riconoscimento di considerazioni genetiche di collegamento e possibile cancellazione; queste tuttavia, sono considerazioni non pertinenti qui.)
Nel momento in cui è stato stabilito il concetto di razza Fisher, gli antisieri erano noti per gli antigeni C, c; D; ed E. Sono stati previsti gli antisieri aggiuntivi, per gli antigeni d ed e, di cui l’anti-e è stato ora stabilito con certezza.
Inoltre, l’esistenza del cromosoma c (d) E allora sconosciuto è stata prevista e successivamente trovata. Il successo di queste previsioni, così come la relativa semplicità della terminologia e dei concetti coinvolti, hanno portato ad un’ampia accettazione dello schema Fisher-Race, specialmente tra i medici e i ricercatori europei.
In sintesi, il concetto britannico riconosce una serie di cromosomi che trasportano diverse combinazioni di C, D, E allelles molto strettamente legate. Queste combinazioni sono tenute a sorgere come risultato di crossing over, così poco frequenti da non essere stati rilevati.
Il simbolo D corrisponde a quello di Rho, e ulteriori paralleli nelle due terminologie sono mostrati nella Tabella 13.6. Allo stesso modo, i due insiemi di simboli per i cinque tipi di Rh-anticorpi possono essere correlati come segue:

Eredità di Sangue Rh Fattori:
è evidente che, in assenza di una posizione dominante, mutazione attraversando, e epistosis (nessuno dei quali ha ancora trovato a verificarsi durante il corso di studi genetici su antigeni Rh), l’Rh del sangue fattori riapparirà di generazione in generazione come caratteristica cluster.
Ad esempio, un incrocio tra un padre di genotipo R2r (CDE/cde) e una madre di genotipo ϒR” (Cde/cdE) può potenzialmente produrre quattro tipi di bambini, come è facilmente dimostrato attraverso l’uso del quadrato di Punnett:

Due, tra i bambini mostrati, possederebbero l’antigene RhofD) che manca alla loro madre. Nell’uso classico dei termini Rh, la loro madre sarebbe “Rh negativo” mentre sarebbero “Rh positivo”. Questo esempio mostra anche che la definizione di positività Rh e negatività è relativa che deve essere fatta in termini di antigeni coinvolti.
In teoria, ogni bambino che possiede antigeni Rh che manca alla madre è positivo rispetto a questi antigeni, mentre sua madre è negativa rispetto a loro. In pratica, tuttavia, l’antigene Rho(D) è stato trovato per essere il più frequentemente coinvolto nella malattia emolitica, con rh'(C) il prossimo, gli altri fattori del sangue sono molto meno frequentemente implicati.
Significato dello sviluppo del corretto concetto delle relazioni genetiche degli antigeni Rh:
Le sezioni precedenti hanno dimostrato che i sistemi di nomenclatura di Weiner o Fisher-Race possono essere usati per descrivere gli antigeni e gli anticorpi Rh. Questo punto è riconosciuto dall’Istituto Nazionale della Sanità che richiede che entrambi i sistemi siano applicati all’etichettatura degli antisieri prodotti commercialmente.
Tuttavia ciò non dovrebbe distogliere l’attenzione dalla necessità di determinare la validità dell’uno o dell’altro concetto alla base di questa nomenclatura, anche se questo può sembrare “accademico” e non di interesse diretto nel lavoro clinico.
Una sola ragione per la necessità di continui sforzi per risolvere questo problema è che, come spesso già notato, gli antigeni sembrano essere i prodotti diretti dei geni che li producono. Gli anticorpi che inducono diventano quindi, a causa delle loro sottili specificità, gli indicatori più sensibili delle variazioni nell’azione genica che sono noti.
Ciò rende indispensabile che si arrivi ad un accurato schema concettuale che metta in relazione la produzione di antigeni con quegli schemi che si stanno evolvendo riguardo alla relazione dei geni con gli enzimi e della struttura degli acidi nucleici con il “codice genetico” utilizzato nella trasmissione ereditaria di-messaggi”.
La considerazione dettagliata di queste relazioni si trova ben oltre lo scopo di questo testo, il lettore interessato viene riferito ai ” racconti popolari di Crick, Gamow e Beadle per un’introduzione alle storie coinvolte.
Stomont ha riassunto le ragioni di una crescente tendenza da parte di diversi genetisti di spicco a favorire il concetto di Wiener, nonostante la sua terminologia più difficile. Il suo riassunto, troppo avanzato per presentare qui, si basa su paralleli tra il comportamento degli antigeni Rh negli esseri umani e le serie B e C di alleli che determinano i tipi di sangue nei bovini.
Queste serie di alleli controllano di gran lunga la più complessa matrice di fattori ematici noti, una matrice le cui relazioni possono essere ragionevolmente spiegate solo in termini di alleli multipli piuttosto che in serie di geni collegati. Ulteriori dettagli riguardanti i gruppi sanguigni del bestiame sono forniti più avanti in questo capitolo. Race e Sanger e Levine presentano discussioni e ulteriori riferimenti del punto di vista di Fisher.
Lo studente dovrebbe rendersi conto che i principali sostenitori di entrambi gli schemi hanno condotto ricerche che raramente sono state eccelse negli annali della biologia e che le risoluzioni sperimentali delle loro differenze non saranno né facili né banali.