7.5: Kompleks IV
Kompleks IV jest końcowym celem w łańcuchu transportu elektronów. Tutaj elektrony, które podróżowały przez innych członków superkompleksu oddechowego, są ostatecznie dostarczane do O2, redukując go do wody. To imponujący wyczyn, ponieważ wiele reaktywnych form tlenu musi powstać między początkowym dodatkiem elektronu a ostatecznym uwolnieniem wody, ale reakcja jest kontrolowana w taki sposób, że możliwość uszkodzenia komórki jest zminimalizowana. W tym samym czasie więcej protonów jest pompowanych przez wewnętrzną błonę mitochondrialną.
- w kompleksie IV elektrony są dostarczane do miejsca przeznaczenia, cząsteczki O2.
- O2 zostaje zredukowane do wody.
ćwiczenia \(\PageIndex{1}\)
napisz zrównoważoną połowę reakcji redoks, aby pokazać, ile elektronów jest potrzebnych do redukcji cząsteczki tlenu do wody.
odpowiedź
O2 → H2O
O2 → 2 H2O (Zbalansowany)
O2 + 4H+ → 2 H2O (Zbalansowany)
O2 + 4e- + 4h+ → 2 H2O (Zbalansowany))
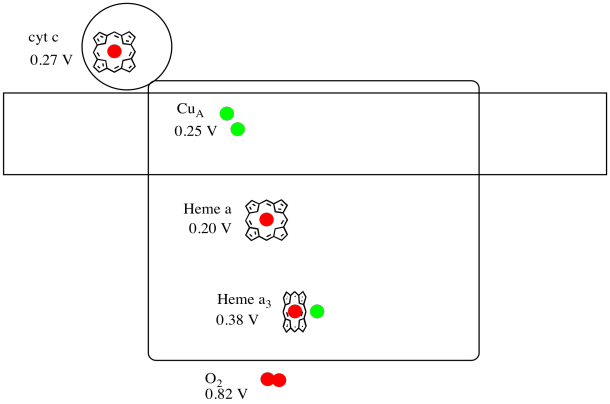
strukturę rentgenowską kompleksu IV przedstawiono poniżej. Ponownie, macierz znajduje się na dolnym końcu obrazu, a przestrzeń międzybłonowa na górze. Tam, na górze, dokuje cytochrom C.
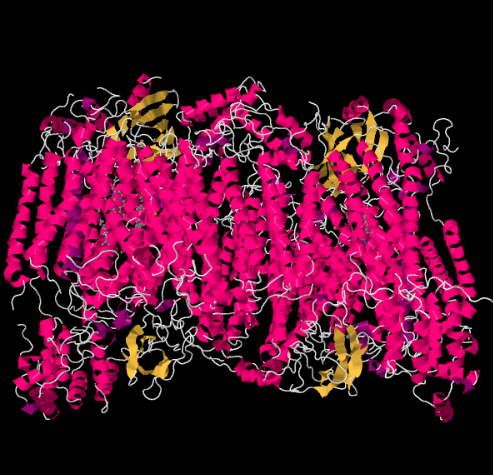
mobilny nośnik elektronów, cytochrom c, wiąże się w kompleksie IV i dostarcza elektron do dwujądrowego miejsca miedziowego zwanego CuA. Możemy zobaczyć tę dwujądrową witrynę miedzi, kiedy spojrzymy wewnątrz białka, poniżej. Jest związany tylko z białkiem i niczym innym, więc widzimy dwa jony miedzi same w sobie na górze obrazu. Ta para atomów miedzi wysyła elektron na Hem, cytochrom a, który można zobaczyć poniżej i po lewej stronie. Stamtąd elektron przechodzi do innego klastra dwujądrowego, tym razem składającego się z żelaza związanego hemem (cytochrom a3) i pobliskiej miedzi (CuB). Miejsce to prowadzi redukcję dioksygenu do wody. W strukturze znajduje się cząsteczka tlenku węgla związana w miejscu aktywnym między cytochromem a3 a CuB. Atomy węgla są przyłączone do żelaza, a tlen do miedzi. Tam wiązałaby się cząsteczka tlenu, czekając, aż zostanie zredukowana do wody.
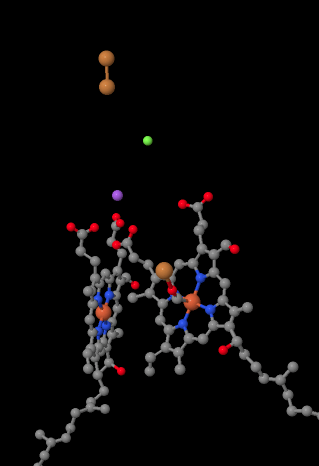
jeśli się nad tym zastanowić, oznacza to, że elektrony poruszają się w przeciwnym kierunku niż to, co widzieliśmy w pierwszych trzech kompleksach. W kompleksach I I II elektrony były dostarczane z matrycy mitochondrialnej i podróżowały w górę w kierunku przestrzeni międzybłonowej, zatrzymując się w ubichinonie w błonie mitochondrialnej. W kompleksie III elektrony podążały w tym kierunku “w górę”, od błony mitochondrialnej do cytochromu c w przestrzeni międzybłonowej. W kompleksie IV elektrony cofają się w kierunku macierzy mitochondrialnej. Pamiętajcie, macierz mitochondrialna jest domieszkowana przez pompowanie protonów, więc te elektrony przemieszczają się z dodatniej strony błony na ujemną. To musi być trudne.
- w kompleksie IV transport elektronów znajduje się w przeciwnym kierunku niż pozostałe kompleksy.
- elektrony przemieszczają się od strony przestrzeni międzymięśniowej do strony macierzy mitochondrialnej, wbrew gradientowi ładunku.
przyjrzyjmy się jeszcze raz ważnym ligandom dla kompleksu. Kreskówka jest pokazana poniżej. W kreskówce cząsteczka O2 jest pokazana jako wiążąca w tej pozycji między hem a3 a CuB. To miejsce, w którym cząsteczka tlenu jest zredukowana do wody.
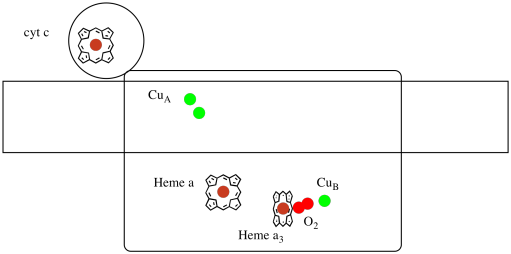
ponieważ cztery elektrony są potrzebne do redukcji O2 do H2O, cztery cząsteczki cytochromu c muszą wiązać się w kompleksie IV, zanim redukcja będzie mogła nastąpić. Jest prawdopodobne, że środowisko koordynacyjne cząsteczki tlenu-pomiędzy dwoma metalami, a nie tylko związane z jednym-pozwala na szybsze zredukowanie go do wody, a nie Tworzenie reaktywnych form tlenu, które utrzymują się w komórce, takich jak nadtlenki.
ćwiczenia \(\PageIndex{2}\)
Załóżmy, że żelazo w Hem A3 zaczyna się w stanie zredukowanym Fe (II), a CuB zaczyna się w stanie zredukowanym Cu(I). Zapewniają mechanizm redukcji tlenu do wody, z dodatkiem czterech elektronów i czterech protonów. Użyj Fe (II) jako dawcy elektronów i lizyny jako dawcy protonów.
Odpowiedz
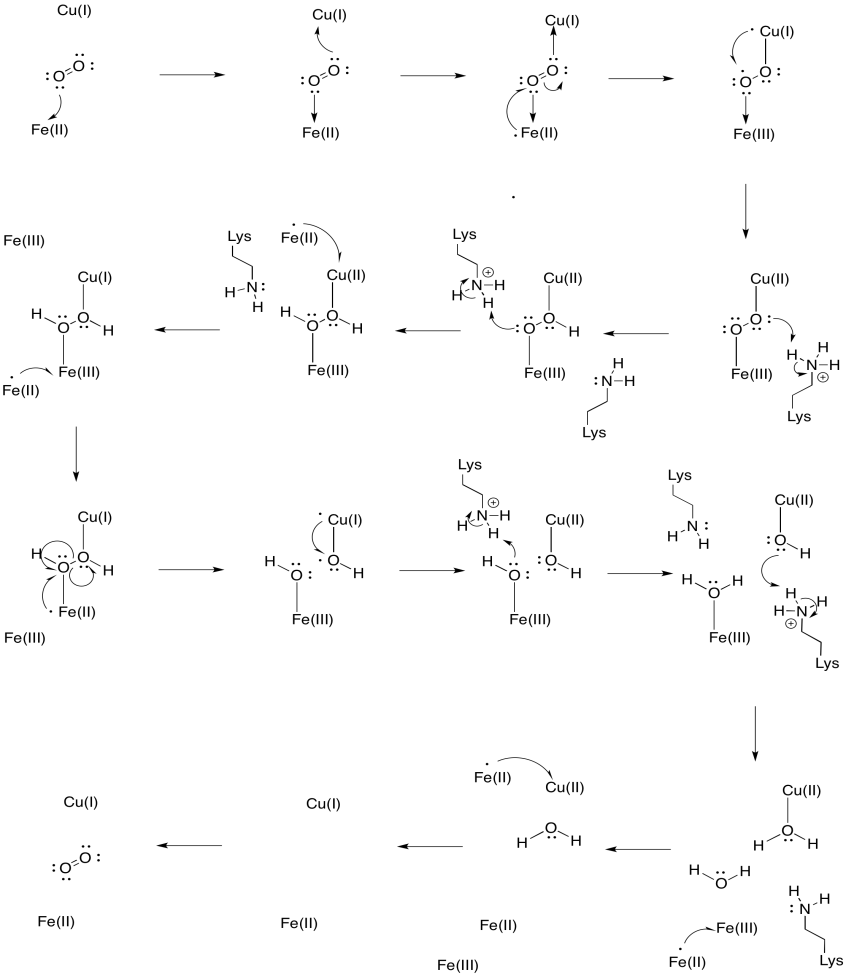
oprócz tych dwóch metali, istnieje również zmodyfikowany koniugat histydyny-tyrozyny związany z CuB. Zasugerowano, że ta tyrozyna stanowi inne źródło natychmiastowych elektronów, które można wykorzystać w redukcji.
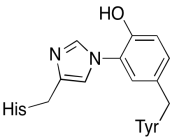
ćwiczenia \(\PageIndex{3}\)
Pokaż, dlaczego tyrozyna może być źródłem zarówno protonu, jak i elektronu w procesach biochemicznych.
Odpowiedz
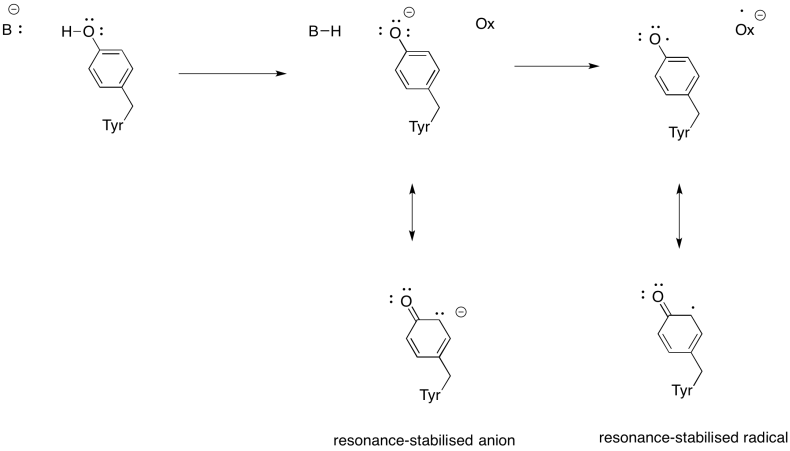
oprócz konieczności redukcji tlenu do wody, Kompleks IV przyczynia się również do gradientu protonów, pompując dodatkowe protony przez błonę mitochondrialną. To zadanie stawia dodatkowe wyzwania. Prosty mechanizm sprzęgania nie jest możliwy, ponieważ elektrony poruszają się w przeciwnym kierunku. Jest jednak, że mechanizm obejmuje zmiany konformacyjne w białku, które występują jak metale zmienić stany utleniania. Subtelne zmiany w środowisku koordynacji mogą spowodować przemieszczenie się reszt aminokwasowych w pobliżu. Łatwo sobie wyobrazić, że jeśli dany aminokwas przesunie się w górę w kierunku przestrzeni międzybłonowej, może pociągnąć za sobą proton.
- pompowanie protonów i transport elektronów przebiegają w przeciwnych kierunkach w kompleksie IV i muszą być odłączone.
- pompowanie protonów w kompleksie IV musi polegać na zmianach konformacyjnych.
ćwiczenia \(\PageIndex{4}\)
na terenie CuA znajdują się dwa coppery, otoczone przez dwie cysteiny pomostowe. Oba są połączone terminalnymi histydynami. Ponadto jedna miedź jest związana dodatkową metioniną, podczas gdy druga jest związana karbonylem ze szkieletu białka.
- narysuj gliniarzy w ich miejscach wiązania.
- opisz geometrię każdej miedzi.
- jeśli każda miedź jest Cu (I), jaka jest skoordynowana liczba elektronów na każdej miedzi w kompleksie?
- jeśli każda miedź jest Cu (I), jaki jest ogólny ładunek na kompleksie?
Odpowiedz a)
a)
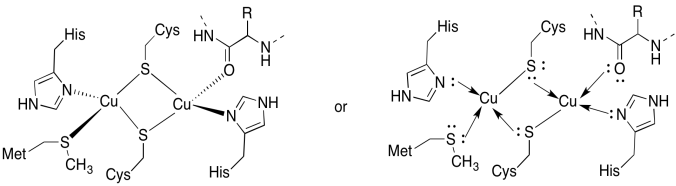
odpowiedź b)
B)
odpowiedź C)
C) Cu (I) = d10
4 x cu ( I) = 2+
2 x Cys-S- = 2-
wszystkie inne neutralne
Razem = 0
ćwiczenia \(\PageIndex{5}\)
miedź w miejscu szczepienia jest związana przez dwie histydyny i koniugat histydyny-tyrozyny.
- narysuj miedź w miejscu wiązania.
- jeśli miedź jest Cu (I), jaka jest skoordynowana liczba elektronów w kompleksie?
- jeśli miedź jest Cu (I), jaki jest ogólny ładunek na kompleksie?
Odpowiedz a)
a)
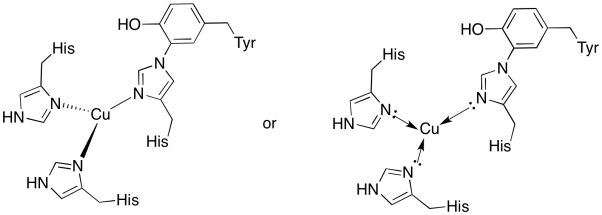
odpowiedź b)
B) trygonalna planarna
odpowiedź C)
C) Cu(I) = d10
365 = 6 E-
razem = 16 E-
odpowiedź D)
d) Cu (I) = 1+
histydines neutral
Total = 1+
ćwiczenia \(\PageIndex{6}\)
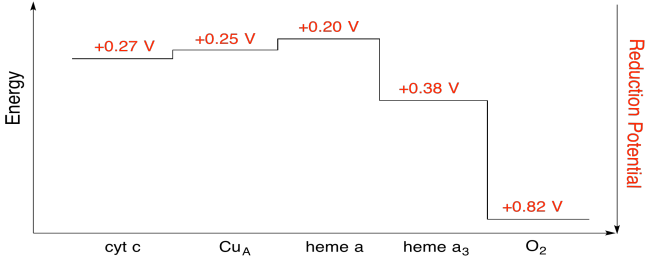
trudno jest zmierzyć potencjał redukcji pojedynczego miejsca w obrębie białka. Jednak naukowcy byli w stanie oszacować te wartości, mierząc widma EPR w różnych warunkach. Zakładając potencjały redukcji poniżej, narysuj diagram postępu reakcji dla transportu elektronu przez całą drogę z cytochromu c do tlenu cząsteczkowego.
 Odpowiedz
Odpowiedz
ćwiczenia \(\PageIndex{7}\)
korzystając z wartości na powyższym rysunku, Oblicz zmianę energii, gdy elektron jest przenoszony z hemu a do hemu a3.
odpowiedź
zakładając, że potencjały redukcji wynoszą:
hem A(ox) + e- → hem a(red) Eored = 0,20 V
hem a3(ox) + e- → hem a3(red) Eored = 0.38 V
wtedy różnica potencjałów dla reakcji, ΔEo = 0,38 – (0,20) V = 0,18 V.
zależność Faradaya ΔG = – n F ΔEo daje
ΔG = – 1 x 96,485 J V-1 mol-1 x 0,13 V = 17,367 J mol-1 = 17,4 kJ mol-1
Chris P Schaller, Ph. D., (College of Saint Benedict / Saint John ‘ s University)