Citomegalovírus (CMV) infecção em pacientes com HIV/AIDS e valores de diagnóstico de CMV-detecção de DNA em diferentes tipos de amostras
- Introdução
- métodos
- indivíduos
- inclusão e exclusão
- reagentes e equipamento
- quantificação do VIH-ARN
- Contagem de linfócitos T CD4+
- CMV
- CMV anticorpo test
- métodos de Estudo
- ácido Nucleico de detecção
- Detecção de linfócitos T subconjuntos
- detecção de anticorpos imunes
- a análise estatística
- resultados
- dados gerais
- Positivo taxas de CMV-DNA-CMV-IgG, e CMV-IgM
- correlação entre a infecção por CMV e a contagem de linfócitos T CD4+
- Detecção de CMV-DNA em diferentes amostras
- Discussão
- conclusões
- Agradecimentos
- Rodapé
Introdução
Citomegalovírus (CMV) é um herpesvirus que é generalizada entre as populações humanas. A infecção por CMV geralmente não causa sintomas e afeta principalmente as glândulas salivares, rins e outros órgãos. No entanto, a replicação viral pode ocorrer em doentes imunocomprometidos e pode contribuir para os danos nos órgãos e nas suas funções. As infecções oportunistas são mais frequentes e graves em doentes infectados pelo VIH/SIDA. A infecção pelo vírus CMV é comum nestes pacientes e pode afetar vários órgãos / sistemas, incluindo os olhos, pulmões, sistema nervoso e sistema digestivo. Muitos estudos exploraram as características virológicas e imunológicas da infecção simples por CMV (1), especialmente as encontradas em mulheres e crianças. As características imunológicas da infecção por CMV, no entanto, são bastante únicas em doentes imunocomprometidos com VIH/SIDA. Existem diferenças nas características clínicas, medidas de tratamento, factores de prognóstico entre os doentes infectados pelo VIH com infecção por CMV e os doentes apenas com infecção por CMV (2). A norma orientadora da China recomendou a necessidade imediata de terapêutica antivírica da CMV e da RMA nos doentes infectados pelo VIH/SIDA com complicações (retinite, pneumonia, encefalite por CMV, enterite, etc.) quando a infecção por CMV é identificada. Devido à não especificidade dos sintomas clínicos causados pela infecção por CMV, o exame laboratorial é a principal base para o diagnóstico da infecção por CMV. Mais duas amplamente utilizados métodos clínicos são CMV replicação do vírus e o soro de métodos imunológicos, incluindo a detecção de CMV IgG-CMV IgM e CMV antígeno PP65 (2) Em pacientes com comprometimento da função imunológica, produção de anticorpos para CMV é enfraquecida ou atrasada, o que pode levar a falso-negativos e aumentar a taxa de falta de diagnóstico, para os mesmos PCR detecção de CMV-DNA tem se tornado o método padrão para o diagnóstico de infecção por CMV e a monitorização do tratamento (3). Daisuke Mizushima et al. relatou que a PCR do ADN-CMV plasmático tem um valor importante no diagnóstico tanto da retinite por CMV como de toda a retinite por CMV-EOD em doentes com infecção avançada por VIH-1 (4). CMV-DNA PCR pode ser detectado em uma variedade de tipos de amostra, tais como plasma, urina, líquido cefalorraquidiano, humor aquoso, fezes, etc. (5). No entanto, poucos artigos analisaram e discutiram a significância e o valor da detecção CMV-DNA PCR em amostras que não o plasma. No presente estudo analisámos retrospectivamente os testes laboratoriais (incluindo CMV-ADN, anticorpos CMV, Contagem de linfócitos CD4+ T, carga viral VIH, etc.).) em 808 pacientes com HIV / AIDS que foram tratados em nosso centro de 2017 a 2019 para entender a co-infecção CMV e os pontos fortes e fracos de vários métodos de detecção. Apresentamos o seguinte artigo / caso de acordo com a lista de controlo de relatórios MDAR (disponível em http://dx.doi.org/10.21037/apm-20-1352).
métodos
indivíduos
um total de 808 doentes com HIV/SIDA admitidos no nosso centro entre janeiro de 2017 e outubro de 2019 foram matriculados. O ARN-VIH, a contagem de linfócitos T CD4+, o ADN CMV e os anticorpos relacionados foram medidos em cada doente. O diagnóstico da infecção pelo HIV foi baseado no diagnóstico de HIV/AIDS e orientações de tratamento (terceira edição) (6), e todos os pacientes foram confirmados como infecção pelo HIV pelo Centro Municipal de controle de doenças de Fuzhou (CDC) ou o CDC local que tratou o paciente. O diagnóstico da infecção por CMV baseou-se nos seguintes critérios: I) CMV-ADN positivo no plasma, líquido de lavagem alveolar, urina, líquido cefalorraquidiano (LCR) e/ou outros fluidos corporais; II) CMV-imunoglobulina M (IgM) positiva; III) diagnóstico oftalmológico da retinite por CMV; (IV) CMV pneumonia, principalmente, manifestando-se como febre, tosse, catarro, e aperto no peito; CMV-DNA positivo em alveolar lavagem de fluidos; (V) CMV enterite ou esofagite, principalmente, manifestando-se como disfagia/engolir a dor, diarréia ou dor abdominal e eficaz de diagnóstico anti-CMV de tratamento; (VI) CMV encefalite manifestando-se como sistema nervoso sintomas e CMV-DNA positivo no LCR) ou no tecido cerebral; (VII) CMV hepatite manifestando-se como febre, alteração da função hepática e desconforto na área de fígado, e CMV-DNA positivo na biópsia hepática. Foi feito um diagnóstico de infecção por CMV se algum dos critérios acima, exceto o item (II), foi cumprido ou se o item (II) Mais qualquer outro critério foi cumprido (7).
todos os procedimentos realizados neste estudo envolvendo participantes humanos estavam de acordo com a Declaração de Helsínquia (tal como revista em 2013). O estudo foi aprovado pelo Comitê de Ética Médica do nosso centro (aprovação No. KS2019-070-01). Os dados são anónimos, pelo que a exigência de consentimento informado foi dispensada.
inclusão e exclusão
critérios de inclusão: doentes com VIH / SIDA que visitaram pela primeira vez o Hospital hepatobiliar de Mengchao da Universidade Médica de Fujian e completaram a detecção de VIH-ARN, ADN CMV, anticorpos CMV-IgG, anticorpos CMV-IgM e linfócitos T CD4+ em 14 dias. Excluir casos de HIV / AIDS que não podem completar os itens de teste acima devido ao tamanho insuficiente da amostra.
reagentes e equipamento
quantificação do VIH-ARN
reacção quantitativa em tempo real de polimerização em cadeia (PCR) fluorescente (FQ-PCR) foi realizada no sistema MX3000P QPCR (Agilent, EUA) utilizando o kit de quantificação do VIH-ARN produzido por QiaGen (Shenzhen, China).
Contagem de linfócitos T CD4+
o instrumento utilizado foi o Citómetro de fluxo de FACSCalibur (Biociências BD, EUA), e o kit de reagente utilizado foi o CD3/CD4/CD8/CD45 BD (Biociências BD, EUA).Foi efectuada uma quantificação de ADN-CMV
CMV
FQ-PCR no sistema MX3000P QPCR (Agilent, EUA) para detectar os níveis de ADN-CMV no plasma, na urina e no líquido cefalorraquidiano (CSF). O kit utilizado foi produzido pela Sansure Biotech (Hunan, China).
CMV anticorpo test
Chemiluminescence immunoassay was performed to detect anti-CMV-IgG and IgM antibodies on the Cobas e601 analyzer (Roche Diagnostics, Germany) with the supporting kits (Roche Diagnostics, Germany).
métodos de Estudo
ácido Nucleico de detecção
Após a pacientes com HIV/AIDS foram admitidos para o nosso hospital, 3 mL de jejum ethylenediaminetetraacetic acid (EDTA)-anticoagulados toda a amostra de sangue foi coletada e, em seguida, centrifugado a 3.000 r/min durante 5 minutos para a colheita de 200 µL de plasma para o HIV-RNA e CMV-detecção de DNA. Em todos os doentes, recolheram-se 5 mL de amostra de urina de manhã e misturaram-se cuidadosamente, tendo sido colhidos 200 µL para detecção de ADN CMV. Para doentes com sintomas neurológicos, foi obtido 1 mL de líquido cefalorraquidiano para detecção de ADN CMV. De acordo com o limite de detecção e o padrão de julgamento positivo do kit de ADN CMV e do kit de ARN VIH. As amostras foram consideradas positivas se o valor CMV-ADN fosse superior a 400 cópias/mL, ou se o nível de VIH-ARN fosse superior a 500 cópias/mL.
Detecção de linfócitos T subconjuntos
Em pacientes com HIV/AIDS, 3 mL de EDTA-anticoagulados jejum toda a amostra de sangue foi coletada no momento de admissão e, em seguida, misturado cuidadosamente para linfócitos T subconjunto de detecção de um BD FACSCalibur citometria de fluxo, utilizando os reagentes auxiliares.
detecção de anticorpos imunes
nos doentes infectados pelo VIH/SIDA, 3 mL de amostra de sangue em jejum foram colhidos à entrada, centrifugados a 3000 r/min durante 5 minutos num tubo sérico com separador de gel, e depois testados na máquina.
todos os ensaios acima referidos foram realizados estritamente de acordo com as instruções relativas ao reagente constantes do manual do fabricante e os procedimentos de funcionamento normalizados dos instrumentos.
a análise estatística
a análise estatística foi realizada utilizando software SPSS 21.0. Os dados de medição normalmente distribuídos são apresentados utilizando a média ± desvio-padrão (x ±DP), e os dados não distribuídos normalmente são expressos em mediana (percentis 25-75). Os dados de contagem são expressos em percentagens e taxas. A comparação dos dados de medição não-normalmente distribuídos entre dois grupos foi realizada usando um teste de soma de rank não-paramétrico, enquanto os dados de contagem foram comparados usando o teste de Qui-quadrado. Um valor P <0, 05 foi considerado estatisticamente significativo.
resultados
dados gerais
os dados gerais de 808 doentes com VIH/SIDA estão resumidos na Tabela 1. O sexo e a idade não mostraram diferença significativa entre o grupo CMV e o grupo não CMV. O absoluto de CD4 no CMV-infectados grupo foi significativamente menor do que o CMV não infectados grupo (Z=-8.87, P<0,001), e o HIV-RNA foi significativamente maior no CMV-infectados grupo do que no não-CMV infectado grupo (Z=-3.207, P<0,05) (Tabela 1).
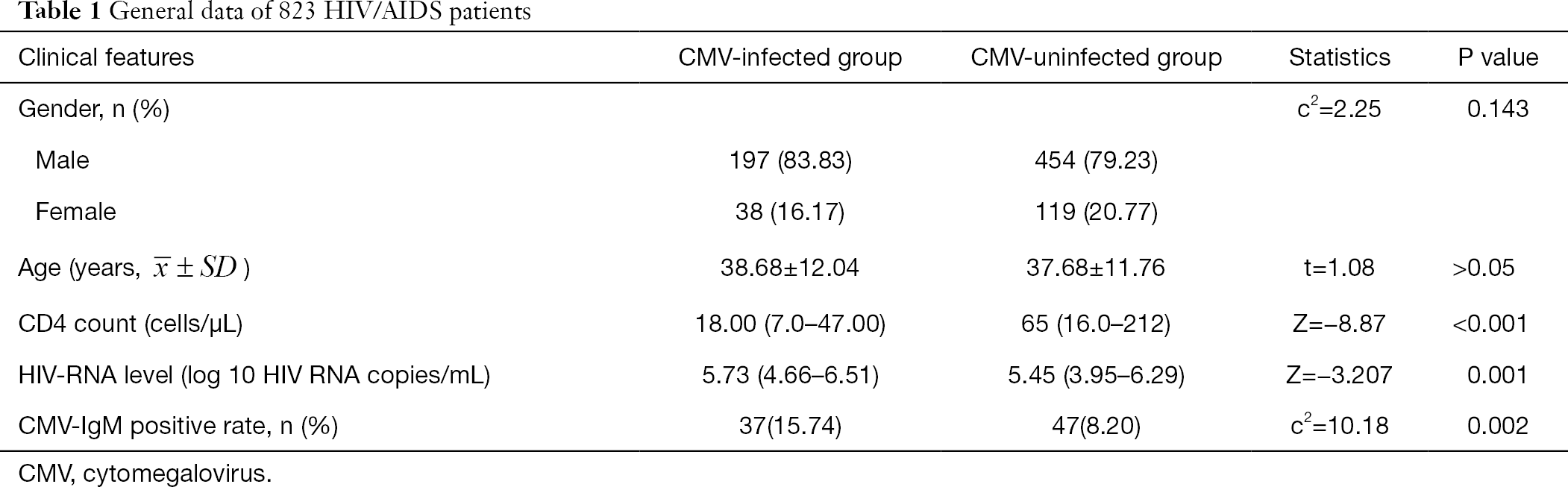
tabela
Positivo taxas de CMV-DNA-CMV-IgG, e CMV-IgM
geral taxa positiva de CMV-DNA foi 29.08% (235/808); especificamente, foi 5.70% (13/228) no QCA 26.01% (77/296) no plasma, e 25.75% (180/699) na urina. A taxa positiva de CMV-IgG foi de 99,8% (806/808), e a taxa positiva de CMV-IgM foi de 10,40% (84/808).
correlação entre a infecção por CMV e a contagem de linfócitos T CD4+
após o agrupamento da contagem de linfócitos CD4+ T, descobrimos que a proporção de doentes infectados com citomegalovírus com baixa frequência de linfócitos CD4+ T era maior do que a dos doentes não infectados por CMV. A incidência de infecção por CMV aumentou com o declínio da contagem de CD4 (Tabela 2).
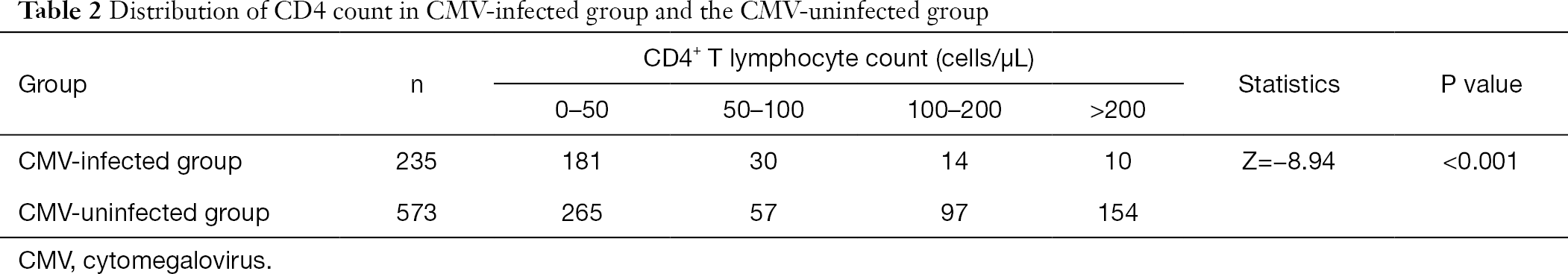
tabela
Detecção de CMV-DNA em diferentes amostras
desses 808 pacientes, 198 pacientes também receberam testes de plasma e na urina CMV-DNA e plasma anti-CMV-IgG e CMV-IgM anticorpos. Utilizando a análise do Qui-quadrado para os dados emparelhados, fizemos comparações emparelhadas entre o CMV-ADN da urina e o CMV-ADN plasmático com o anticorpo CMV-IgM plasmático, respectivamente. Verificou-se que os resultados da urina e plasma CMV-DNA de detecção significativamente diferente do que a do plasma CMV-IgG anticorpos ensaio (P<0.001), enquanto que o resultado de plasma CMV-detecção de DNA não foi significativamente diferente do que a da urina CMV-detecção de DNA (P>0.05) (Tabelas 3,4).

tabela Completa
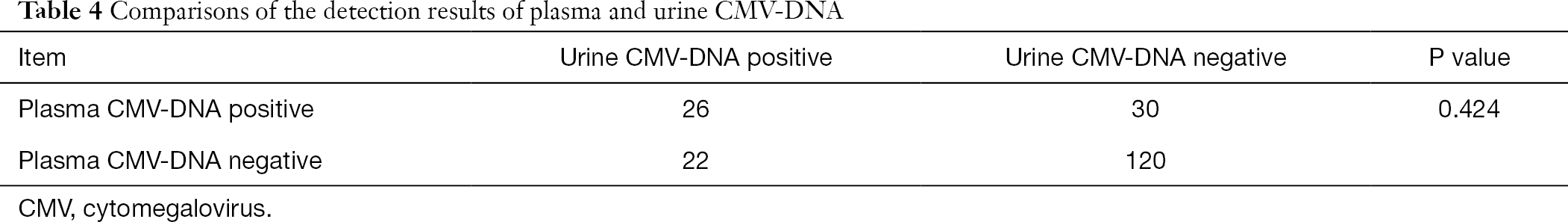
tabela
Discussão
CMV é um membro da β-herpes vírus do grupo e é caracterizada pela sua rigorosa especificidade de espécie e de alta incidência na população humana. A seroprevalência CMV é de cerca de 85% em crianças e até 95% em adultos. No nosso estudo actual, a taxa positiva de CMV-IgG atingiu 99, 8%. CMV é latente na maioria dos casos, mas em indivíduos imunocomprometidos, o vírus se replica exponencialmente e se espalha por todo o corpo com o sangue, causando CMV viremia e até mesmo doença CMV orgânica (8). A infecção por CMV é uma das infecções oportunistas comuns em doentes infectados por VIH/SIDA. Linfócitos T CD4+ são as células alvo do vírus HIV, e suas contagens podem muitas vezes refletir o curso da AIDS e também pode ser usado como um indicador para avaliar o estado imunológico dos pacientes com AIDS. Este estudo analisou a infecção por CMV, a contagem de CD4 e o nível de VIH-ARN em 808 doentes com VIH/SIDA. Descobrimos que a taxa positiva de CMV em pacientes com AIDS aumentou com a diminuição da contagem de CD4 e com o aumento da carga viral do HIV. Também em nosso estudo atual, até 77,02% dos pacientes com CMV positivos tiveram uma contagem CD4 de < 50 células / µL, sugerindo que CD4 < 50 células / µL é um fator de risco para a co-infecção VIH-CMV, o que é consistente com a descoberta de Deng et al. (9). O nível quantitativo de ARN VIH no grupo infectado com CMV foi superior ao do grupo não infectado com CMV, o que sugeriu indirectamente que níveis elevados de carga viral VIH-ARN eram outro factor de risco de infecção por CMV em doentes infectados com VIH/SIDA .Por conseguinte, recomenda-se que os doentes com VIH/SIDA iniciem o tratamento com RMA o mais rapidamente possível para promover a reconstituição imunitária para prevenir infecções oportunistas e o rastreio do VHC é essencial para doentes com VIH/SIDA com uma contagem de CD4 <50 células/µL (2).
também avaliámos os valores dos ensaios de ácido nucleico viral e dos métodos imunológicos na detecção clínica da infecção por CMV. Estudos realizados na China e a nível internacional demonstraram que o ADN-CMV aparece mais cedo do que os sintomas clínicos e as reacções serológicas das infecções por CMV. O FQ-PCR é atualmente o método de quantificação microbiana mais preciso e rápido e é capaz de superar alguns problemas de PCR tradicional (por exemplo, contaminação do produto de amplificação e não quantificação) (10). Em nosso estudo atual,a taxa positiva de DNA CMV foi de 5.70% (13 / 228) nas amostras do LCR de 228 doentes com sintomas neurológicos, o que foi muito inferior ao das amostras de plasma e urina, o que pode ser explicado pela barreira hemato-encefálica e susceptibilidade aos órgãos. O anticorpo anti-CMV-IgM é frequentemente utilizado como marcador de infecção viral activa; no entanto, a taxa positiva do anticorpo anti-CMV-IgM foi de apenas 10, 40% (84/808) nos nossos doentes com VIH/SIDA, o que foi inferior à taxa positiva da infecção CMV notificada nas populações não-VIH / SIDA (11). Além disso, sua taxa positiva teve um fraco acordo com os resultados da detecção de ácido nucleico, que pode ser devido ao sistema imunológico enfraquecido ou devido à geração atrasada de anticorpos IgM em pacientes HIV/AIDS. Assim, a detecção de anticorpos CMV-IgM tem um papel limitado no rastreio HCM em doentes infectados pelo VIH/SIDA. Além disso, a taxa positiva de infecção por CMV em 808 pacientes foi de 29,05% (235/808) em nosso estudo atual, que é ligeiramente superior aos 21,85% relatados por Li et al., e pode ser devido à maior variedade de amostras (incluindo plasma, urina e LCR) coletadas neste estudo (12). A taxa positiva de ADN CMV foi de 25, 57% na urina e 26, 01% no plasma, a diferença não foi estatisticamente significativa. Portanto, recomendamos que o rastreio do ADN-CMV no plasma e na urina seja realizado quando a contagem de linfócitos T CD4+ for inferior a 200 células/µL, especialmente quando <50 células/µL; além disso, é necessária a detecção de ADN-CMV no líquido cefalorraquidiano se estiverem presentes sintomas neurológicos óbvios.
conclusões
em conclusão, a baixa contagem de linfócitos T CD4+ e a elevada carga viral VIH-1 são factores de risco para a infecção por CMV em doentes com VIH/SIDA. A detecção de ADN-CMV da urina ou plasma por FQ-PCR é altamente valiosa no rastreio da infecção por CMV em doentes infectados pelo VIH/SIDA, enquanto a detecção de níveis de IgG e IgM do CMV no sangue tem um valor clínico limitado. Recomenda-se o rastreio do ADN do sangue ou da urina em doentes com SIDA para prevenir e diagnosticar precocemente a infecção por CMV e melhorar a sua qualidade de vida.
Agradecimentos
Financiamento: Patrocinado pela Chave Especialidade Clínica Disciplina Programa de Construção de Fujian, P. R. C.
Rodapé
lista de verificação de Relatórios: Os autores tenham concluído o MDAR lista de verificação de relatórios. Disponível em http://dx.doi.org/10.21037/apm-20-1352
Declaração de partilha de Dados: Disponível em http://dx.doi.org/10.21037/apm-20-1352
conflitos de Interesses: todos os autores preencheram o formulário de divulgação uniforme da ICMJE (disponível em http://dx.doi.org/10.21037/apm-20-1352). Os autores não têm conflitos de interesses a declarar.Declaração Ética: os autores são responsáveis por todos os aspectos do trabalho, garantindo que as questões relacionadas com a exatidão ou integridade de qualquer parte do trabalho sejam adequadamente investigadas e resolvidas. Todos os procedimentos realizados neste estudo envolvendo participantes humanos foram de acordo com a Declaração de Helsinque (revisada em 2013). O estudo foi aprovado pelo Comitê de Ética Médica do nosso centro (aprovação No. KS2019-070-01). Os dados são anónimos, pelo que a exigência de consentimento informado foi dispensada.
open Access Statement: This is an Open Access article distributed in accordance with the Creative Commons Attribution-NonCommercial-NoDerivs 4.0 International License (CC BY-NC-ND 4.0), que permite a replicação e distribuição não-comercial do artigo com a estrita condição de que não sejam feitas alterações ou edições e o trabalho original seja devidamente citado (incluindo links para a publicação formal através do DOI relevante e da licença). Ver: https://creativecommons.org/licenses/by-nc-nd/4.0/.
- Yu X, Tong M, He G. Effects of cytomegalovirus infection on regulatory immune cells in pregnant women Chinese. Journal of Nosocomiology. 2017;27:2103-6.
- o grande projecto nacional de Ciência e Tecnologia apoia o grupo de investigação oportunista de infecções durante o 13. º Plano Quinquenal. Consenso de especialistas em diagnóstico clínico e tratamento da SIDA complicado com a doença por citomegalovírus . Journal of Southwest University( Natural Science Edition): 1-17 .
- Hodowanec AC, Pikis a, Komatsu TE, et al. Tratamento e prevenção da doença CMV em receptores de transplante: conhecimento atual e perspectivas futuras. J Clin Pharmacol 2019; 59: 784-98. Mizushima D, Nishijima T, Yashiro S, et al. Utilidade de diagnóstico da PCR de adn do citomegalovírus plasmático quantitativo para as doenças end-orgânicas do citomegalovírus em doentes com infecção por VIH-1. J Acquir Immune Defic Syndr 2015; 68:140-6. Michaelides a, Liolios L, Glare EM, et al. Aumento da carga de adn do citomegalovírus humano (HCMV) nos leucócitos do sangue periférico após transplante pulmonar correlaciona-se com pneumonite HCMV. Transplantation 2001; 72: 141-7.
- the infection of neurology, AIDS group of Chinese medical association. Orientações para o diagnóstico e tratamento do VIH/SIDA (terceira edição). Chinese Journal of Infectious Diseases 2015; (10): 577-93.
- Corrales I, Giménez e, Solano C, et al. Incidência e dinâmica da infecção activa por citomegalovírus em doentes transplantados de células estaminais alogénicas de acordo com polimorfismos nucleótidos únicos nos genes CCR5, MCP-1, IL-10 e TLR9 do dador e receptor. J Med Virol 2015; 87: 248-55. Tagarro a, Del Valle R, Dominguez-Rodríguez S, et al. Padrões de crescimento em crianças com infecção congénita por citomegalovírus. Pediatr Infect Dis J 2019; 38: 1230-5. Deng X, Liu J, Zhang M, et al. Análise das características virológicas e imunológicas do VIH/SIDA combinada com a infecção por citomegalovírus. Chinese Journal of Hospital Infection 2019; 29: 2241-6.Kawano Y, Kawada J, Kamya Y, et al. Análise de doentes com microRNA viral e humana circulante com infecção congénita por citomegalovírus. J Perinatol 2016; 36: 1101-5.
- Li l, Gao S, Zhang T, et al. Comparação da detecção de ADN e detecção IgM da infecção por citomegalovírus humano e discussão do seu valor de Aplicação combinado. Chinese Journal of Experimental Diagnostics 2015; (1):78-80.
- Li X, Cao L, Yu C, et al. Estudo sobre a infecção por citomegalovírus em doentes com SIDA. Medicina Preventiva Moderna 2012;39:2278-9.
(English Language Editor: J. Gray)