Claisen Rearranjo
O Claisen rearranjo (para não ser confundido com a condensação de Claisen) é um poderoso carbono–carbono bond-formação de reação química descoberto por Rainer Ludwig Claisenin 1912. O aquecimento de um éter alílico vinílico iniciará um rearranjo a-sigmatrópico para dar um carbonilo γ, δ-insaturado.
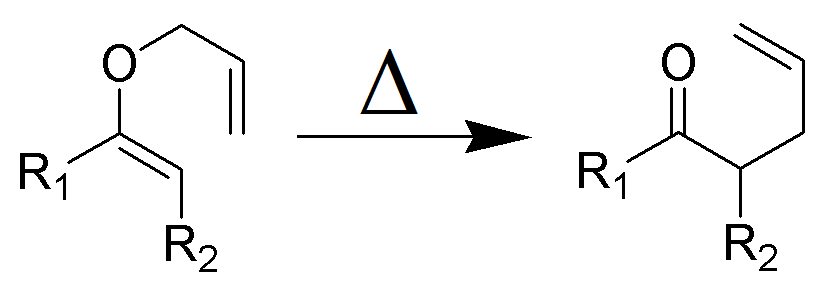
Figura 1: Wikimedia (Own work) – sigmatropic rearranjo.O rearranjo de Claisen é uma reação exotérmica, concertada (clivagem de ligação e recombinação) pericíclico. As regras de Woodward–Hoffmann mostram uma via de reacção estereoespecífica e supra-facial. A cinética é da primeira ordem e toda a transformação procede através de um estado de transição Cíclico altamente ordenado e é intramolecular. Os experimentos Crossover eliminam a possibilidade do rearranjo ocorrer através de um mecanismo de reação intermolecular e são consistentes com um processo intramolecular.
existem efeitos substanciais de solventes observados no rearranjo de Claisen, onde os solventes polares tendem a acelerar a reação em maior extensão. Os solventes de ligação ao hidrogénio deram as constantes de maior velocidade. Por exemplo, as misturas etanol/água com solventes apresentam constantes de taxa 10 vezes superiores ao sulfolano. Reagentes trivalentes organoalumínio, tais como trimetilalumínio, têm sido mostrados para acelerar esta reação.
o primeiro rearranjo Claisen relatado é o rearranjo sigmatrópico de um éter alilfenílico para Intermediário 1, que rapidamente tautomeriza para um fenol Orto-substituído.
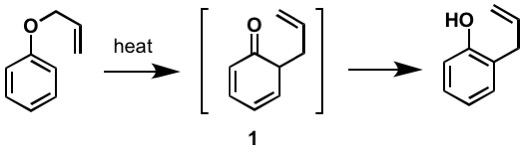
Figura 2: By Kchemyoung (Own work) , via Wikimedia Commons
- o rearranjo Irlanda-Claisen é a reação de um carboxilato alílico com uma base forte (tal como diisopropilamida de lítio) para dar um ácido carboxílico γ,δ-insaturado. O rearranjo prossegue via sililketeno acetal, que é formado por prender o enolato de lítio com clorotrimetilsilano. Como o Bellus-Claisen (acima), o rearranjo Irlanda-Claisen pode ter lugar à temperatura ambiente e acima. Os acetais de sililceteno e Z configurados dão origem, respectivamente, a produtos anti e syn reorganizados. Existem inúmeros exemplos de rearranjos enantiosselectivos Irlanda-Claisen encontrados na literatura para incluir reagentes de boro quiral e o uso de auxiliares quirais.
- Johnson–Claisen rearranjo
- o rearranjo de foto-Claisen está intimamente relacionado com o rearranjo de fotos-Fries, que procede através de um mecanismo radical semelhante. Éteres Aryl passam pelo rearranjo photo-Claisen, enquanto o rearranjo photo-Fries utiliza ésteres arílicos.
- Hetero-Claisens
- Aza–Claisen
- oxidação do crómio
- Overman rearranjo
- rearranjo Claisen Zwitteriónico
- Claisen rearranjo na natureza
o rearranjo Irlanda-Claisen é a reação de um carboxilato alílico com uma base forte (tal como diisopropilamida de lítio) para dar um ácido carboxílico γ,δ-insaturado. O rearranjo prossegue via sililketeno acetal, que é formado por prender o enolato de lítio com clorotrimetilsilano. Como o Bellus-Claisen (acima), o rearranjo Irlanda-Claisen pode ter lugar à temperatura ambiente e acima. Os acetais de sililceteno e Z configurados dão origem, respectivamente, a produtos anti e syn reorganizados. Existem inúmeros exemplos de rearranjos enantiosselectivos Irlanda-Claisen encontrados na literatura para incluir reagentes de boro quiral e o uso de auxiliares quirais.
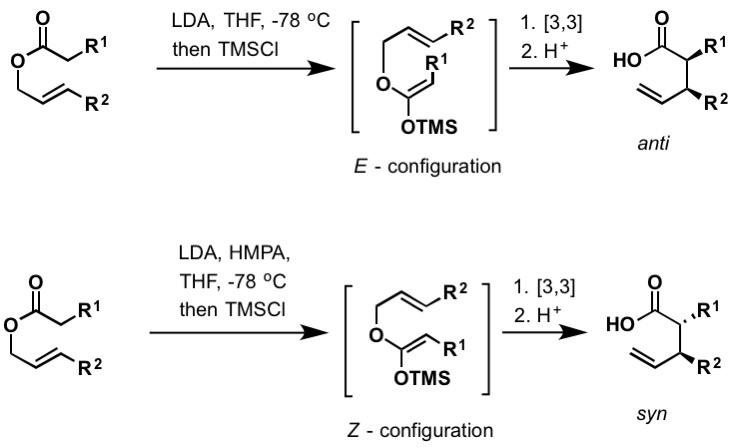
Figura 5: Imagem usada com permissão (CC BY-SA 4.0; Kchemyoung)
Johnson–Claisen rearranjo
Johnson–Claisen rearranjo é a reação de um allylic álcool com um orthoester para produzir um γ,δ-insaturados éster. Ácidos fracos, como o ácido propiónico, têm sido usados para catalisar esta reacção. Este rearranjo muitas vezes requer altas temperaturas (100 a 200 °C) e pode levar em qualquer lugar de 10 a 120 horas para completar. No entanto, o aquecimento assistido por microondas na presença de argila KSF ou ácido propiónico tem demonstrado aumentos dramáticos na taxa de reacção e nos rendimentos.
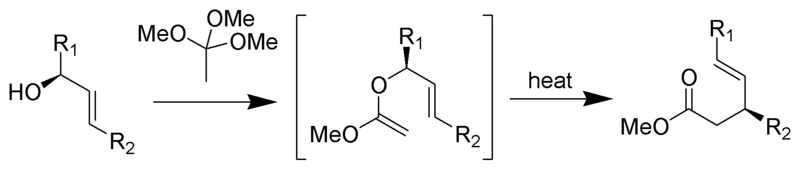
mecanismo:
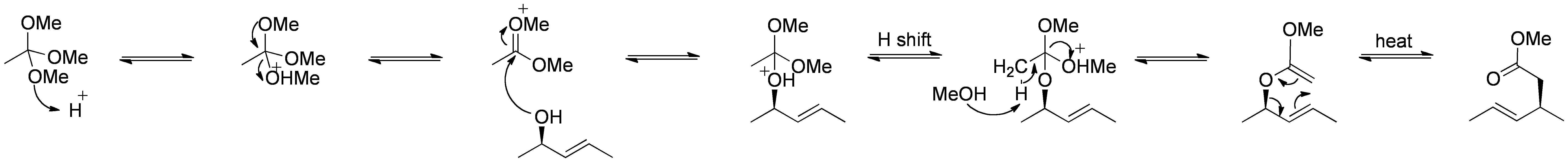
By Self Made by RAN 10 ( – ), via Wikimedia Commons
o rearranjo de foto-Claisen está intimamente relacionado com o rearranjo de fotos-Fries, que procede através de um mecanismo radical semelhante. Éteres Aryl passam pelo rearranjo photo-Claisen, enquanto o rearranjo photo-Fries utiliza ésteres arílicos.
Hetero-Claisens
Aza–Claisen
Um iminium pode servir como um dos pi-ligado metades no rearranjo.
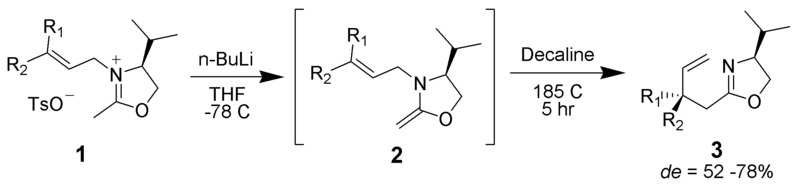
por nenhum autor legível por máquina fornecido. ~K assumido (baseado em direitos de Autor). , via Wikimedia Commons
oxidação do crómio
o crómio pode oxidar álcoois alílicos a cetonas alfa-beta insaturadas do lado oposto da ligação insaturada do álcool. Isto é através de uma reação concertada hetero-Claisen, embora haja diferenças mecanicistas uma vez que o átomo de crómio tem acesso a orbitais de Concha d que permitem a reação sob um conjunto menos restrito de geometrias.
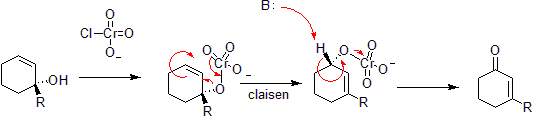
O projeto foi Takometer na Wikipédia em inglês -Phosphorimidate Rearranjo ou Staudinger–Reação de Claisen instala um fosfito no lugar de um álcool e leva vantagem do Staudinger redução para converter um imine. A subsequente Claisen é impulsionada pelo fato de que uma ligação dupla P=O é mais energeticamente favorável do que uma ligação dupla P=N.
.png?revision=1&size=bestfit&width=660&height=112)
By Howcheng at en.wikipédia , via Wikimedia Commons
Overman rearranjo
O Overman rearranjo (em homenagem a Larry Overman) é um rearranjo de Claisen allylic trichloroacetimidates para allylic trichloroacetamides.
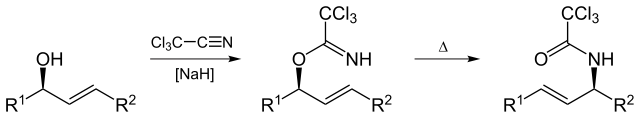
By Yikrazuul (Own work) , via Wikimedia Commons
Overman rearranjo is applicable to synthesis of vicinol diamino comp from 1,2 vicinal allylic diol.
rearranjo Claisen Zwitteriónico
diferentemente dos rearranjos Claisen típicos que requerem aquecimento, rearranjo Claisen zwitteriónico ocorre à temperatura ambiente ou abaixo dela. O acyl íons de amônio são altamente seletivos para Z-enolates em condições brandas
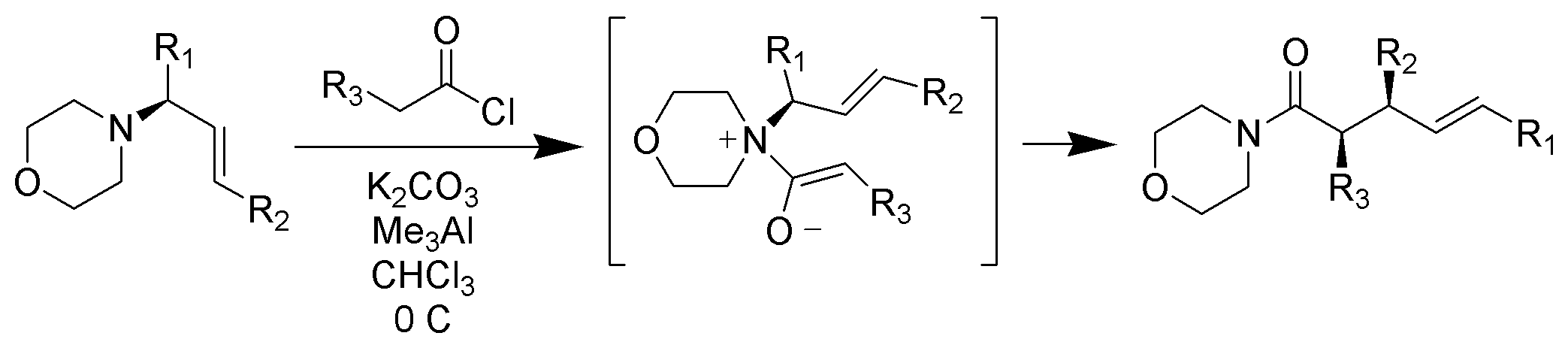
https://upload.wikimedia.org/wikiped…ent_Scheme.png
Claisen rearranjo na natureza
A enzima Chorismate mutase (CE 5.4.99.5) catalisa o rearranjo de Claisen do íon corismato ao íon prefenato, um intermediário chave na Via do ácido xiimico (a via biossintética para a síntese da fenilalanina e tirosina).
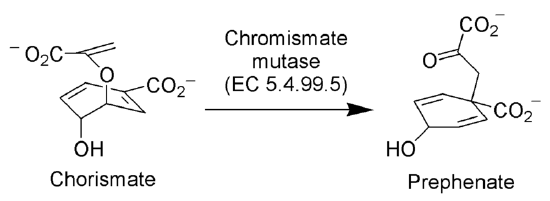
por nenhum autor legível por máquina fornecido. ~K assumido (baseado em direitos de Autor). , via Wikimedia Commons