25.6: koenzym B12 – Vitamin B12
kobalamin, eller Vitamin B12, är den största och mest komplexa av alla typer av vitaminer. Upptäckten av kobalamin gjordes när forskare försökte hitta ett botemedel mot skadlig anemi, en anemisk sjukdom orsakad av frånvaro av inneboende faktor i magen. Kobalamin studerades, renades och samlades i små röda kristaller, och dess kristalliseringsstruktur bestämdes under ett Röntgenanalysexperiment utfört av forskaren Hodkin. En molekylstruktur av kobalamin är enkel, men innehåller många olika sorter och komplex som visas i Figur 1. Undersökningen av vitaminets molekylstruktur hjälper forskare att få en bättre förståelse för hur kroppen använder Vitamin B12 för att bygga röda blodkroppar och förhindra skadliga anemi syndrom.
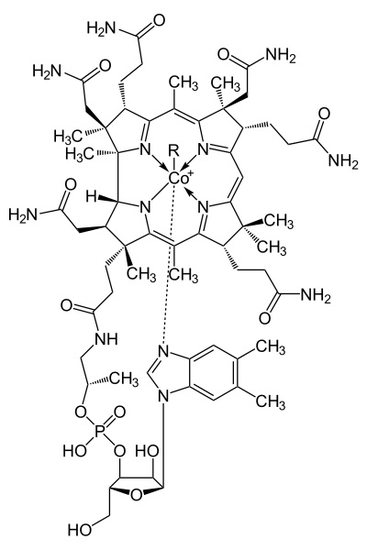
Figur 1
kobalamins metalloenzymstruktur presenterar en korrinring med kobolt, den enda metallen i molekylen, placerad mitt i strukturen med fyra koordinerade kvävebindningar från fyra pyrrolgrupper. Dessa fyra underenhetsgrupper separeras jämnt på samma plan, mittemot varandra. De är också förbundna med varandra genom en C-CH3-metylenlänk på de andra sidorna, genom en C-H på ena sidan och genom att två pyrroler direkt kommer samman. Tillsammans bildar de en perfekt korrinring som visas i Figur 2. Den femte liganden kopplad till kobolt är ett kväve som kommer från 5,6-dimethylbensimidazol. Den presenterar sig som en axiell som löper rakt ner från kobolt precis under korrinringen. Denna bensimidazol är också ansluten till ett fem kolsocker, som så småningom fäster sig till en fosfatgrupp och sedan remmar tillbaka till resten av strukturen. Eftersom axialen sträcker sig hela vägen ner är bindningen mellan kobolt och 5,6-dimetylbensimidazol svag och kan ibland ersättas med besläktade molekyler såsom en 5-hydrozylbensimidazol, en adenin eller någon annan liknande grupp. I den sjätte positionen ovanför Korrinringen kan den aktiva platsen för kobolt direkt ansluta till flera olika typer av ligander. Det kan ansluta till CN för att bilda en Cyanokobalami, till en metylgrupp för att bilda en metylkobalamin, till en 5′-deoxiadenosgrupp för att bilda en adenosylkobalamin och OH, Hydroxikobalamin. Kobolt är alltid redo att oxidera från 1+ förändring till 2+ och 3+ för att matcha dessa r-grupper som är anslutna till den. Till exempel innehåller hydroxokobalamin kobolt som har en 3+ laddning medan Metyladenosyl innehåller en kobolt som har en 1+ laddning.
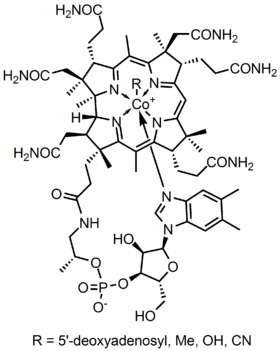
Figur 2
punktgruppskonfigurationen för kobalamin är C4v.för att bestämma denna symmetri måste man se att strukturen kan rotera sig fyra gånger och så småningom kommer tillbaka till sin ursprungliga position. Dessutom finns det inget sigma h-plan och ingen vinkelrätt C2-yxa. Men eftersom det finns Sigma v-plan som skär molekylerna i jämna delar är det tydligt att bestämma att strukturen av kobalamin är en C4v. med kobolt som molekylens mittmetall Bar kobalamin en förvrängd oktaedrisk konfiguration. Den axiella som förbinder kobolt till 5,6 dimetylbensimidazol sträcker sig hela vägen ner till botten. Dess avstånd är flera gånger längre än avståndet från kobolt och den bifogade R-gruppen ovanför den. Detta kan ibland också kallas en tetragonal struktur. Hela formen övergripande liknar en oktaedrisk, men de två axiella grupperna är olika och separerade i ojämna avstånd. Eftersom det bara finns ett metalloenzymcenter i systemet, tilldelas den punktgrupp och konfiguration som just nämnts också strukturen som helhet. Eftersom metallokoenzymstrukturen sträcks ut är den ganska svagt samordnad och kan brytas isär eller ersättas med andra grupper som nämnts ovan.
forskare har visat att både IR-och Raman-spektroskopi användes för att bestämma molekylens struktur. Detta bestäms genom att observera teckentabellerna för punktgrupp C4v, punktgruppssymmetrin för kobalamin. På IR-sidan kan man se att det finns grupper som drz, (x, y), (rz, ry). Å andra sidan finns det på Raman – sidan grupper som X-kvadrat +y-kvadrat, z-kvadrat, x-kvadrat-y-kvadrat, xy, xz, yz. Raman-sidan indikerade att det fanns sträckningslägen i molekylen och hänför sig tillbaka till sträckningen av 5,6-dimetylbensimidazolaxialen som anslöts direkt under Koboltmetallen. Sträckningen kan ses i Figur 3.
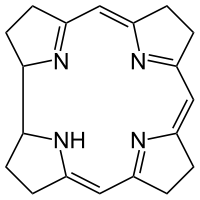
Figur 3
Kobalaminenzymer kan katalysera några olika typer av reaktioner. En av dem är reaktionen av intramolekylära omarrangemang. Under denna omläggning utbyts koenzym till de två grupperna som är fästa vid intilliggande kolatomer. En annan reaktion innefattar överföring av metylgruppen i vissa metyleringsreaktioner, såsom omvandling av homocystein till metionin, biosysntes av kolin och tymin etc. Dessa interaktioner kan ge fördelaktiga värden till de biologiska kropparna.
kobalamin har många fördelaktiga effekter när det gäller biologiska existenser. De spelar en roll för att upprätthålla ett hälsosamt kroppssystem och hjälpa till att hjälpa produktionen av kroppens genetiska material. Cyanokobalamin, en typ av kobalamin, arbetar för att generera bildandet av röda blodkroppar och läka många olika skador i nervsystemet. Kobalamin tjänar också som en viktig roll i metabolismen av fettsyror som är väsentliga för upprätthållandet av myelin. Studier har visat att personer med vitamin B12-brist kommer att avslöja oregelbunden förstörelse av myelin shealthen, vilket leder till parlys och död. Några av de andra symtomen på bristen på kobalamin är dålig tillväxt, megaloblastisk benmärg, förändringar i mag-tarmkanalen, Leucoopenia och hypersegmenterade nutrophills, degenerativa förändringar i ryggmärgen och nervsystemet och utsöndring av metylmalonsyra och homocystin i urinen.
genom åren har Vitamin B12 visat sig vara väsentligt för nervsystemet och produktionen av röda blodkroppar. En studie utförd av forskare vid National Institutes of Health, Trinity College Dublin, föreslog att en brist på Vitamin B12 kan öka risken för neuralrörsdefekt hos barn (Miller). Genom att studera kobalamins struktur och funktion kan forskare därför experimentera och bilda Vitamin B12 i sina laboratorier och tjäna samhället som helhet.